A+、B+、C–、D、E五种粒子(分子和离子)中,每个粒子均有10个电子。已知:①A++C–=E+D②B++C–=2D
(1)C–离子的电子式是_________
(2)具有相同空间构型的粒子______ 和______ ,E分子的空间构型为_________ ,_______ 性分子。
(3)分别写出A+和D反应、B+和E反应的离子方程式_____________ 、_____________ 。
(1)C–离子的电子式是
(2)具有相同空间构型的粒子
(3)分别写出A+和D反应、B+和E反应的离子方程式
更新时间:2020-03-06 17:18:28
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】铁触媒是重要的催化剂,CO易与铁触媒作用导致其失去催化活性:Fe+5CO=Fe(CO)5;除去CO的化学反应方程式为:[Cu(NH3)2]OOCCH3+CO+NH3=[Cu(NH3)3(CO)]OOCCH3。
请回答下列问题:
(1)C、N、O的电负性由大到小的顺序为_________________ ,基态Fe原子的价电子排布图为________________ 。
(2)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是__________ ,与CO互为等电子体的分子的电子式为_________________ 。
(3)配合物[Cu(NH3)2]OOCCH3中碳原子的杂化类型是_____________ ,配体中提供孤对电子的原子是___________________________________ 。
(4)用[Cu(NH3)2]OOCCH3除去CO的反应中,肯定有_______________ 形成。
a.离子键 b.配位键 c.非极性键 d.б键
(5)NaAlH4晶体的晶胞如图 ,与Na+紧邻且等距的AlH4-有
,与Na+紧邻且等距的AlH4-有___________ 个;NaAlH4晶体的密度为_________ g·cm-3(用含a的代数式表示)。
请回答下列问题:
(1)C、N、O的电负性由大到小的顺序为
(2)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是
(3)配合物[Cu(NH3)2]OOCCH3中碳原子的杂化类型是
(4)用[Cu(NH3)2]OOCCH3除去CO的反应中,肯定有
a.离子键 b.配位键 c.非极性键 d.б键
(5)NaAlH4晶体的晶胞如图
 ,与Na+紧邻且等距的AlH4-有
,与Na+紧邻且等距的AlH4-有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铜是应用较为广泛的有色金属。
(1)基态铜原子的价电子排布式为_____________ 。
(2)金属化合物Cu2Zn合金具有较高的熔点、较大的强度、硬度和耐磨度。则Cu2Zn合金的晶体类型是______ 。
(3)某含铜化合物的离子结构如图所示。

① 该离子中存在的作用力有__________ 。
a.离子键 b.共价键 c.配位键
d.氢键 e.范德华力
② 该离子中第二周期的非金属元素的第一电离能由大到小的顺序是______ 。
③ 该离子中N原子的杂化类型有_________ 。
(4)晶胞有两个基本要素:
① 原子坐标参数,表示晶胞内部各原子的相对位置,下图为铜与氧形成的某化合物晶胞,其中原子坐标参数A 为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0),则D原子的坐标参数为
,0),则D原子的坐标参数为_____________ 。
② 晶胞参数,描述晶胞的大小和形状,设晶胞的边长为apm,则O的配位数是_______ 。
(1)基态铜原子的价电子排布式为
(2)金属化合物Cu2Zn合金具有较高的熔点、较大的强度、硬度和耐磨度。则Cu2Zn合金的晶体类型是
(3)某含铜化合物的离子结构如图所示。

① 该离子中存在的作用力有
a.离子键 b.共价键 c.配位键
d.氢键 e.范德华力
② 该离子中第二周期的非金属元素的第一电离能由大到小的顺序是
③ 该离子中N原子的杂化类型有
(4)晶胞有两个基本要素:
① 原子坐标参数,表示晶胞内部各原子的相对位置,下图为铜与氧形成的某化合物晶胞,其中原子坐标参数A 为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0),则D原子的坐标参数为
,0),则D原子的坐标参数为② 晶胞参数,描述晶胞的大小和形状,设晶胞的边长为apm,则O的配位数是

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)据汞的原子结构示意图 ,汞在第
,汞在第___ 周期。
(2)NH3、H2O、H2S分别为氮、氧、硫3种元素对应的氢化物,其中沸点最高的是____ ,其中心原子杂化轨道类型:___ 。
(3)下列有关性质的比较能用元素周期律解释的是__ (填字母,下同)。
a.酸性:HCl>H2SO3
b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2
d.热稳定性:Na2CO3>NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是___ 。
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。
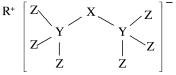
①R的元素符号为___ 。
②X的氢化物的电子式:___ 。
③写出Y的最高价氧化物的一种用途__ 。
(1)据汞的原子结构示意图
 ,汞在第
,汞在第(2)NH3、H2O、H2S分别为氮、氧、硫3种元素对应的氢化物,其中沸点最高的是
(3)下列有关性质的比较能用元素周期律解释的是
a.酸性:HCl>H2SO3
b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2
d.热稳定性:Na2CO3>NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①R的元素符号为
②X的氢化物的电子式:
③写出Y的最高价氧化物的一种用途
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有A、B、C、D四种主族元素,原子序数依次增大,A元素原子 轨道上有2个未成对电子。B元素原子的p轨道中有3个未成对电子,其简单气态氢化物在水中的溶解度在同族元素所形成的简单氢化物中最大。C的最高化合价和最低化合价的代数和为4,其最高价氧化物中含C的质量分数为40%,且其核内质子数等于中子数。D元素原子得一个电子填入
轨道上有2个未成对电子。B元素原子的p轨道中有3个未成对电子,其简单气态氢化物在水中的溶解度在同族元素所形成的简单氢化物中最大。C的最高化合价和最低化合价的代数和为4,其最高价氧化物中含C的质量分数为40%,且其核内质子数等于中子数。D元素原子得一个电子填入 轨道后,
轨道后, 轨道为全充满状态。请回答下列问题:
轨道为全充满状态。请回答下列问题:
(1) 分子中含有
分子中含有___________ 个 键,属于
键,属于___________ (填“极性”或“非极性”)分子。
(2)B的简单气态氢化物的立体构型为___________ , 原子采用
原子采用___________ 杂化。
(3)写出 的常见氧化物与
的常见氧化物与 的氧化物中互为等电子体的一组物质:
的氧化物中互为等电子体的一组物质:___________ 。
(4)C元素的电负性___________ (填“>”“<”或“=”)D元素的电负性,用一个化学方程式表示:___________ 。
 轨道上有2个未成对电子。B元素原子的p轨道中有3个未成对电子,其简单气态氢化物在水中的溶解度在同族元素所形成的简单氢化物中最大。C的最高化合价和最低化合价的代数和为4,其最高价氧化物中含C的质量分数为40%,且其核内质子数等于中子数。D元素原子得一个电子填入
轨道上有2个未成对电子。B元素原子的p轨道中有3个未成对电子,其简单气态氢化物在水中的溶解度在同族元素所形成的简单氢化物中最大。C的最高化合价和最低化合价的代数和为4,其最高价氧化物中含C的质量分数为40%,且其核内质子数等于中子数。D元素原子得一个电子填入 轨道后,
轨道后, 轨道为全充满状态。请回答下列问题:
轨道为全充满状态。请回答下列问题:(1)
 分子中含有
分子中含有 键,属于
键,属于(2)B的简单气态氢化物的立体构型为
 原子采用
原子采用(3)写出
 的常见氧化物与
的常见氧化物与 的氧化物中互为等电子体的一组物质:
的氧化物中互为等电子体的一组物质:(4)C元素的电负性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有A、B、C、D、E五种单核微粒:A原子核内有7个质子,7个中子,核外有7个电子;B微粒其电子层结构与氖原子相同,但其电子数比质子数多2个;C微粒核电荷数为11,并带有一个单位的正电荷;D微粒核外有10个电子,当得到2个电子后微粒呈电中性;E微粒呈电中性且核内无中子。
(1)依次写出A、B、C、D四种微粒的符号:_______ 、_______ 、_______ 、_______ 。
(2)写出两种由上述元素组成的含有10个电子的多核微粒的符号_______ 、_______ 。
(1)依次写出A、B、C、D四种微粒的符号:
(2)写出两种由上述元素组成的含有10个电子的多核微粒的符号
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)已知阳离子M2+的原子核内有n个中子,M原子的质量数为A,则a克M2+中所含电子的物质的量是____ mol。
(2)向1L1mol/L的NaOH溶液中通入0.6molCO2,所得溶液中Na2CO3与NaHCO3物质的量浓度之比为____ 。
(1)已知阳离子M2+的原子核内有n个中子,M原子的质量数为A,则a克M2+中所含电子的物质的量是
(2)向1L1mol/L的NaOH溶液中通入0.6molCO2,所得溶液中Na2CO3与NaHCO3物质的量浓度之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)26Al和27Al_______(选填编号)。
(2)碳元素的一种核素也可以考古断代,其原子符号为_______ ;
(3)10 g10Be所含的中子数与质子数之差为_______ 个。
(4)自然界一共存在三种硅的稳定同位素,分别是28Si、29Si和30Si。计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素的_______ 。硅原子的结构示意图为 _______ ,核外能量最高的电子位于_______ (填电子层符号)层。
(1)26Al和27Al_______(选填编号)。
| A.是同一种元素 | B.是同一种核素 | C.具有相同的中子数 | D.具有相同的化学性质 |
(3)10 g10Be所含的中子数与质子数之差为
(4)自然界一共存在三种硅的稳定同位素,分别是28Si、29Si和30Si。计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素的
您最近一年使用:0次



