回答下列问题:
(1)已知阳离子M2+的原子核内有n个中子,M原子的质量数为A,则a克M2+中所含电子的物质的量是____ mol。
(2)向1L1mol/L的NaOH溶液中通入0.6molCO2,所得溶液中Na2CO3与NaHCO3物质的量浓度之比为____ 。
(1)已知阳离子M2+的原子核内有n个中子,M原子的质量数为A,则a克M2+中所含电子的物质的量是
(2)向1L1mol/L的NaOH溶液中通入0.6molCO2,所得溶液中Na2CO3与NaHCO3物质的量浓度之比为
更新时间:2022-04-04 12:57:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)下列五个反应
A.5Cl2+I2+6H2O=10HCl+2HIO3
B.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
C.2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O
D.2NaCl+2H2O 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
E.MnO2+4HCl MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
上述反应中氯元素只被氧化的是_____________ ,(填字母,下同)只被还原的是_____________ ,部分被氧化的是_____________ ,C中被氧化与被还原的物质的量之比为_____________ 。
(2)在反应4(NH4)2SO4 N2↑+6NH3↑+3SO2↑+SO3↑+7H2O中,氧化产物与还原产物的物质的量之比为
N2↑+6NH3↑+3SO2↑+SO3↑+7H2O中,氧化产物与还原产物的物质的量之比为___________ ,生成56gN2转移的电子___________ mol。
(3)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10A1+6NaNO3+4NaOH==10NaA1O2+3N2↑+2H2O。上述反应中,若产生2mol N2,转移电子数为_________ (用NA表示阿伏伽德罗常数);用“双线桥”表示反应中电子转移,化合价的变化,反应类型:______________ 。
(4)将等质量的两份镁、铝合金分别投入足量的NaOH和HCl中,在相同的情况下测得生成气体的体积之比为1:2,求合金中镁、铝的物质的量之比为___________ 。
A.5Cl2+I2+6H2O=10HCl+2HIO3
B.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
C.2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O
D.2NaCl+2H2O
 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑ E.MnO2+4HCl
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O 上述反应中氯元素只被氧化的是
(2)在反应4(NH4)2SO4
 N2↑+6NH3↑+3SO2↑+SO3↑+7H2O中,氧化产物与还原产物的物质的量之比为
N2↑+6NH3↑+3SO2↑+SO3↑+7H2O中,氧化产物与还原产物的物质的量之比为(3)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10A1+6NaNO3+4NaOH==10NaA1O2+3N2↑+2H2O。上述反应中,若产生2mol N2,转移电子数为
(4)将等质量的两份镁、铝合金分别投入足量的NaOH和HCl中,在相同的情况下测得生成气体的体积之比为1:2,求合金中镁、铝的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在标准状况下,由一氧化碳和二氧化碳组成的混合气体为6.72L,质量为12g,此混合物中一氧化碳和二氧化碳物质的量之比是____ ,碳原子和氧原子个数比是____ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知硫酸钠晶体(Na2SO4·10H2O)为1mol,请计算填空:
(1)钠离子的物质的量是_______ ,硫酸钠晶体的物质的量是_______ ;
(2)所含硫酸根离子的物质的量是_______ ,硫酸根离子的数目是_______ ;
(3)所含结晶水的物质的量是_______ ,所含氧原子的物质的量是_______ 。
(1)钠离子的物质的量是
(2)所含硫酸根离子的物质的量是
(3)所含结晶水的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】漂白粉是一种常用杀菌、消毒剂,其有效成分为次氯酸钙。如图为制取漂白粉的工业流程简图。

(1)流程Ⅰ得到浓度为80 g/L氢氧化钠溶液,其物质的量浓度是_______ mol/L。
(2)流程 Ⅱ的反应条件(2)是_______ 。
(3)流程 Ⅲ中发生两个反应,写出其中一个的氧化还原反应的方程式:_______ 。
(4)流程 Ⅳ中操作b是_______ (写名称)。
(5)用化学方程式说明较纯的次氯酸钙粉末必须密封保存的原因:_______ 。

(1)流程Ⅰ得到浓度为80 g/L氢氧化钠溶液,其物质的量浓度是
(2)流程 Ⅱ的反应条件(2)是
(3)流程 Ⅲ中发生两个反应,写出其中一个的氧化还原反应的方程式:
(4)流程 Ⅳ中操作b是
(5)用化学方程式说明较纯的次氯酸钙粉末必须密封保存的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求回答问题
(1) KAl(SO4)2的电离方程式_______________________ 。
(2)向石蕊试液中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是______________ 、_________________ (填微粒符号)。
(3) 实验室用质量分数为36.5%,密度为1.19g·cm-3的浓盐酸来配制100ml,2mol/L的稀盐酸,需要用量筒量取_______________ ml 该浓盐酸。
(4)化学方程式H2S+H2SO4(浓)=SO2↑+S↓+2H2O,当生成4.48L (标况) SO2时,转移的电子是__________ mol。
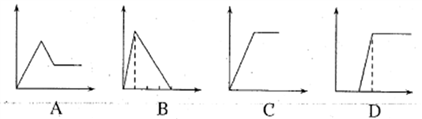
(5)下列四个图象中,横坐标表示加入物质的物质的量,纵坐标表示生成沉淀的量或产生气体的量,从A~D中选择符合各题要求的序号填人表中。
(1) KAl(SO4)2的电离方程式
(2)向石蕊试液中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是
(3) 实验室用质量分数为36.5%,密度为1.19g·cm-3的浓盐酸来配制100ml,2mol/L的稀盐酸,需要用量筒量取
(4)化学方程式H2S+H2SO4(浓)=SO2↑+S↓+2H2O,当生成4.48L (标况) SO2时,转移的电子是
(5)下列四个图象中,横坐标表示加入物质的物质的量,纵坐标表示生成沉淀的量或产生气体的量,从A~D中选择符合各题要求的序号填人表中。

溶液 | 加入的物质 | 序号 |
①AlCl3溶液 | 通入过量的NH3 | |
②Na2CO3和NaOH的溶液 | 滴入过量的盐酸 | |
③NaAlO2溶液 | 滴加稀硫酸至过量 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题。
(1)下列物质中:①SO2;②液态氯化氢;③CH4;④熔融NaOH;⑤NH4Cl固体;⑥氨水。属于混合物的是___________ (填序号,下同);能导电的是___________ ;属于电解质的是___________ ;属于非电解质的是___________ 。分别写出④和⑤的电离方程式:___________ 。
(2)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常见的消毒药品:84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。回答下面问题:
①过氧乙酸(CH3COOOH)的摩尔质量是___________ 。38gCH3COOOH中含有的O原子数为___________ NA,含有的H原子的物质的量为___________ 。
②过氧化氢(H2O2)极易分解,在MnO2催化作用下能完全分解为水和氧气,写出其化学方程式___________ 。过氧化氢的水溶液叫双氧水,2mol/L的双氧水500mL完全分解生成氧气的体积为___________ L(标准状态),转移电子数为___________ NA
③在相同状态下质量相同的臭氧和氯气,他们的物质的量之比为___________ ,原子个数之比为___________ ,密度之比为___________ 。
④84消毒液的有效成分为NaClO,同时还含有少量的NaCl,某84消毒液有效氯含量为3.55%,密度1.0g/mL,将此溶液稀释200倍后进行使用,此时c(NaClO) =___________ mol/L。
(1)下列物质中:①SO2;②液态氯化氢;③CH4;④熔融NaOH;⑤NH4Cl固体;⑥氨水。属于混合物的是
(2)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常见的消毒药品:84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。回答下面问题:
①过氧乙酸(CH3COOOH)的摩尔质量是
②过氧化氢(H2O2)极易分解,在MnO2催化作用下能完全分解为水和氧气,写出其化学方程式
③在相同状态下质量相同的臭氧和氯气,他们的物质的量之比为
④84消毒液的有效成分为NaClO,同时还含有少量的NaCl,某84消毒液有效氯含量为3.55%,密度1.0g/mL,将此溶液稀释200倍后进行使用,此时c(NaClO) =
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】理解化学用语的内涵和外延,掌握背后的规律性内容,是步入化学学科的必经之路。请用相应的化学用语回答下列问题:
(1)1911年,卢瑟福在α粒子的散射实验中,用α粒子轰击氮原子核,发现了质子的存在,提出了原子的核式结构,该核反应为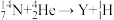 ,则Y的核素符号为
,则Y的核素符号为___________ 。
(2)Sr是第五周期第IIA族元素,用电子式表示SrF2的形成过程___________ 。
(3)汽车安全气囊中的主要物质为NaN3,此物质中共价键的类型为___________ 。
(4)元素周期表的第三周期元素中,最高价氧化物对应的水化物呈两性的是___________ (填元素符号,下同);最高价氧化物对应的水化物的酸性最强的是___________ 。
(1)1911年,卢瑟福在α粒子的散射实验中,用α粒子轰击氮原子核,发现了质子的存在,提出了原子的核式结构,该核反应为
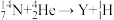 ,则Y的核素符号为
,则Y的核素符号为(2)Sr是第五周期第IIA族元素,用电子式表示SrF2的形成过程
(3)汽车安全气囊中的主要物质为NaN3,此物质中共价键的类型为
(4)元素周期表的第三周期元素中,最高价氧化物对应的水化物呈两性的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求写出下列微粒的化学符号。
(1)3个镁离子_______ 。
(2)质量数为35的氯离子_______ 。
(3)铝离子的结构示意图_______ 。
(4)硫离子的电子式_______ 。
(5)写一个含有10个电子的阳离子:_______ (化学符号)。
(6)写出氯酸钾的化学式,并标出其中氯元素的化合价:_______
(1)3个镁离子
(2)质量数为35的氯离子
(3)铝离子的结构示意图
(4)硫离子的电子式
(5)写一个含有10个电子的阳离子:
(6)写出氯酸钾的化学式,并标出其中氯元素的化合价:
您最近一年使用:0次