按要求回答问题
(1) KAl(SO4)2的电离方程式_______________________ 。
(2)向石蕊试液中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是______________ 、_________________ (填微粒符号)。
(3) 实验室用质量分数为36.5%,密度为1.19g·cm-3的浓盐酸来配制100ml,2mol/L的稀盐酸,需要用量筒量取_______________ ml 该浓盐酸。
(4)化学方程式H2S+H2SO4(浓)=SO2↑+S↓+2H2O,当生成4.48L (标况) SO2时,转移的电子是__________ mol。
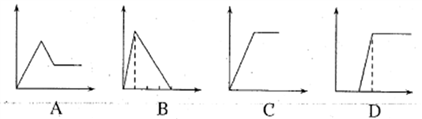
(5)下列四个图象中,横坐标表示加入物质的物质的量,纵坐标表示生成沉淀的量或产生气体的量,从A~D中选择符合各题要求的序号填人表中。
(1) KAl(SO4)2的电离方程式
(2)向石蕊试液中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是
(3) 实验室用质量分数为36.5%,密度为1.19g·cm-3的浓盐酸来配制100ml,2mol/L的稀盐酸,需要用量筒量取
(4)化学方程式H2S+H2SO4(浓)=SO2↑+S↓+2H2O,当生成4.48L (标况) SO2时,转移的电子是
(5)下列四个图象中,横坐标表示加入物质的物质的量,纵坐标表示生成沉淀的量或产生气体的量,从A~D中选择符合各题要求的序号填人表中。

溶液 | 加入的物质 | 序号 |
①AlCl3溶液 | 通入过量的NH3 | |
②Na2CO3和NaOH的溶液 | 滴入过量的盐酸 | |
③NaAlO2溶液 | 滴加稀硫酸至过量 |
更新时间:2018-01-17 17:22:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)标准状况下,1.7gNH3与___ LH2S气体含有的氢原子数相同。
(2)标准状况,NH3与CH4组成的混合气体的平均密度为0.75g·L-1,该混合气体的平均摩尔质量为___ ,NH3的体积分数为___ 。
(3)常温下,在27.9g水中溶解12.1gCu(NO3)2·3H2O,恰好达到饱和。设该溶液密度为1.20g·cm-3。
求:①溶质的质量分数为___ 。
②该溶液中NO 的物质的量浓度为
的物质的量浓度为___ 。
③取出20.0mL该溶液,配成浓度为1.00mol·L-1的稀溶液,则稀释后溶液的体积是___ mL。
④将一根质量为100g的铁棒插入到该溶液中,一段时间后取出,洗净、干燥后称量,铁棒的质量变为100.2g,此时溶液中Fe(NO3)2的物质的量浓度是___ (忽略溶液体积的变化)。
(1)标准状况下,1.7gNH3与
(2)标准状况,NH3与CH4组成的混合气体的平均密度为0.75g·L-1,该混合气体的平均摩尔质量为
(3)常温下,在27.9g水中溶解12.1gCu(NO3)2·3H2O,恰好达到饱和。设该溶液密度为1.20g·cm-3。
求:①溶质的质量分数为
②该溶液中NO
 的物质的量浓度为
的物质的量浓度为③取出20.0mL该溶液,配成浓度为1.00mol·L-1的稀溶液,则稀释后溶液的体积是
④将一根质量为100g的铁棒插入到该溶液中,一段时间后取出,洗净、干燥后称量,铁棒的质量变为100.2g,此时溶液中Fe(NO3)2的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】填空:
(1)0. 5 mol NH3分子中所含氮原子数为__________ 个;
(2)1.2g RSO4中含0.01 mol R2+,则RSO4的摩尔质量是__________ ;
(3)0.1 mol·L-1的 Cu(NO3)2溶液中NO3-的物质的量浓度是__________ ;
(4)新制氯水在阳光照射下产生的无色气体是__________ ;
(5)配制100 mL 1 mol/L NaCl溶液,定容后,把容量瓶倒置摇匀后发现液面低于刻度线,补加水至刻度处,会引起所配溶液物质的量浓度__________ (选填“偏高、偏低、无影响”);
(6)实验室制备氯气时,收集氯气常采用__________ 法。
(1)0. 5 mol NH3分子中所含氮原子数为
(2)1.2g RSO4中含0.01 mol R2+,则RSO4的摩尔质量是
(3)0.1 mol·L-1的 Cu(NO3)2溶液中NO3-的物质的量浓度是
(4)新制氯水在阳光照射下产生的无色气体是
(5)配制100 mL 1 mol/L NaCl溶液,定容后,把容量瓶倒置摇匀后发现液面低于刻度线,补加水至刻度处,会引起所配溶液物质的量浓度
(6)实验室制备氯气时,收集氯气常采用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
Ⅰ.现有下列10种物质:①NaHSO4固体②Ba(OH)2溶液③Cu ④酒精 ⑤烧碱 ⑥熔融KNO3 ⑦稀硝酸 ⑧硫酸 ⑨液态HCl ⑩氨气,回答下列问题:
(1)上述物质中能导电的是_______________ (填序号,下同);
(2)属于电解质的是________________ ,属于非电解质的是_______________ ;
(3)将②加入①的水溶液中至刚好沉淀完全的的离子方程式:____________________ 。
Ⅱ根据所学知识,完成相关题目:
(4)0.4 mol NH3分子中所含H原子数与______ 个H2O分子中所含H原子数相等。
(5)配制 240mL 0.2 mol·L-1 的碳酸钠溶液,应用托盘天平称取_____ g Na2CO3固体。
(6)某实验小组人员用质量分数为98 %,密度为1.84 g/cm3的浓硫酸配制100 mL 2.3 mol/L的稀硫酸。该浓硫酸的浓度为________ mol/L,需量取浓硫酸的体积为__________ mL。
Ⅰ.现有下列10种物质:①NaHSO4固体②Ba(OH)2溶液③Cu ④酒精 ⑤烧碱 ⑥熔融KNO3 ⑦稀硝酸 ⑧硫酸 ⑨液态HCl ⑩氨气,回答下列问题:
(1)上述物质中能导电的是
(2)属于电解质的是
(3)将②加入①的水溶液中至刚好沉淀完全的的离子方程式:
Ⅱ根据所学知识,完成相关题目:
(4)0.4 mol NH3分子中所含H原子数与
(5)配制 240mL 0.2 mol·L-1 的碳酸钠溶液,应用托盘天平称取
(6)某实验小组人员用质量分数为98 %,密度为1.84 g/cm3的浓硫酸配制100 mL 2.3 mol/L的稀硫酸。该浓硫酸的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某化合物 A 由两种元素组成,可以发生如下的转化。
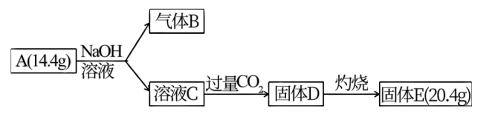
已知∶标准状况下,气体B的密度是氢气的8倍;固体E既溶于NaOH溶液又可溶于稀硫酸。
请回答∶
(1)B的化学式是______
(2)组成A的元素有______
(3)请写出 A 与 NaOH溶液反应的化学方程式_______

已知∶标准状况下,气体B的密度是氢气的8倍;固体E既溶于NaOH溶液又可溶于稀硫酸。
请回答∶
(1)B的化学式是
(2)组成A的元素有
(3)请写出 A 与 NaOH溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铝、铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)向盐酸中滴加偏铝酸钠至过量,写出该过程的离子方程式:________ 、___________ 。
(2)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2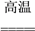 6SO2+Fe3O4,有6 mol FeS2参加反应,转移
6SO2+Fe3O4,有6 mol FeS2参加反应,转移________ mol电子。
(3)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为_______ ;从腐蚀废液回收得到金属铜,还需要的试剂是_______ 。
(1)向盐酸中滴加偏铝酸钠至过量,写出该过程的离子方程式:
(2)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2
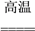 6SO2+Fe3O4,有6 mol FeS2参加反应,转移
6SO2+Fe3O4,有6 mol FeS2参加反应,转移(3)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求填空:
(1)下列物质中:①能导电的是________ (填代号,以下同);
②属于电解质的是____________ ;
③属于非电解质的是____________ 。
A.NaOH 溶液 B.Cu C.液态HCl D.蔗糖溶液
E.液氯 F.氨水 G.胆矾晶体 H.无水乙醇
(2)若将0.2mol 钠、镁、铝分别投入到100mL 1mol·L-1的盐酸中,在标准状况下,产生氢气体积之比是_____________ 。
(3)取等质量的铁硅合金样品两份,分别投入到足量的稀盐酸和足量的稀氢氧化钠溶液中,充分反应后,收集到等量的氢气,则原合金样品中铁和硅的物质的量之比为______________________ 。
(4)向盛有10mL1mol·L-1NH4Al(SO4)2溶液的烧杯中滴加1mol·L-1NaOH 溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
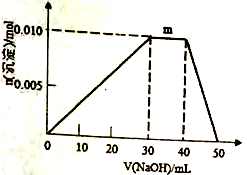
①写出m点反应的离子方程式____________________________________ 。
②若NH4Al(SO4)2溶液改加20mL1.2mol/LBa(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为________ mol。
(1)下列物质中:①能导电的是
②属于电解质的是
③属于非电解质的是
A.NaOH 溶液 B.Cu C.液态HCl D.蔗糖溶液
E.液氯 F.氨水 G.胆矾晶体 H.无水乙醇
(2)若将0.2mol 钠、镁、铝分别投入到100mL 1mol·L-1的盐酸中,在标准状况下,产生氢气体积之比是
(3)取等质量的铁硅合金样品两份,分别投入到足量的稀盐酸和足量的稀氢氧化钠溶液中,充分反应后,收集到等量的氢气,则原合金样品中铁和硅的物质的量之比为
(4)向盛有10mL1mol·L-1NH4Al(SO4)2溶液的烧杯中滴加1mol·L-1NaOH 溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:

①写出m点反应的离子方程式
②若NH4Al(SO4)2溶液改加20mL1.2mol/LBa(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铝及其化合物在生产、生活中有重要应用。
(1)铝是一种重要的金属元素,在周期表中位于第________ 周期________ 族.
(2)钢制品镀铝后能有效防止钢材腐蚀,为测定镀层的厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6 mol电子时,所得还原产物的物质的量为________ mol。
(3)工业上常用铝土矿(含SiO2等杂质)生产铝。从Na2SiO3和NaAlO2混合溶液中制得Al(OH)3,需要从下列试剂中选择两种,选用的试剂组合最好是_________ 。
a. NaOH溶液 b.氨水 c. CO2 d. 盐酸
(4)请完成(3)中涉及到的离子方程式:_______________ 、______________ 、________________ 。
(5)铝能与氢氧化钠溶液反应,硅也可以发生类似反应,请写出硅与氢氧化钠溶液反应的化学方程式____________________ 。
(1)铝是一种重要的金属元素,在周期表中位于第
(2)钢制品镀铝后能有效防止钢材腐蚀,为测定镀层的厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6 mol电子时,所得还原产物的物质的量为
(3)工业上常用铝土矿(含SiO2等杂质)生产铝。从Na2SiO3和NaAlO2混合溶液中制得Al(OH)3,需要从下列试剂中选择两种,选用的试剂组合最好是
a. NaOH溶液 b.氨水 c. CO2 d. 盐酸
(4)请完成(3)中涉及到的离子方程式:
(5)铝能与氢氧化钠溶液反应,硅也可以发生类似反应,请写出硅与氢氧化钠溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.根据下表左边的“实验操作”,从右边的“实验现象”中选择正确的字母代号,填入对应“答案”的空格中。
Ⅱ.某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案。
(1)提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成。
(2)设计实验:①利用下图装置分别对一定量的Na2CO3和NaHCO3进行加热;②为了检验CO2的生成,试管B中应加入的物质是_____________ 。
(3)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有_______________ 沉淀生成(填沉淀的颜色),说明Na2CO3和NaHCO3的热稳定性是:Na2CO3_______ NaHCO3(填“>”或“<”)。
(4)某同学在探究NaHCO3的热稳定性时,称取了8.4gNaHCO3,充分加热,请你计算理论上可产生CO2气体的体积为__________ L(标准状况)。
| 实验操作 | 答案 | 实验现象 |
| (1)让一束光线通过Fe(OH)3胶体 | A.呈蓝色 B.生成白色胶状沉淀 C.呈现光亮“通路” D.产生红褐色沉淀 | |
| (2)向盛有FeCl3溶液的试管中加入NaOH溶液 | ||
| (3)向Al2(SO4)3溶液中滴加氨水 | ||
| (4)向土豆片上滴加碘水 |
Ⅱ.某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案。
(1)提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成。
(2)设计实验:①利用下图装置分别对一定量的Na2CO3和NaHCO3进行加热;②为了检验CO2的生成,试管B中应加入的物质是
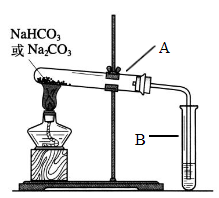
(3)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有
(4)某同学在探究NaHCO3的热稳定性时,称取了8.4gNaHCO3,充分加热,请你计算理论上可产生CO2气体的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。
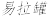
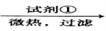

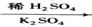
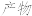
回答下列问题:
(1)为尽量少引入杂质,试剂①应选用NaOH溶液,若选用H2SO4溶液,其后果是________________________ 。
(2)易拉罐溶解过程中主要反应的化学方程式为____________________________ ;滤液A中的某种离子与NH4+、HCO3-均能反应生成沉淀B,该离子与NH4+反应的离子方程式为_____________________________________________ 。
(3)明矾与硫磺焙烧时发生反应的化学方程式为:KAl(SO4)2·12H2O+S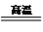 K2SO4+Al2O3+SO2↑+H2O(未配平),配平后的化学计量数依次为
K2SO4+Al2O3+SO2↑+H2O(未配平),配平后的化学计量数依次为___________________________ ;每生成67.2L标准状况下的SO2,转移电子的物质的量为________ ;焙烧产生的SO2经催化氧化、吸收等过程可制得硫酸,若SO2催化氧化时的转化率为96.0%,则理论上用该法生成硫酸时硫元素的总转化率为__________ 。
(4)实验室需要用1mol/L的KAl(SO4)2溶液225ml,用明矾配制用到的玻璃仪器有____________________________________ 。
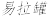
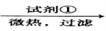

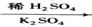
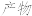
回答下列问题:
(1)为尽量少引入杂质,试剂①应选用NaOH溶液,若选用H2SO4溶液,其后果是
(2)易拉罐溶解过程中主要反应的化学方程式为
(3)明矾与硫磺焙烧时发生反应的化学方程式为:KAl(SO4)2·12H2O+S
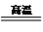 K2SO4+Al2O3+SO2↑+H2O(未配平),配平后的化学计量数依次为
K2SO4+Al2O3+SO2↑+H2O(未配平),配平后的化学计量数依次为(4)实验室需要用1mol/L的KAl(SO4)2溶液225ml,用明矾配制用到的玻璃仪器有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】消毒剂因能杀灭病原微生物、切断传染病的传播途径而在生活中广泛应用。过氧乙酸(一元弱酸)、“84”消毒液、二氧化氯 、
、 、
、 等均是生活中常见消毒剂。
等均是生活中常见消毒剂。
(1)下列消毒剂属于电解质的是_______。
(2)写出 的电离方程式
的电离方程式_______ 。
(3)解释“84”消毒液与洁厕灵(主要成分是盐酸)不能混合使用的原因_______ 。
(4)将氯气转化为液氯的过程中,说法错误的是_______。
(5)氯气与下列物质反应时,氯原子只得到电子的是_______。
(6)下列实验现象的“解释或结论”正确的是_______。
(7)在酸性介质中,次氯酸根与碘离子反应,析出碘。反应如下:
请标出电子转移的方向和数目_______ 。
(8)消毒效率可用单位质量消毒剂的得电子数来表示。计算 的消毒效率约是氯气的
的消毒效率约是氯气的_______ 倍。(保留到小数点后两位)
(9)用固体 通过下列转化过程能制得某种具有消毒作用的气体。下列说法错误的是_______。
通过下列转化过程能制得某种具有消毒作用的气体。下列说法错误的是_______。

已知:过程中锰元素最终转化为
 、
、 、
、 等均是生活中常见消毒剂。
等均是生活中常见消毒剂。(1)下列消毒剂属于电解质的是_______。
A. | B.过氧乙酸 | C. | D.“84”消毒液 |
(2)写出
 的电离方程式
的电离方程式(3)解释“84”消毒液与洁厕灵(主要成分是盐酸)不能混合使用的原因
(4)将氯气转化为液氯的过程中,说法错误的是_______。
| A.需要降温或加压 | B.氯分子间的平均距离减小 |
| C.氯分子数目减小 | D.氯分子间的作用力减小 |
(5)氯气与下列物质反应时,氯原子只得到电子的是_______。
| A.Cu | B. | C. | D. |
(6)下列实验现象的“解释或结论”正确的是_______。
| 选项 | 实验现象 | 解释或结论 |
| A | 氯气能使湿润的淀粉KI试纸变蓝:氯气能使 溶液变橙色 溶液变橙色 | 氧化性: |
| B | 氧气能使湿润的蓝色石蕊试纸先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | 氯气通入 的水溶液中,溶液的导电能力增强 的水溶液中,溶液的导电能力增强 | 氯气是强电解质 |
| D | 氧气通入 溶液中,溶液变棕黄色 溶液中,溶液变棕黄色 | 氧化性: |
| A.A | B.B | C.C | D.D |
(7)在酸性介质中,次氯酸根与碘离子反应,析出碘。反应如下:

请标出电子转移的方向和数目
(8)消毒效率可用单位质量消毒剂的得电子数来表示。计算
 的消毒效率约是氯气的
的消毒效率约是氯气的(9)用固体
 通过下列转化过程能制得某种具有消毒作用的气体。下列说法错误的是_______。
通过下列转化过程能制得某种具有消毒作用的气体。下列说法错误的是_______。
已知:过程中锰元素最终转化为

| A.G与H均为氧化产物 | B.实验中 只作氧化剂 只作氧化剂 |
| C.实验中浓盐酸体现出酸性和还原性 | D.G与H的物质的量之和可能为 |
您最近一年使用:0次
【推荐2】《天工开物》中记载了以炉甘石为原料炼锌的方法,发生的化学反应之一: 。
。
(1)作氧化剂的物质是______ ,碳元素的化合价______ (填“升高”或“降低”)。
(2)反应中每生成1molZn,消耗CO的物质的量是______ mol,转移电子的物质的量是______ mol。
 。
。(1)作氧化剂的物质是
(2)反应中每生成1molZn,消耗CO的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为: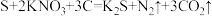 。该反应中,被还原的元素是
。该反应中,被还原的元素是_______ (元素符号)。
(2)饮用水中的NO 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,可以在碱性条件下用铝粉将NO
的浓度,可以在碱性条件下用铝粉将NO 还原为N2,其化学方程式为:10Al + 6NaNO3 + 4NaOH = 10NaAlO2 + 3N2↑ + 2 H2O。请回答下列问题:
还原为N2,其化学方程式为:10Al + 6NaNO3 + 4NaOH = 10NaAlO2 + 3N2↑ + 2 H2O。请回答下列问题:
①上述反应中,被氧化的元素_______ ,还原产物是_______ 。
②用双线桥法表示上述反应中电子转移的方向和数目:_______ 。
(3) 是高效、绿色的水处理剂,其原理如图所示。请回答下列问题:
是高效、绿色的水处理剂,其原理如图所示。请回答下列问题:

①高铁酸钾( )属于
)属于_______ (“酸”、“碱”、“盐”或“氧化物”),其中铁的化合价为_______ 价。
②过程a中 体现
体现_______ (填“氧化“或“还原”)性,反应过程中消耗1个 转移电子数
转移电子数_______ 。
(4)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体Cl2。请将方程式补充完整:_______ 。
_______NaClO+_______HCl(浓) =_______NaCl+_______Cl2↑+_______H2O
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:
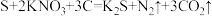 。该反应中,被还原的元素是
。该反应中,被还原的元素是(2)饮用水中的NO
 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,可以在碱性条件下用铝粉将NO
的浓度,可以在碱性条件下用铝粉将NO 还原为N2,其化学方程式为:10Al + 6NaNO3 + 4NaOH = 10NaAlO2 + 3N2↑ + 2 H2O。请回答下列问题:
还原为N2,其化学方程式为:10Al + 6NaNO3 + 4NaOH = 10NaAlO2 + 3N2↑ + 2 H2O。请回答下列问题:①上述反应中,被氧化的元素
②用双线桥法表示上述反应中电子转移的方向和数目:
(3)
 是高效、绿色的水处理剂,其原理如图所示。请回答下列问题:
是高效、绿色的水处理剂,其原理如图所示。请回答下列问题:
①高铁酸钾(
 )属于
)属于②过程a中
 体现
体现 转移电子数
转移电子数(4)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体Cl2。请将方程式补充完整:
_______NaClO+_______HCl(浓) =_______NaCl+_______Cl2↑+_______H2O
您最近一年使用:0次



