铝、铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)向盐酸中滴加偏铝酸钠至过量,写出该过程的离子方程式:________ 、___________ 。
(2)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2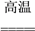 6SO2+Fe3O4,有6 mol FeS2参加反应,转移
6SO2+Fe3O4,有6 mol FeS2参加反应,转移________ mol电子。
(3)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为_______ ;从腐蚀废液回收得到金属铜,还需要的试剂是_______ 。
(1)向盐酸中滴加偏铝酸钠至过量,写出该过程的离子方程式:
(2)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2
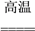 6SO2+Fe3O4,有6 mol FeS2参加反应,转移
6SO2+Fe3O4,有6 mol FeS2参加反应,转移(3)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为
更新时间:2017-12-19 21:39:37
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)向含有Cr2O72-的酸性废水中滴加硫酸亚铁溶液生成Cr3+,反应的离子方程式为____
(2)FeO·Cr2O3+Na2CO3+NaNO3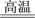 Na2CrO4+Fe2O3+CO2+NaNO2 该反应配平后FeO·Cr2O3与NaNO3的系数比为
Na2CrO4+Fe2O3+CO2+NaNO2 该反应配平后FeO·Cr2O3与NaNO3的系数比为________________ 。
(3)FePO4、Li2CO3、H2C2O4混合后高温煅烧制LiFePO4的化学方程式为_____________
(4)用NaOH、H2O2的混合溶液吸收ClO2生产NaClO2,氧化剂与还原剂的物质的量之比为________ 。
(2)FeO·Cr2O3+Na2CO3+NaNO3
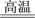 Na2CrO4+Fe2O3+CO2+NaNO2 该反应配平后FeO·Cr2O3与NaNO3的系数比为
Na2CrO4+Fe2O3+CO2+NaNO2 该反应配平后FeO·Cr2O3与NaNO3的系数比为(3)FePO4、Li2CO3、H2C2O4混合后高温煅烧制LiFePO4的化学方程式为
(4)用NaOH、H2O2的混合溶液吸收ClO2生产NaClO2,氧化剂与还原剂的物质的量之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空
(1)在S2-、Fe2+、Fe、Mg2+、H2S、I-、H+中,既有氧化性又有还原性的是________ 。
(2)实验室可用以下反应制备氯气:KClO3+6HCl(浓)= KCl+ 3Cl2↑+3H2O。反应中有1 mol电子转移时制得氯气44g,则反应物可能的组合是_______________
A.K35ClO3+6H35Cl B.K35ClO3+6H37Cl
C.K37ClO3+6H35Cl D.K37ClO3+6H37Cl
(3)将57.6 g的Cu片加入50 mL 18 mol/L的H2SO4溶液中并加热,被还原的H2SO4的物质的量为_________ (填“>”、“=”、“<”)0.45 mol
(4)火箭发射时以肼(N2H4)为燃料,也可以用一氧化氮作氧化剂,在此反应过程中若转移2 mol电子,则消耗燃料肼的质量为_______ 。
(5)已知溶液中含有以下离子: 、
、 、
、 、
、 、
、 、CH3COO-、Na+当加入足量Na2O2固体后,离子浓度几乎保持不变的是
、CH3COO-、Na+当加入足量Na2O2固体后,离子浓度几乎保持不变的是___________ 。
(1)在S2-、Fe2+、Fe、Mg2+、H2S、I-、H+中,既有氧化性又有还原性的是
(2)实验室可用以下反应制备氯气:KClO3+6HCl(浓)= KCl+ 3Cl2↑+3H2O。反应中有1 mol电子转移时制得氯气44g,则反应物可能的组合是
A.K35ClO3+6H35Cl B.K35ClO3+6H37Cl
C.K37ClO3+6H35Cl D.K37ClO3+6H37Cl
(3)将57.6 g的Cu片加入50 mL 18 mol/L的H2SO4溶液中并加热,被还原的H2SO4的物质的量为
(4)火箭发射时以肼(N2H4)为燃料,也可以用一氧化氮作氧化剂,在此反应过程中若转移2 mol电子,则消耗燃料肼的质量为
(5)已知溶液中含有以下离子:
 、
、 、
、 、
、 、
、 、CH3COO-、Na+当加入足量Na2O2固体后,离子浓度几乎保持不变的是
、CH3COO-、Na+当加入足量Na2O2固体后,离子浓度几乎保持不变的是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】磷是重要的元素,能形成多种含氧酸和含氧酸盐。回答下列问题:
Ⅰ. 亚磷酸(H3PO3)是二元酸,H3PO3溶液存在电离平衡:H3PO3 H+ + H2PO
H+ + H2PO 。亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3。
。亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3。
(1)写出亚磷酸钠(Na2HPO3)中磷的化合价___________ 。
(2)当亚磷酸与少量NaOH溶液反应的离子方程式为___________ 。
(3)亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式___________ 。
Ⅱ.已知:①次磷酸(H3PO2)是一种一元弱酸;
②常温下,电离平衡常数Ka(H3PO2)=5.9×10-2,Ka(CH3COOH)=1.8×10-5;
(4)下列说法正确的是___________。
(5)次磷酸钠NaH2PO2具有强还原性,是一种很好的化学镀剂。如NaH2PO2能将溶液中的Ni2+还原为Ni,用于化学镀镍。酸性条件下镀镍溶液中发生如下反应:____
___________Ni2++___________H2PO +___________(___________)═___________Ni+___________H2PO
+___________(___________)═___________Ni+___________H2PO +_______(___________)请完成并配平上列的离子方程式。
+_______(___________)请完成并配平上列的离子方程式。
Ⅲ.磷酸是三元弱酸(H3PO4)
(6)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为: 2Ca3(PO4)2+6SiO2 6CaSiO3+P4O10 10C+P4O10
6CaSiO3+P4O10 10C+P4O10  P4+10CO
P4+10CO
若反应生成31 g P4,则反应过程中转移的电子数为___________ (用NA表示阿伏加德罗常数的值)。
Ⅰ. 亚磷酸(H3PO3)是二元酸,H3PO3溶液存在电离平衡:H3PO3
 H+ + H2PO
H+ + H2PO 。亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3。
。亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3。(1)写出亚磷酸钠(Na2HPO3)中磷的化合价
(2)当亚磷酸与少量NaOH溶液反应的离子方程式为
(3)亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式
Ⅱ.已知:①次磷酸(H3PO2)是一种一元弱酸;
②常温下,电离平衡常数Ka(H3PO2)=5.9×10-2,Ka(CH3COOH)=1.8×10-5;
(4)下列说法正确的是___________。
A.次磷酸的电离方程式为:H3PO2⇌H++H2PO |
| B.NaH2PO2属于酸式盐 |
| C.浓度均为0.1mol•L-1的次磷酸(H3PO2)与盐酸相比前者导电能力强 |
| D.0.1mol•L-1NaH2PO2溶液的pH比0.1mol•L-1CH3COONa溶液的pH小 |
___________Ni2++___________H2PO
 +___________(___________)═___________Ni+___________H2PO
+___________(___________)═___________Ni+___________H2PO +_______(___________)请完成并配平上列的离子方程式。
+_______(___________)请完成并配平上列的离子方程式。Ⅲ.磷酸是三元弱酸(H3PO4)
(6)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为: 2Ca3(PO4)2+6SiO2
 6CaSiO3+P4O10 10C+P4O10
6CaSiO3+P4O10 10C+P4O10  P4+10CO
P4+10CO若反应生成31 g P4,则反应过程中转移的电子数为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
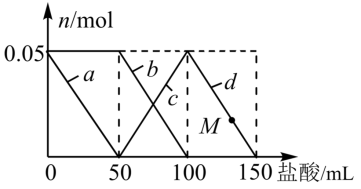
【推荐1】向100mL含Na2CO3、NaAlO2的混合溶液中逐滴加入HCl溶液,测得溶液中的某几种离子的物质的量的变化如图所示:
(1)已知 与
与 在溶液中反应而不能大量共存,写出两者反应的离子方程式:
在溶液中反应而不能大量共存,写出两者反应的离子方程式:___________ 。
(2)a和c曲线表示的离子分别是___________ 、___________ 。d曲线表示的离子方程式为___________ 。
(3)加入HCl溶液的物质的量浓度为___________ ,M点溶液中沉淀的质量为___________ 。
(4)原混合溶液中的Na+与 的物质的量之比为
的物质的量之比为___________ 。
(5)另取AlCl3溶液和NaOH溶液反应,当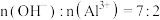 时,写出反应的离子方程式:
时,写出反应的离子方程式:___________ 。

(1)已知
 与
与 在溶液中反应而不能大量共存,写出两者反应的离子方程式:
在溶液中反应而不能大量共存,写出两者反应的离子方程式:(2)a和c曲线表示的离子分别是
(3)加入HCl溶液的物质的量浓度为
(4)原混合溶液中的Na+与
 的物质的量之比为
的物质的量之比为(5)另取AlCl3溶液和NaOH溶液反应,当
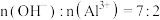 时,写出反应的离子方程式:
时,写出反应的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水中后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol·L-1HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示。试回答:
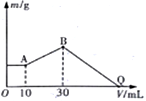
(1)A点沉淀物的化学式为_____________ ,A点溶液中的溶质是___________________ ;B点沉淀物的化学式为____________________ 。
(2)原混合物中MgCl2的物质的量为________________ ,AlCl3的物质的量为__________ ,NaOH的物质的量为________________ 。
(3)HCl溶液在Q点的加入量是____________________ 。

(1)A点沉淀物的化学式为
(2)原混合物中MgCl2的物质的量为
(3)HCl溶液在Q点的加入量是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】由短周期元素组成的中学常见的含钠元素的物质A、B、C、D,存在如图转化关系(部分生成物和反应条件已略去)。

(1)若A为过氧化钠,A与CO2反应的化学方程式为________ ,A与水反应的离子方程式为_____ 。
(2)①向饱和C溶液中通CO2,化学方程式为:_____ 。
②1mol/L的B溶液逐滴加入1L 1mol /L的AlCl3溶液中,产生白色沉淀39g,则所加入的B溶液的体积为_____ L。
(3)下列图象中,横坐标表示加入试剂或通入气体的物质的量,纵坐标表示产生沉淀或气体的质量,用图象的序号或文字回答下列问题:

I.表示向 Na2CO3和 NaHCO3的混合溶液中逐渐滴加稀盐酸的是_______________ ;
II.表示向 NaAlO2溶液中逐渐滴加稀盐酸的是_____ ;
III.表示向 NaAlO2溶液中通入 CO2的是_____ ;③图_____ (填“能”或“不能”)代表向含 NaOH 的澄清石灰水中通入 CO2。

(1)若A为过氧化钠,A与CO2反应的化学方程式为
(2)①向饱和C溶液中通CO2,化学方程式为:
②1mol/L的B溶液逐滴加入1L 1mol /L的AlCl3溶液中,产生白色沉淀39g,则所加入的B溶液的体积为
(3)下列图象中,横坐标表示加入试剂或通入气体的物质的量,纵坐标表示产生沉淀或气体的质量,用图象的序号或文字回答下列问题:

I.表示向 Na2CO3和 NaHCO3的混合溶液中逐渐滴加稀盐酸的是
II.表示向 NaAlO2溶液中逐渐滴加稀盐酸的是
III.表示向 NaAlO2溶液中通入 CO2的是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】某合金中铜和铁的物质的量均为0.3mol,将其全部投入bmL4mol/L的硝酸溶液中,使其充分反应(假设NO是唯一的还原产物)。
(1)若金属有剩余,其质量为m1g,在溶液中再滴入稀硫酸后,剩余金属为m2g,则m1与m2的关系为:m1_____ m2(填“>”、“<”或“=”)。
(2)若b=450mL,则溶液中的金属阳离子为________________ 。
(3)若合金与硝酸溶液恰好反应完全,求b的取值范围___________ (要有计算过程)
(1)若金属有剩余,其质量为m1g,在溶液中再滴入稀硫酸后,剩余金属为m2g,则m1与m2的关系为:m1
(2)若b=450mL,则溶液中的金属阳离子为
(3)若合金与硝酸溶液恰好反应完全,求b的取值范围
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用所给的工艺流程生产单质碘:
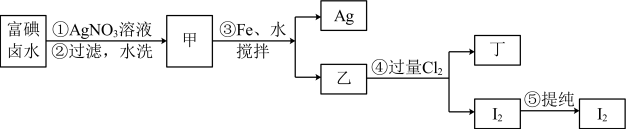
(1)碘位于元素周期表中的第___________ 周期第___________ 族。
(2)步骤③加Fe的目的是___________
(3)写出步骤④的化学方程式:___________ 。
(4)上述生产流程中,可以循环利用的副产物是,已知上述流程得到的该副产物含杂质,现需将其制成生产所需的试剂,先后还需加入___________ 、___________ 来进行处理。
(5)甲物质见光易变黑,其原因是(用化学方程式表示)___________ 。
(6)第⑤步操作可供提纯I2的两种方法是和___________ 、___________ 。

(1)碘位于元素周期表中的第
(2)步骤③加Fe的目的是
(3)写出步骤④的化学方程式:
(4)上述生产流程中,可以循环利用的副产物是,已知上述流程得到的该副产物含杂质,现需将其制成生产所需的试剂,先后还需加入
(5)甲物质见光易变黑,其原因是(用化学方程式表示)
(6)第⑤步操作可供提纯I2的两种方法是和
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)向某溶液中加入KSCN溶液无明显现象,再滴入数滴氯水后,溶液立即变成红色,则原溶液中一定含有________ 离子,要除去FeCl3溶液中少量的氯化亚铁,可行的办法是________ (填字母)。
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式
______________________________________________ 。
(2)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,写出FeCl3与金属铜反应的离子方程式_____________________________________________ 。
(3)向沸水中逐滴滴加1 mol·L-1FeCl3溶液至液体呈透明的红褐色,该分散系中微粒直径的范围是_________ ,区别该液体和FeCl3溶液可用_________________ 方法。
| A.加入铜粉 | B.加入铁粉 | C.通入氯气 | D.加入KSCN溶液 |
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式
(2)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,写出FeCl3与金属铜反应的离子方程式
(3)向沸水中逐滴滴加1 mol·L-1FeCl3溶液至液体呈透明的红褐色,该分散系中微粒直径的范围是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某小组同学分别探究FeCl2溶液、FeCl3溶液的性质。
I.探究FeCl2溶液的性质。
(1)从物质类别角度判断FeCl2属于___________ ,因此可以与某些碱反应。
(2)预测FeCl2具有氧化性,因此可以与Zn反应,此时Zn体现___________ 性。
(3)预测FeCl2具有还原性,预测依据是___________ ,因此可以与酸性KMnO4溶液反应。
(4)进行如下实验操作:
①i中的现象是___________ ,用化学方程式表示产生该现象的原因:___________ 、___________ 。
②ii中反应的离子方程式是___________ 。
③iii中的现象是___________ 。
(5)某同学认为iii中现象并不能证明Fe2+具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象、②___________ , 为证实该反应中Fe2+确实被氧化,需要在反应后的溶液中加入试剂___________ ,观察到现象___________ 。
II.探究FeCl3溶液的性质。
小组同学进行如下实验操作并观察到对应现象:
(6)iv中反应的离子方程式是___________ 。
(7)vi 中滴加氯水过程中,氯水反应的离子方程式是___________ 。
III.小组同学探究vi中褪色原因,提出两种假设: a.铁离子被转化,b. SCN被转化。
(8)分别向褪色后的溶液中滴加0.1 mol/L FeCl3溶液和KSCN溶液各1滴,观察到___________ 现象,得出结论:假设b成立。
(9)进一步预测SCN-可能被转化为SO ,通过实验验证了该预测,写出实验操作及现象
,通过实验验证了该预测,写出实验操作及现象___________ 。
I.探究FeCl2溶液的性质。
(1)从物质类别角度判断FeCl2属于
(2)预测FeCl2具有氧化性,因此可以与Zn反应,此时Zn体现
(3)预测FeCl2具有还原性,预测依据是
(4)进行如下实验操作:
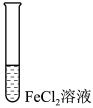 | 序号 | 操作 |
| i | 滴加NaOH溶液 | |
| ii | 加入少量锌粉 | |
| iii | 滴加酸性KMnO4溶液 |
②ii中反应的离子方程式是
③iii中的现象是
(5)某同学认为iii中现象并不能证明Fe2+具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象、②
II.探究FeCl3溶液的性质。
小组同学进行如下实验操作并观察到对应现象:
| 操作 | 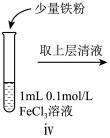 |  | 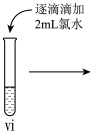 |
| 现象 | 溶液由棕黄色变为浅绿色 | 无明显现象 | 溶液变为红色, 而后红色褪去 |
(7)vi 中滴加氯水过程中,氯水反应的离子方程式是
III.小组同学探究vi中褪色原因,提出两种假设: a.铁离子被转化,b. SCN被转化。
(8)分别向褪色后的溶液中滴加0.1 mol/L FeCl3溶液和KSCN溶液各1滴,观察到
(9)进一步预测SCN-可能被转化为SO
 ,通过实验验证了该预测,写出实验操作及现象
,通过实验验证了该预测,写出实验操作及现象
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁元素及其化合物在生活生产中有广泛的用途。回答下列问题:
(1)Fe3+与SCN-的反应常用来检验Fe3+的存在: Fe3+ + 3SCN- Fe(SCN)3
Fe(SCN)3
若溶液中含有Fe3+,则加入KSCN溶液后的现象为_________ 向加入KSCN后的混合溶液中再加入少量NaOH固体,观察到的现象是_____________ ,产生该现象的原因是________________ 。
(2)向FeSO4溶液中滴入NaOH溶液,会观察到先产生白色沉淀,后迅速变为灰绿色,久置后变为红褐色,用化学方程式说明产生该现象的原因__________________ 。
(3)FeCl3溶液常被用作蚀刻剂腐蚀印刷电路板: 2Fe3++ Cu==2Fe2+ + Cu2+在过量FeCl3溶液腐蚀印刷电路板后的溶液中,加入过量铁粉,依次发生______ 、________ 两个反应(写离子方程式),若最后溶液中有固体剩余,则溶液中不可能含有的离子是____ 。
(4)FeCl2溶液在空气中容易被氧化,0.1 mol· L-1的FeCl2溶液暴露在空气中,20min 后,Fe2+的浓度变为0.05 mol· L-1,则20 min内,以Fe2+ 表示的平均反应速率为_____________ 若要验证该溶液中Fe2+未被完全氧化,则可以需要加入_____ 若出现_________ 现象,则证明Fe2+未被完全氧化。
(5)下列有关铁及其化合物的说法正确的是________
A.铁是第四周期第VIIIB族元素
B.亚铁盐只有还原性,没有氧化性
C.铁粉和铜粉的混合物可用磁铁吸引的方法分离
D.工业上通常采用电解法来冶炼单质铁
E.Fe3O4是一种纯净物
F.铁粉和氧化铝的混合物是一种铝热剂
(1)Fe3+与SCN-的反应常用来检验Fe3+的存在: Fe3+ + 3SCN-
 Fe(SCN)3
Fe(SCN)3 若溶液中含有Fe3+,则加入KSCN溶液后的现象为
(2)向FeSO4溶液中滴入NaOH溶液,会观察到先产生白色沉淀,后迅速变为灰绿色,久置后变为红褐色,用化学方程式说明产生该现象的原因
(3)FeCl3溶液常被用作蚀刻剂腐蚀印刷电路板: 2Fe3++ Cu==2Fe2+ + Cu2+在过量FeCl3溶液腐蚀印刷电路板后的溶液中,加入过量铁粉,依次发生
(4)FeCl2溶液在空气中容易被氧化,0.1 mol· L-1的FeCl2溶液暴露在空气中,20min 后,Fe2+的浓度变为0.05 mol· L-1,则20 min内,以Fe2+ 表示的平均反应速率为
(5)下列有关铁及其化合物的说法正确的是
A.铁是第四周期第VIIIB族元素
B.亚铁盐只有还原性,没有氧化性
C.铁粉和铜粉的混合物可用磁铁吸引的方法分离
D.工业上通常采用电解法来冶炼单质铁
E.Fe3O4是一种纯净物
F.铁粉和氧化铝的混合物是一种铝热剂
您最近半年使用:0次



