写出以下反应的化学方程式:
(1)Na与水反应:_______
(2)将CO2通入Na2CO3溶液中:_______
(3)将铜粉溶解在浓FeCl3溶液中:_______
(4)向FeCl3溶液中滴加氨水:_______
(1)Na与水反应:
(2)将CO2通入Na2CO3溶液中:
(3)将铜粉溶解在浓FeCl3溶液中:
(4)向FeCl3溶液中滴加氨水:
更新时间:2020-03-15 11:18:08
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】用化学用语表示:
(1)根据下列几种粒子的结构示意图,回答问题:
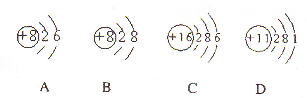
①写出B微粒的符号_________ ;
②若A微粒的中子数为10,写出A微粒的符号________ ;
③写出C、D两种元素形成的化合物在水溶液中的电离方程式:__________________________ ;
(2)写出下列反应的化学方程式:
①小块钠投入到水中__________________________________ ;
②工业上制备漂白粉____________________________________ 。
(1)根据下列几种粒子的结构示意图,回答问题:
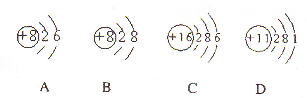
①写出B微粒的符号
②若A微粒的中子数为10,写出A微粒的符号
③写出C、D两种元素形成的化合物在水溶液中的电离方程式:
(2)写出下列反应的化学方程式:
①小块钠投入到水中
②工业上制备漂白粉
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】A、B、C、D是钠及其重要化合物,有着非常广泛的用途,已知B是常见的供氧剂。其相互转化关系如图所示(部分条件省略),回答下列问题:

(1)已知B为淡黄色粉末,则B为_______
(2)写出B→C的化学方程式:_______
(3)写出D→C的化学方程式:_______
(4)若A为金属钠,46 g A完全转化成D(涉及的其它反应物均足量),生成D的质量为_______ g。

(1)已知B为淡黄色粉末,则B为
(2)写出B→C的化学方程式:
(3)写出D→C的化学方程式:
(4)若A为金属钠,46 g A完全转化成D(涉及的其它反应物均足量),生成D的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】写出下列个反应的方程式。
(1)钠和水的反应____________________________________ (写出离子方程式)。
(2)过氧化钠和二氧化碳的反应_____________________ (写出化学方程式)。
(3)铜与稀硝酸反应___________________________________ (写出化学方程式)。
(4)向FeBr2通入等物质的量的Cl2______________________ (写出离子方程式)。
(5)Cl2通入NaOH溶液中___________________ (写出化学方程式)。
(1)钠和水的反应
(2)过氧化钠和二氧化碳的反应
(3)铜与稀硝酸反应
(4)向FeBr2通入等物质的量的Cl2
(5)Cl2通入NaOH溶液中
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图象。下图是钠的价类二维图:
(1)写出二维图中缺失①中某种淡黄色固体能做供氧剂的原因___________ (用化学方程式表示,写一个即可)
(2)写出 的电离方程式
的电离方程式___________ ; 溶液常因温度过高而分解含有少量
溶液常因温度过高而分解含有少量 ,除去杂质
,除去杂质 的方法为
的方法为___________ (用离子方程式表示)。
(3)向300 mL 某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2(忽略溶液体积的变化),充分反应后,得到Na2CO3和NaHCO3的混合溶液。向上述所得溶液中,逐滴滴加1 mol·L-1的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:___________ 。
②B点时,反应所得溶液中溶质的物质的量浓度是___________ 。

(1)写出二维图中缺失①中某种淡黄色固体能做供氧剂的原因
(2)写出
 的电离方程式
的电离方程式 溶液常因温度过高而分解含有少量
溶液常因温度过高而分解含有少量 ,除去杂质
,除去杂质 的方法为
的方法为(3)向300 mL 某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2(忽略溶液体积的变化),充分反应后,得到Na2CO3和NaHCO3的混合溶液。向上述所得溶液中,逐滴滴加1 mol·L-1的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:

②B点时,反应所得溶液中溶质的物质的量浓度是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】钠及其重要化合物之间的转化关系如下图所示,部分物质及反应条件略去。
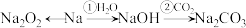

回答下列问题:
(1)少量的金属钠应保存在_______ 中。
(2) 为
为_______ 色固体。
(3)反应①的还原剂是_______ 。
(4)反应②的溶液中,NaOH实际参加反应的离子是_______ (填“ ”或“
”或“ ”)。
”)。
(5)反应③的化学方程式为_______ 。
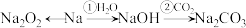

回答下列问题:
(1)少量的金属钠应保存在
(2)
 为
为(3)反应①的还原剂是
(4)反应②的溶液中,NaOH实际参加反应的离子是
 ”或“
”或“ ”)。
”)。(5)反应③的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】某小组同学探究碳酸钠和碳酸氢钠的性质,请你与他们一起完成,并回答问题。
(1)预测:从物质的类别来看,碳酸钠属于___ 类,可以与___ 等类别(至少写出两类)的物质发生反应。
(2)设计实验并得出结论:
(3)除去Na2CO3粉末中混有的少量NaHCO3固体的方法是__ ,所涉及的化学反应方程式为___ 。
(4)除去NaHCO3溶液中的Na2CO3,方法是__ ,反应方程式为___ 。
(1)预测:从物质的类别来看,碳酸钠属于
(2)设计实验并得出结论:
| 实验步骤 | 实验现象 | 结论或解释(用离子方程式表示) |
| ①分别向盛有Na2CO3溶液和NaHCO3的试管中滴加少量澄清石灰水 | 均产生浑浊 | 碳酸钠溶液:Ca2++CO =CaCO3↓ =CaCO3↓碳酸氢钠溶液: |
| ②向盛有Na2CO3溶液的试管中滴加稀盐酸 | 开始无气泡产生一段时间后产生气泡 | ①CO +H+=HCO +H+=HCO ② |
(3)除去Na2CO3粉末中混有的少量NaHCO3固体的方法是
(4)除去NaHCO3溶液中的Na2CO3,方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】氯化铁可用于金属蚀刻,如日常生活中不锈钢广告牌上的图形和文字就可用氯化铁溶液来蚀刻。
(1)写出氯化铁溶液蚀刻铁制品时发生反应的离子方程式。_________
(2)用化学方程式解释氯化铁蚀刻铜箔电路板的反应原理。_________
(1)写出氯化铁溶液蚀刻铁制品时发生反应的离子方程式。
(2)用化学方程式解释氯化铁蚀刻铜箔电路板的反应原理。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】把一小块金属钠投入水中,观察到以下各种现象:钠浮在水面上,熔成闪亮的小球,四处游动,逐渐减少,直至消失。
(1)写出该反应的离子方程式:_______ ,其中钠熔成闪亮小球的原因是_______ 。
(2)将所得溶液平均分成两份:
①一份加入足量的铝片充分反应,写出该反应的离子方程式:_______ 。
②向另一份溶液中滴加FeCl3溶液至沉淀不再增加,写出生成沉淀的离子方程式:_______ ;然后将沉淀过滤、洗涤、干燥、灼烧,最后得到Fe2O3固体1.6 g,通过计算,可知最初加入金属钠的质量为_______ g(保留小数点后两位小数)。
(1)写出该反应的离子方程式:
(2)将所得溶液平均分成两份:
①一份加入足量的铝片充分反应,写出该反应的离子方程式:
②向另一份溶液中滴加FeCl3溶液至沉淀不再增加,写出生成沉淀的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】钠、铝、铁是三种重要的金属。请回答:
(1)钠元素的金属性比铝的_______ (填“强”或“弱”)。
(2)将一小块金属钠投入水中,发生反应的离子方程式为_______ ;
(3)取一定量的FeCl3,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成_______ 色。
b.向另一支试管中滴加NaOH溶液,反应的离子方程式是_______ 。
(4)野外焊接钢轨常采用铝热反应,发生的反应为 。
。
a.该反应所属基本反应类型是_______ 。
b.该反应中,发生氧化反应的是_______ (填化学式包括以下各空),发生还原反应的_______ ,氧化产物是_______ ,还原产物是_______ 。
(1)钠元素的金属性比铝的
(2)将一小块金属钠投入水中,发生反应的离子方程式为
(3)取一定量的FeCl3,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,反应的离子方程式是
(4)野外焊接钢轨常采用铝热反应,发生的反应为
 。
。a.该反应所属基本反应类型是
b.该反应中,发生氧化反应的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】铁是一种重要的金属材料,它的单质及化合物在生产生活中应用广泛。
(1)铁元素有三种常见的氧化物,分别是 FeO、Fe2O3、Fe3O4.其中具有磁性的是_______ ,可作为红色颜料的是_______ 。
(2)某补铁口服液中含有 Fe2+,为检验其是否被氧化变质,可取少量该口服液,向其中 滴加 KSCN 溶液,若溶液变为_______ 色,则说明其已变质。向该口服液中加入维生素 C 可防止其被氧化变质,此过程中利用了维生素 C 的_______ 性。
(3)FeCl3可作为铜电路板的腐蚀液,其反应原理为Cu与FeCl3溶液反应生成FeCl2和CuCl2,该反应的化学方程式为_______ 。向反应后的溶液中加入_______ ,可回收 Cu,并得到FeCl2溶液。
(1)铁元素有三种常见的氧化物,分别是 FeO、Fe2O3、Fe3O4.其中具有磁性的是
(2)某补铁口服液中含有 Fe2+,为检验其是否被氧化变质,可取少量该口服液,向其中 滴加 KSCN 溶液,若溶液变为
(3)FeCl3可作为铜电路板的腐蚀液,其反应原理为Cu与FeCl3溶液反应生成FeCl2和CuCl2,该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题
(1)在一定量的稀 中慢慢加入铁粉,得到的
中慢慢加入铁粉,得到的 的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。
的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。
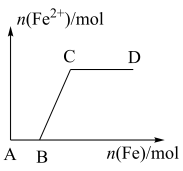
请将正确答案的序号填在相应的横线上。
①Fe3+②Fe2+③Fe、Fe2+ ④Fe2+、Fe3+
i.AB段铁元素以_________ 形式存在。
ii.BC段铁元素以_________ 形式存在
iii.CD段铁元素以__________ 形式存在。
(2)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:__________________ 。
(1)在一定量的稀
 中慢慢加入铁粉,得到的
中慢慢加入铁粉,得到的 的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。
的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。
请将正确答案的序号填在相应的横线上。
①Fe3+②Fe2+③Fe、Fe2+ ④Fe2+、Fe3+
i.AB段铁元素以
ii.BC段铁元素以
iii.CD段铁元素以
(2)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
您最近一年使用:0次



