氰气[(CN)2]性质与卤素相似,分子中4个原子处于同一直线.下列叙述正确的是( )
| A.是极性分子 |
| B.键长:N≡C大于C≡C |
C.CN﹣的电子式: 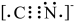 |
| D.和烯烃一样能发生加成反应 |
更新时间:2020-03-21 20:38:02
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
| A.HCl、HBr、HI的熔沸点依次增大,热稳定性也依次增强 |
| B.CO2和N2中,各原子的最外层都具有8电子稳定结构 |
| C.Na2O和Na2O2的阴、阳离子的个数比相同,化学键类型也相同 |
| D.MgF2既含有离子键又含有非极性共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】硒(Se)可用作光敏材料、电解锰行业催化剂等,是周期表中第34号元素。已知:Na2Se2+2H+=2Na++Se+H2Se。下列说法错误的是
A.中子数为40的硒原子: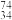 Se Se | B.H2Se的结构式:H—Se—H |
| C.Na2Se2中阴阳离子个数比为1∶1 | D.Na+的结构示意图: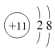 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
A.甲醛(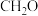 )分子中 )分子中 键和 键和 键的个数比为2∶1 键的个数比为2∶1 |
B. 易溶于苯、 易溶于苯、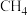 难溶于水,都可用“相似相溶”原理解释 难溶于水,都可用“相似相溶”原理解释 |
| C.键长越长,往往键能越大,共价键越稳定 |
| D.只含非极性键的分子一定是非极性分子,只含极性键的分子一定是极性分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中正确的是( )
| A.在分子中,两个成键的原子间的距离叫键长 | B.H-Cl键比H-I键稳定 |
| C.含有极性键的一定是极性分子 | D.键能越大,说明该分子越易受热分解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列说法正确的有几项
①键长:碳碳三键>碳碳双键>碳碳单键 ②酸性:CF3COOH>CCl3COOH>CH3COOH
③沸点:正戊烷>异戊烷>新戊烷 ④熔点:SiO2>NaCl>C60
⑤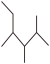 的名称为3,4-二甲基-2-乙基戊烷 ⑥键角:CH4>NH3>PH3
的名称为3,4-二甲基-2-乙基戊烷 ⑥键角:CH4>NH3>PH3
⑦HF比HCl沸点高的原因是HF分子内存在氢键
⑧甲苯与液溴在光照条件下可生成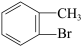 ⑨正己烷和2,2-二甲基丁烷互为同系物
⑨正己烷和2,2-二甲基丁烷互为同系物
⑩单烯烃和氢气加成后得到饱和烃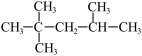 ,则该单烯烃可能有2种结构
,则该单烯烃可能有2种结构
⑪主族元素的电负性越大,其元素原子的第一电离能一定越大
⑫在任何情况下,都是σ键比π键强度大
①键长:碳碳三键>碳碳双键>碳碳单键 ②酸性:CF3COOH>CCl3COOH>CH3COOH
③沸点:正戊烷>异戊烷>新戊烷 ④熔点:SiO2>NaCl>C60
⑤
 的名称为3,4-二甲基-2-乙基戊烷 ⑥键角:CH4>NH3>PH3
的名称为3,4-二甲基-2-乙基戊烷 ⑥键角:CH4>NH3>PH3⑦HF比HCl沸点高的原因是HF分子内存在氢键
⑧甲苯与液溴在光照条件下可生成
 ⑨正己烷和2,2-二甲基丁烷互为同系物
⑨正己烷和2,2-二甲基丁烷互为同系物⑩单烯烃和氢气加成后得到饱和烃
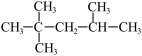 ,则该单烯烃可能有2种结构
,则该单烯烃可能有2种结构⑪主族元素的电负性越大,其元素原子的第一电离能一定越大
⑫在任何情况下,都是σ键比π键强度大
| A.5项 | B.6项 | C.4项 | D.8项 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】意大利化学家阿伏加德罗的重大贡献是建立分子学说,下列说法正确的是
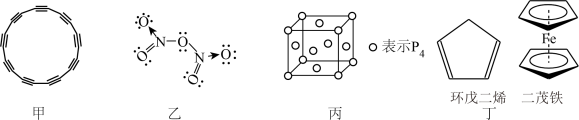

| A.18个碳原子构成的碳环分子的结构如图甲所示,该分子属于有机物 |
B. 的结构如图乙,可看作 的结构如图乙,可看作 分子中H原子被硝基取代而形成, 分子中H原子被硝基取代而形成, 是非极性分子 是非极性分子 |
C.白磷( )晶胞如图丙所示,白磷晶体中1个 )晶胞如图丙所示,白磷晶体中1个 分子周围有8个紧邻的 分子周围有8个紧邻的 分子 分子 |
| D.图丁中,环戊二烯中的原子有两种杂化方式,双环戊二烯合铁又称二茂铁为极性分子,无离子键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列物质的有关说法正确的是
| A.HCl极易溶于水,是因为它是极性分子 |
| B.H2O比H2S稳定,是因为水分之间有氢键 |
| C.SiO2和CO2都是共价化合物,所以晶体类型相同 |
| D.Na+的半径大于Mg2+,所以熔点Na2O>MgO |
您最近一年使用:0次

 发生反应:
发生反应: 。下列说法正确的是
。下列说法正确的是 的电子式为
的电子式为
 的结构式为
的结构式为

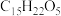 ,结构如图所示,该分子中包含7个手性碳原子
,结构如图所示,该分子中包含7个手性碳原子

