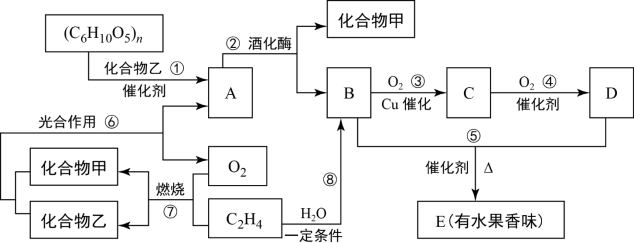
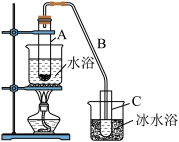
某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯。
已知: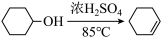 +H2O
+H2O
(1)制备粗品
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是_______ ,导管B除了导气外还具有的作用是_______________________ 。
②试管C置于冰水浴中的目的是_______________________ 。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_____ 层(填“上”或“下”),分液后用__________ (填编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按下图装置蒸馏,冷却水从_____ 口进入(填“f”或“g”)。蒸馏时要加入生石灰,目的是____________________________________ 。
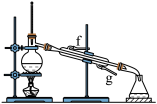
③收集产品时,控制的温度应在_______ 左右,实验制得的环己烯精品质量低于理论产量,可能的原因是____________ (填字母序号,下同)。
a.蒸馏时从70 ℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是____________ 。
a.用酸性高锰酸钾溶液
b.用金属钠
c.测定沸点

已知:
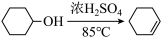 +H2O
+H2O密度(g·cm-3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是
②试管C置于冰水浴中的目的是
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按下图装置蒸馏,冷却水从

③收集产品时,控制的温度应在
a.蒸馏时从70 ℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是
a.用酸性高锰酸钾溶液
b.用金属钠
c.测定沸点
更新时间:2020-03-20 11:41:05
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
【推荐1】3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:
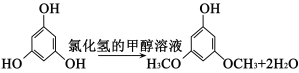
甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。
①分离出甲醇的操作是_______ 。
②萃取用到的分液漏斗使用前需_______ 并洗净。分液时,有机层在分液漏斗的_______ (填“上”或“下”)层。
(2)分离得到的有机层,依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是_______ ,用饱和食盐水洗涤的目的是_______ 。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是_______ (填序号)
①加入无水CaCl2干燥 ②重结晶 ③过滤除去干燥剂 ④蒸馏除去乙醚
(4)写出间苯三酚和过量浓溴水反应的化学方程式_______

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
| 物质 | 沸点 | 熔点 | 密度(20℃)/g·cm3 | 溶解性 |
| 甲醇 | 64.7 | - | 0.7915 | 易溶于水 |
| 乙醚 | 34.5 | - | 0.7138 | 微溶于水 |
| 3,5-二甲氧基苯酚 | - | 33~36 | - | 易溶于甲醇、乙醚,微溶于水 |
①分离出甲醇的操作是
②萃取用到的分液漏斗使用前需
(2)分离得到的有机层,依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是
①加入无水CaCl2干燥 ②重结晶 ③过滤除去干燥剂 ④蒸馏除去乙醚
(4)写出间苯三酚和过量浓溴水反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室以苯甲醛为原料制备间溴苯甲醛的反应如下:
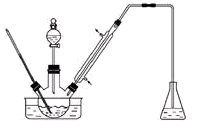

已知:(1)间溴苯甲醛温度过高时易被氧化。
(2)溴、苯甲醛、1,2-二氯乙烷、间溴苯甲醛的沸点见下表:
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后装入三颈烧瓶(如图所示),缓慢滴加经浓硫酸干燥过的足量液溴,控温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机层用10% NaHCO3溶液洗涤。
步骤3:经洗涤的有机层加入适量无水MgSO4固体,放置一段时间后过滤出MgSO4•nH2O晶体。
步骤4:减压蒸馏有机层,收集相应馏分。
(1) 实验装置中冷凝管的主要作用是_____ ,锥形瓶中应为_______ (填化学式)溶液。
(2) 步骤1反应过程中,为提高原料利用率,适宜的温度范围为(填序号)______ 。
A.>229℃ B.58.8℃~179℃ C.<58.8℃
(3) 步骤2中用10% NaHCO3溶液洗涤,是为了除去溶于有机层的______ (填化学式)。
(4) 步骤3中加入无水MgSO4固体的作用是___________________________________ 。
(5) 步骤4中采用减压蒸馏,是为了防止____________________________________ 。


已知:(1)间溴苯甲醛温度过高时易被氧化。
(2)溴、苯甲醛、1,2-二氯乙烷、间溴苯甲醛的沸点见下表:
| 物质 | 溴 | 苯甲醛 | 1,2-二氯乙烷 | 间溴苯甲醛 |
| 沸点/℃ | 58.8 | 179 | 83.5 | 229 |
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后装入三颈烧瓶(如图所示),缓慢滴加经浓硫酸干燥过的足量液溴,控温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机层用10% NaHCO3溶液洗涤。
步骤3:经洗涤的有机层加入适量无水MgSO4固体,放置一段时间后过滤出MgSO4•nH2O晶体。
步骤4:减压蒸馏有机层,收集相应馏分。
(1) 实验装置中冷凝管的主要作用是
(2) 步骤1反应过程中,为提高原料利用率,适宜的温度范围为(填序号)
A.>229℃ B.58.8℃~179℃ C.<58.8℃
(3) 步骤2中用10% NaHCO3溶液洗涤,是为了除去溶于有机层的
(4) 步骤3中加入无水MgSO4固体的作用是
(5) 步骤4中采用减压蒸馏,是为了防止
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
【推荐3】[实验化学]
3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。①分离出甲醇的操作是的_________ 。
②萃取用到的分液漏斗使用前需_______ 并洗净,分液时有机层在分液漏斗的_____ 填(“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是______________ ;用饱和食盐水洗涤的目的是______________ 。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是_____ (填字母)。
a.蒸馏除去乙醚 b..重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤。为了防止倒吸,减压过滤完成后应先_______ ,再______ 。
3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
| 甲醇 | 64. 7 |  | 0. 7915 | 易溶于水 |
| 乙醚 | 34. 5 |  | 0. 7138 | 微溶于水 |
| 3,5-二甲氧基苯酚 |  | 33 ~36 |  | 易溶于甲醇、乙醚,微溶于水 |
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。①分离出甲醇的操作是的
②萃取用到的分液漏斗使用前需
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是
a.蒸馏除去乙醚 b..重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤。为了防止倒吸,减压过滤完成后应先
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】在实验室用乙醇制取乙烯时,常会看到烧瓶中的液体变黑,并在制得的乙烯中混有 、
、 等杂质。某课外小组的同学设计了图所示的装置,用来制取乙烯并验证乙烯的性质。
等杂质。某课外小组的同学设计了图所示的装置,用来制取乙烯并验证乙烯的性质。
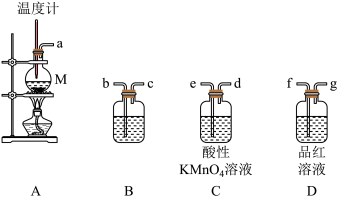
回答下列问题:
(1)实验室制取乙烯的反应原理:___________ 。
(2)装置A中一处明显的错误是___________ ,玻璃仪器M的名称为___________ ,其中加入碎瓷片的作用是___________ 。
(3)为证明实验过程中有 产生,并验证乙烯的性质,正确的装置连接顺序
产生,并验证乙烯的性质,正确的装置连接顺序
___________ ,装置B中应添加的试剂___________ ,装置C中的现象___________ 。
 、
、 等杂质。某课外小组的同学设计了图所示的装置,用来制取乙烯并验证乙烯的性质。
等杂质。某课外小组的同学设计了图所示的装置,用来制取乙烯并验证乙烯的性质。
回答下列问题:
(1)实验室制取乙烯的反应原理:
(2)装置A中一处明显的错误是
(3)为证明实验过程中有
 产生,并验证乙烯的性质,正确的装置连接顺序
产生,并验证乙烯的性质,正确的装置连接顺序
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】丙酮[ (CH3)2CO]是一种无色透明液体,沸点56.53℃,易溶于水和乙醇、乙醚等有机溶剂。实验室可采用重铬酸钾氧化异丙醇[(CH3)2CHOH](沸点82. 45°C)来制取,实验装置如图所示(加热装置和夹持装置略)。步骤如下:

①在某规格的圆底烧瓶中,将5 g重铬酸钾用5 mL水溶解后加入5 mL异丙醇,摇匀。
②取一小烧杯加6 mL水,缓慢加入2 mL浓硫酸,混匀后加入恒压滴液漏斗中,组装仪器并通入冷凝水。
③加热圆底烧瓶中的混合物至沸腾,用恒压滴液漏斗滴加稀硫酸,保持烧瓶中的液体微沸,控制温度收集55°C ~57°C馏分,即得到产品。
回答下列问题:
(1)选用圆底烧瓶时,所盛液体总体积一般应介于其容量的_______ 之间;本实验中,直形冷凝管_______ (填 “能”或“不能”)用蛇形冷凝管( )代替,理由是
)代替,理由是_______ 。
(2)在圆底烧瓶中,酸性K2Cr2O7溶液将(CH3)2CHOH氧化为(CH3)2CO时,还原产物为Cr3+反应的离子方程式为_______ ;若浓硫酸不经稀释,易发生副反应,可能的有机副产物有异丙醚[ (CH3)2CHOCH( CH3)2]和_______ ( 填结构简式),无机物则为_______ 和CO2。
(3)实验中采用边反应边分离出产物的方法,目的是_______ 。
(4)为了初步测定产品纯度,需要配制100 mL NaOH标准溶液,配制100 mL标准溶液时需要的玻璃仪器有_______ 、烧杯、量筒、玻璃棒、胶头滴管;测定原理可简化表示为:(CH3)2CO + NH2OH·HCl=(CH3)2C =NOH + HCl+H2O,以澳酚蓝为指示剂,用NaOH标准溶液滴定反应生成的盐酸。若测定时样品质量为0. 8120g,与NH2OH·HCl完全反应后,用0.5000 mol · L-1NaOH溶液滴定生成的盐酸,消耗25.20 mL标准溶液。则初步测得产品纯度(质量分数)为_______ 。

①在某规格的圆底烧瓶中,将5 g重铬酸钾用5 mL水溶解后加入5 mL异丙醇,摇匀。
②取一小烧杯加6 mL水,缓慢加入2 mL浓硫酸,混匀后加入恒压滴液漏斗中,组装仪器并通入冷凝水。
③加热圆底烧瓶中的混合物至沸腾,用恒压滴液漏斗滴加稀硫酸,保持烧瓶中的液体微沸,控制温度收集55°C ~57°C馏分,即得到产品。
回答下列问题:
(1)选用圆底烧瓶时,所盛液体总体积一般应介于其容量的
 )代替,理由是
)代替,理由是(2)在圆底烧瓶中,酸性K2Cr2O7溶液将(CH3)2CHOH氧化为(CH3)2CO时,还原产物为Cr3+反应的离子方程式为
(3)实验中采用边反应边分离出产物的方法,目的是
(4)为了初步测定产品纯度,需要配制100 mL NaOH标准溶液,配制100 mL标准溶液时需要的玻璃仪器有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】软锰矿(成分如表1所示)的成分是二氧化锰,其中还含有少量二氧化硅、铁、氧化铝以及少量的重金属等。废铁屑还原软锰矿生产高纯硫酸锰晶体的工艺流程如图1所示。
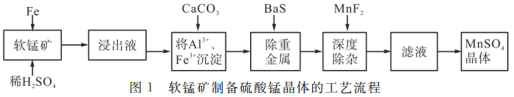
表1软锰矿的化学成分
(1)浸出液中检测到存在Fe3+,软锰矿与铁屑发生的离子反应是___________ ;
(2)加入碳酸钙之前需要加入双氧水的作用是___________ ,用碳酸钙除去铁、铝的原理是___________ 。(表2数据可供参考)。
表2不同金属离子沉淀的pH
(3)深度除杂中所加二氟化锰的作用是___________ 。
(4)从滤液中获得硫酸锰晶体的方法是___________ 。(硫酸锰在不同温度下的溶解度见表3)
表3硫酸锰在不同温度下的溶解度
(5)H2SO4/MnO2的物质的量比不同对锰的浸出率η有影响;实验表明,当H2SO4、MnO2的物质的量比2.1∶1锰的浸出率较高(见图2),请结合反应原理说明原因:___________ 。
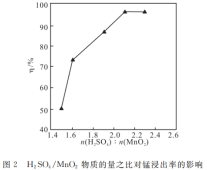

表1软锰矿的化学成分
| 成分 | 含量/% | 成分 | 含量/% |
| MnO2 | 35.23 | Fe | 2.16 |
| SiO2 | 15.67 | Al2O3 | 3.34 |
| MgO | 0.18 | CaO | 4.82 |
(2)加入碳酸钙之前需要加入双氧水的作用是
表2不同金属离子沉淀的pH
| 物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 1.5 | 6.5 | 3.3 | 7.7 |
| 沉淀完全 | 3.7 | 9.7 | 5.2 | 9.8 |
(4)从滤液中获得硫酸锰晶体的方法是
表3硫酸锰在不同温度下的溶解度
| 温度/℃ | 50 | 80 | 90 | 100 |
| 溶解度/(g/100g水) | 58 | 48 | 42 | 34 |

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
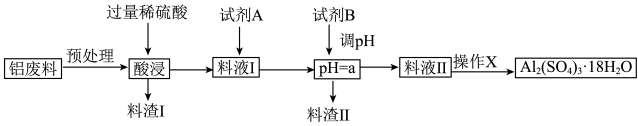
【推荐2】硫酸铝在造纸、水净化、土壤改良中有着广泛应用。某化工厂利用含铅废料(成分为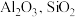 及少量
及少量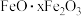 )制备硫酸铝晶体的工艺流程如下图所示,回答相关问题。
)制备硫酸铝晶体的工艺流程如下图所示,回答相关问题。
已知生成氢氧化物沉淀的 如下表:
如下表:
(1)“预处理”时需要将铝废料粉碎,目的是_______ 。
(2)料渣Ⅰ的成分是_______ ,酸浸时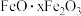 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(3)试剂 是一种液态绿色氧化剂,料液Ⅰ中反应的离子方程式
是一种液态绿色氧化剂,料液Ⅰ中反应的离子方程式_______ 。
(4) 的范围是
的范围是_______ ,试剂B最好是_______ ,目的是_______ 。(用离子方程式和必要的文字描述)
(5)操作 的内容是
的内容是_______ 、过滤、洗涤、干燥等。
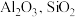 及少量
及少量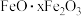 )制备硫酸铝晶体的工艺流程如下图所示,回答相关问题。
)制备硫酸铝晶体的工艺流程如下图所示,回答相关问题。
已知生成氢氧化物沉淀的
 如下表:
如下表: |  |  | |
开始沉淀时 | 3.6 | 6.3 | 2.3 |
完全沉淀时 | 4.9 | 8.3 | 3.2 |
(2)料渣Ⅰ的成分是
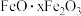 发生反应的离子方程式为
发生反应的离子方程式为(3)试剂
 是一种液态绿色氧化剂,料液Ⅰ中反应的离子方程式
是一种液态绿色氧化剂,料液Ⅰ中反应的离子方程式(4)
 的范围是
的范围是(5)操作
 的内容是
的内容是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
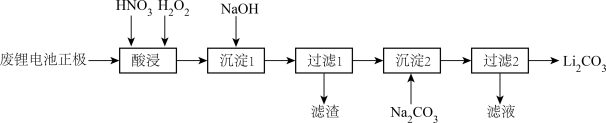
【推荐3】实验室回收利用废旧锂离子电池正极材料锰酸锂LiMn2O4)的一种流程如下:
(1)废旧电池可能残留有单质锂,拆解不当易爆炸、着火,为了安全,对拆解环境的要求是_______________________________________________________ 。
(2)“酸浸”时采用HNO3和H2O2的混合液体,可将难溶的LiMn2O4转化为 Mn ( NO3)2、LiNO3等产物。请写出该反应离子方程式:_________________________________ 。
如果采用盐酸溶解,从反应产物的角度分析,以盐酸代替HNO3和H2O2混合物的缺点是___________ 。
(3)“过滤2”时,洗涤Li2CO3沉淀的操作是_________________________________ 。
(4)把分析纯碳酸锂与二氧化锰两种粉末,按物质的量1:4混合均匀加热可重新生成 LiMn2O4,升温到515℃时,开始有CO2产生,同时生成固体A,比预计碳酸锂的分解温度(723℃)低很多,可能的原因是______________________ 。
(5)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀的pH=7.7。请补充由上述过程中,制得的Mn(OH)2制备高纯MnCO3的操作步骤[实验中可选用的试剂:H2SO4、Na2CO3、C2H5OH]:向Mn(OH)2中边搅拌边加入______________________ 。
(6)味精厂、化肥厂、垃圾渗滤液等排放的废水中往往含有高浓度的氨氮,若不经处理直接排放会对水体造成严重的污染。电化学氧化法:电化学去除氨氮主要是氯气和次氯酸的间接氧化作用。对某养猪场废水进行电化学氧化处理,选用IrO2-TiO2/Ti电极作为阳极,阴极采用网状钛板,加入一定量的NaCl,调节溶液的pH,在电流密度为85mA·cm-2下电解,180min内去除率达到98.22%。阳极发生的电极反应式是______________________ ;HClO氧化除去氨氮的反应离子方程式是_________________________________ 。

(1)废旧电池可能残留有单质锂,拆解不当易爆炸、着火,为了安全,对拆解环境的要求是
(2)“酸浸”时采用HNO3和H2O2的混合液体,可将难溶的LiMn2O4转化为 Mn ( NO3)2、LiNO3等产物。请写出该反应离子方程式:
如果采用盐酸溶解,从反应产物的角度分析,以盐酸代替HNO3和H2O2混合物的缺点是
(3)“过滤2”时,洗涤Li2CO3沉淀的操作是
(4)把分析纯碳酸锂与二氧化锰两种粉末,按物质的量1:4混合均匀加热可重新生成 LiMn2O4,升温到515℃时,开始有CO2产生,同时生成固体A,比预计碳酸锂的分解温度(723℃)低很多,可能的原因是
(5)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀的pH=7.7。请补充由上述过程中,制得的Mn(OH)2制备高纯MnCO3的操作步骤[实验中可选用的试剂:H2SO4、Na2CO3、C2H5OH]:向Mn(OH)2中边搅拌边加入
(6)味精厂、化肥厂、垃圾渗滤液等排放的废水中往往含有高浓度的氨氮,若不经处理直接排放会对水体造成严重的污染。电化学氧化法:电化学去除氨氮主要是氯气和次氯酸的间接氧化作用。对某养猪场废水进行电化学氧化处理,选用IrO2-TiO2/Ti电极作为阳极,阴极采用网状钛板,加入一定量的NaCl,调节溶液的pH,在电流密度为85mA·cm-2下电解,180min内去除率达到98.22%。阳极发生的电极反应式是
您最近一年使用:0次