下表为元素周期表的一部分。
完成下列填空
(1)氮原子的电子排布式为_________ ,Z元素在元素周期表中的位置为______
(2)上表中原子半径最大的元素是(写元素符号)_____________ ,该原子的核外电子占有_____________ 个轨道,有___________ 种运动状态。
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是______________
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1moY单质比1mol硫单质得电子多
c.Y和硫两元素单最低价氢化物受热分解,前者的分解温度高
(4)X与Z两元素的单质反应生成1molX的高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出:X的电子式为______________ 该反应的热化学方程式__________________
(5)简述碳的同位素中一种原子的用途___________
| 碳 | 氮 | Y | |
| X | 硫 | Z |
完成下列填空
(1)氮原子的电子排布式为
(2)上表中原子半径最大的元素是(写元素符号)
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1moY单质比1mol硫单质得电子多
c.Y和硫两元素单最低价氢化物受热分解,前者的分解温度高
(4)X与Z两元素的单质反应生成1molX的高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出:X的电子式为
(5)简述碳的同位素中一种原子的用途
更新时间:2020-03-25 09:57:23
|
相似题推荐
【推荐1】已知下列热化学方程式:
①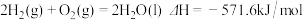
②
③
请回答:
(1)上述反应中属于放热反应的是_______ (填序号,下同),属于吸热反应的是_______ 。
(2)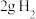 完全燃烧生成液态水,放出的热量为
完全燃烧生成液态水,放出的热量为_______ 。
(3)已知 稀溶液与
稀溶液与 稀溶液反应生成
稀溶液反应生成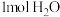 时,放出12.1kJ热量,用离子方程式表示该反应的热化学方程为
时,放出12.1kJ热量,用离子方程式表示该反应的热化学方程为_______ 。
(4)已知:
 ,
,
则断开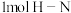 键与断开
键与断开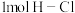 键所需能量相差约为
键所需能量相差约为_______ kJ。
①
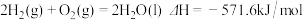
②

③

请回答:
(1)上述反应中属于放热反应的是
(2)
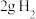 完全燃烧生成液态水,放出的热量为
完全燃烧生成液态水,放出的热量为(3)已知
 稀溶液与
稀溶液与 稀溶液反应生成
稀溶液反应生成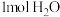 时,放出12.1kJ热量,用离子方程式表示该反应的热化学方程为
时,放出12.1kJ热量,用离子方程式表示该反应的热化学方程为(4)已知:

 ,
,
则断开
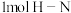 键与断开
键与断开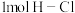 键所需能量相差约为
键所需能量相差约为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】依据事实,写出下列反应的热化学方程式。
(1)1 mol C2H4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出1411 kJ能量:_____________________________ 。
(2)1 mol C2H5OH(l)与适量O2(g)反应生成CO2(g)和H2O(l),放出1366.8 kJ热量:_______________________ 。
(3)2 mol Al(s)与适量O2(g)发生反应生成Al2O3(s),放出1669.8 kJ热量:________________________ 。
(4)在200°C、101 kPa时,1 mol H2与碘蒸气作用生成HI气体,放出14.9 kJ热量:___________________________ 。
(1)1 mol C2H4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出1411 kJ能量:
(2)1 mol C2H5OH(l)与适量O2(g)反应生成CO2(g)和H2O(l),放出1366.8 kJ热量:
(3)2 mol Al(s)与适量O2(g)发生反应生成Al2O3(s),放出1669.8 kJ热量:
(4)在200°C、101 kPa时,1 mol H2与碘蒸气作用生成HI气体,放出14.9 kJ热量:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,立即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态双氧水反应,生成水蒸气和氮气,放出256.652kJ的热量。
(1)反应的热化学方程式为__ 。
(2)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是:__ 。
(3)发射卫星可用肼为燃料,二氧化氮作氧化剂,两者反应生成氮气和水蒸气。已知:
①N2(g)+2O2(g)=2NO2(g)ΔH=+67.7kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g)ΔH=-534kJ·mol-1
肼和二氧化氮反应的热化学方程式为__ 。
(1)反应的热化学方程式为
(2)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是:
(3)发射卫星可用肼为燃料,二氧化氮作氧化剂,两者反应生成氮气和水蒸气。已知:
①N2(g)+2O2(g)=2NO2(g)ΔH=+67.7kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g)ΔH=-534kJ·mol-1
肼和二氧化氮反应的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】联合国大会将2019年定为“化学元素周期表国际年”,显示了元素周期表的重要性。表中列出了a~j10种元素在周期表中的位置:
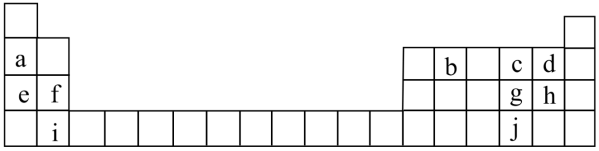
(1)元素a的原子结构示意图为_____ 。
(2)元素b可以形成多种单质,写出其中的两种_____ (填名称)。
(3)元素a~j中非金属性最强的是____ (填元素符号),元素h和i形成的化合物中化学键的类型是_____ 键。
(4)若e单质着火,可用于灭火的物质是____ (填字母)。
(5)3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法正确的有____ (填字母)。

(1)元素a的原子结构示意图为
(2)元素b可以形成多种单质,写出其中的两种
(3)元素a~j中非金属性最强的是
(4)若e单质着火,可用于灭火的物质是
| A.自来水 | B.CO2 | C.干沙子 | D.湿抹布 |
| A.a的金属性比e弱 | B.自然界中,e的储量比a高 |
| C.a的原子半径比e大 | D.基于a的电池质量轻、易携带 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】下表是元素周期表的一部分,请回答:
(1)元素⑦的原子结构示意图为_____ ;元素⑩的名称为______ ;
(2)在这些元素中,化学性质最活泼的金属元素是____ (填元素符号,下同),最不活泼的元素是___ ;原子半径最小的元素是_____ ;
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是___ (填化学式,下同);具有两性的是____ 。
| 族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(1)元素⑦的原子结构示意图为
(2)在这些元素中,化学性质最活泼的金属元素是
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】有7种短周期元素,其原子半径及主要化合价如下:
完成下列填空:
(1)A在元素周期表中的位置是_______ 。
(2)上述7种元素形成的简单离子中,离子半径最大是_______ (用离子符号表示)
(3)甲是由G、H两种元素组成的18e-分子,用电子式表示其形成过程_______ 。
(4)用一个化学方程式表示E元素的非金属性比D强_______ 。
| 元素代号 | A | B | D | E | F | G | H |
| 原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
| 主要化合价 | +1 | +3 | +6,-2 | +7,-1 | +5,-3 | -2 | +1 |
完成下列填空:
(1)A在元素周期表中的位置是
(2)上述7种元素形成的简单离子中,离子半径最大是
(3)甲是由G、H两种元素组成的18e-分子,用电子式表示其形成过程
(4)用一个化学方程式表示E元素的非金属性比D强
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】如图是硫元素价态与含硫元素物质类别的二维坐标图。

请回答下列问题
(1)硫元素在周期表中的位置为____ 。
(2)氧元素比硫元素的非金属性___ (填“强”或“弱”),不能说明该非金属性强弱的事实是___ 。
A.热稳定性H2O比H2S强
B.H2S水溶液在空气中变浑浊
C.H2O比H2S的沸点高
D.在一定条件下,O2与Cu反应生成CuO,S与Cu反应生成Cu2S
(3)写出b与j混合,发生反应的化学方程式为_______ 。
(4)已知硒(Se)与硫是相邻周期同主族元素,画出硒原子结构示意图_______ 。

请回答下列问题
(1)硫元素在周期表中的位置为
(2)氧元素比硫元素的非金属性
A.热稳定性H2O比H2S强
B.H2S水溶液在空气中变浑浊
C.H2O比H2S的沸点高
D.在一定条件下,O2与Cu反应生成CuO,S与Cu反应生成Cu2S
(3)写出b与j混合,发生反应的化学方程式为
(4)已知硒(Se)与硫是相邻周期同主族元素,画出硒原子结构示意图
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】2019年为元素周期表发现150周年,故将2019年定为“国际化学元素周期表年”,新版周期表包含118种元素,表中代表元素周期表前四周期。回答下列问题:
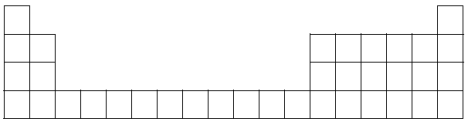
(1)将铁的元素符号填写在上述元素周期表相应的空格中____ 。
(2)短周期元素M、N的原子序数依次增大,原子M、N的最外层电子数均为最内层电子数的2倍。写出工业生产上用M制备N的化学方程式____ 。
(3)下列有关性质的比较正确且能用元素周期律解释的是___ (填标号)。
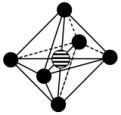
(4)SCl6分子的空间结构为正八面体形(如图所示)。1molSCl6中含有___ molS-Cl键。
(5)写出短周期主族元素中原子半径最大的元素与第二周期第VIA族元素形成的既有离子键又有共价键的物质的电子式____ ,该物质与水反应时,还原剂为____ 。

(1)将铁的元素符号填写在上述元素周期表相应的空格中
(2)短周期元素M、N的原子序数依次增大,原子M、N的最外层电子数均为最内层电子数的2倍。写出工业生产上用M制备N的化学方程式
(3)下列有关性质的比较正确且能用元素周期律解释的是
| A.酸性:HCl>HClO | B.非金属性:N>P |
| C.碱性:NaOH>Al(OH)3 | D.沸点:HF>HCl |

(5)写出短周期主族元素中原子半径最大的元素与第二周期第VIA族元素形成的既有离子键又有共价键的物质的电子式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】硫代硫酸盐是一类具有应用前景的浸金试剂。硫代硫酸根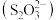 可看作是
可看作是 中的一个
中的一个 原子被
原子被 原子取代的产物。
原子取代的产物。
(1)基态 原子价层电子排布式是
原子价层电子排布式是___________ 。
(2)比较 原子和O原子的第一电离能大小,从原子结构的角度说明理由:
原子和O原子的第一电离能大小,从原子结构的角度说明理由:___________ 。
(3) 的空间结构是
的空间结构是___________ 。
(4)同位素示踪实验可证实 中两个
中两个 原子的化学环境不同,实验过程为
原子的化学环境不同,实验过程为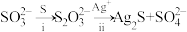 。过程ⅱ中,
。过程ⅱ中, 断裂的只有硫硫键,若过程ⅰ所用试剂是
断裂的只有硫硫键,若过程ⅰ所用试剂是 和
和 ,过程ⅱ含硫产物是
,过程ⅱ含硫产物是___________ 。
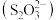 可看作是
可看作是 中的一个
中的一个 原子被
原子被 原子取代的产物。
原子取代的产物。(1)基态
 原子价层电子排布式是
原子价层电子排布式是(2)比较
 原子和O原子的第一电离能大小,从原子结构的角度说明理由:
原子和O原子的第一电离能大小,从原子结构的角度说明理由:(3)
 的空间结构是
的空间结构是(4)同位素示踪实验可证实
 中两个
中两个 原子的化学环境不同,实验过程为
原子的化学环境不同,实验过程为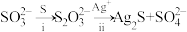 。过程ⅱ中,
。过程ⅱ中, 断裂的只有硫硫键,若过程ⅰ所用试剂是
断裂的只有硫硫键,若过程ⅰ所用试剂是 和
和 ,过程ⅱ含硫产物是
,过程ⅱ含硫产物是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】m、n、x、y四种主族元素在周期表里的相对位置如下图所示。已知它们的原子序数总和为46,则:
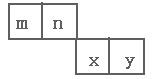
(1)写出n元素基态原子电子排布图:________________________ 。
(2)元素x气态氢化物的分子式为___________ ,空间构型为____________ 。
(3)m与y所形成的化合物含______________ 键,属_____________ 分子。(填“极性”或“非极性”)
(4)x位于周期表的第_____ 周期,第_____ 族;其原子结构示意图为____________ 。
(5)由n、y的氢化物相互作用所生成的物质的电子式为______________________ ,此物质属于_______________ 化合物。(填“离子”或“共价”)

(1)写出n元素基态原子电子排布图:
(2)元素x气态氢化物的分子式为
(3)m与y所形成的化合物含
(4)x位于周期表的第
(5)由n、y的氢化物相互作用所生成的物质的电子式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
(2)近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为FeSmAsFO组成的化合物。回答下列问题:
①Fe成为阳离子时首先失去___________ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___________ 。
②比较离子半径:F___________ O2-(填“大于”“等于”或“小于”)。
(3)在周期表中,与Li的化学性质最相似的邻族元素是___________ ,该元素基态原子核外M层电子的自旋状态___________ (填“相同”或“相反”)。
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
A.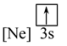 | B.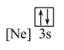 | C.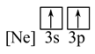 | D.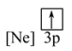 |
①Fe成为阳离子时首先失去
②比较离子半径:F
(3)在周期表中,与Li的化学性质最相似的邻族元素是
您最近一年使用:0次

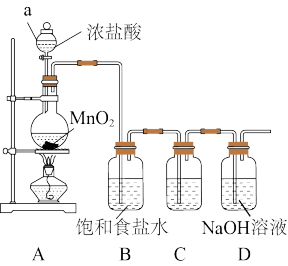
 仪器a的名称为
仪器a的名称为 装置C中盛放的试剂可以选用
装置C中盛放的试剂可以选用 填序号
填序号 ,当C中观察到
,当C中观察到 溶液
溶液 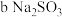 溶液
溶液 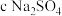 溶液
溶液 若反应后装置D中
若反应后装置D中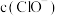 :
: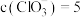 :1,则反应中被氧化的Cl原子与被还原的Cl原子个数比为
:1,则反应中被氧化的Cl原子与被还原的Cl原子个数比为

