下图中的A→K分别代表初中化学中的常见物质。已知:A、C两物质组成元素相同;G溶液为某物质的稀溶液,G的浓溶液能使小木棍变黑。图中部分生成物未标出。
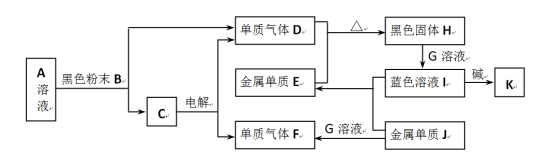
请回答下列问题:
(1)写出J可能的化学式:_______ (任写一种)。
(2)写出下列反应的化学方程式:
①A →C + D:_______ ;
②F + H → E + C:_______ ;
③I + 碱 → K:_______ (任写一种)。
(3)写出实验室制取F常用反应的化学方程式:_______ 。

请回答下列问题:
(1)写出J可能的化学式:
(2)写出下列反应的化学方程式:
①A →C + D:
②F + H → E + C:
③I + 碱 → K:
(3)写出实验室制取F常用反应的化学方程式:
19-20高一·浙江·阶段练习 查看更多[1]
(已下线)【新东方】高中化学X001
更新时间:2020-03-20 09:45:56
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】已知CO和H2的混合气体称为水煤气,可由碳与水蒸气在高温下反应生成。如下图:

已知:单质E可作为半导体材料,化合物F是有毒的氧化物,C为液态。据此,请填空:
(1)氧化物A是___________
(2)化合物F是___________
(3)反应②的化学方程式是_____________________________ ;
(4)反应③的化学方程式是______________________________ 。

已知:单质E可作为半导体材料,化合物F是有毒的氧化物,C为液态。据此,请填空:
(1)氧化物A是
(2)化合物F是
(3)反应②的化学方程式是
(4)反应③的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)碱洗铝材除其表面的氧化膜,碱洗时常有气泡冒出,原因是____ (用离子方程式表示)。为将碱洗后溶液中的铝以沉淀形式回收,最好应加入下列试剂中的________ (填字母)。
a.稀H2SO4b.盐酸 c.CO2d.氨水 e.NaOH
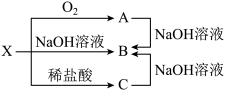
(2)已知X是某金属单质,X、A、B、C含同一种元素,可发生如下转化:
①写出下列物质的化学式:X:___ ,A:____ ,B:___ ,C:_____ 。
②写出以下反应的离子方程式:A→B:_______ ;C→B:__________ 。
a.稀H2SO4b.盐酸 c.CO2d.氨水 e.NaOH
(2)已知X是某金属单质,X、A、B、C含同一种元素,可发生如下转化:
①写出下列物质的化学式:X:
②写出以下反应的离子方程式:A→B:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】用如图所示装置进行铜与浓硫酸反应的实验。

请回答:
(1)铜与浓硫酸反应的化学方程式是______________________ 。
(2)实验中,观察到品红溶液_____________ ,石蕊溶液________________________ 。说明SO2_____________________ 。(填选项)
a.有氧化性 b.有还原性 c.有漂白性 d.水溶液显酸性
(3)为进一步确认产生的气体是二氧化硫,还应补充的操作是_________________ 。
(4)试管D中氢氧化钠溶液的作用是__________ ,用离子方程式说明___________ 。

请回答:
(1)铜与浓硫酸反应的化学方程式是
(2)实验中,观察到品红溶液
a.有氧化性 b.有还原性 c.有漂白性 d.水溶液显酸性
(3)为进一步确认产生的气体是二氧化硫,还应补充的操作是
(4)试管D中氢氧化钠溶液的作用是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】本题包括4小题,请按要求回答下列问题:
(1)小苏打(碳酸氢钠)可用于中和过多的胃酸,写出该反应的离子方程式________ 。
(2)向蔗糖中加入浓硫酸时,蔗糖变黑,体积膨胀,变成海绵状的炭。蔗糖变黑,说明浓硫酸具有_____ 性,后产生有刺激性气味的气体,说明浓硫酸具有_____ 性。
(3)NO2是_______ 色的有毒气体,它与水反应的化学方程式为________________ ,该反应中氧化剂与还原剂的质量比为________ 。
(4)用10 mol·L—1 H2SO4配制 480mL 1mol·L—1 H2SO4,有如下几个操作:
①计算并用量筒量取 x mL10 mol·L—1 H2SO4,稀释;
②将稀释后的溶液转入规格为 y 的容量瓶中;
③用少量蒸馏水洗涤烧杯和玻璃棒2–3次,并转入容量瓶;
④继续向容量瓶中加蒸馏水至刻度线;⑤将容量瓶塞紧,充分摇匀。
Ⅰ.请填写上述步骤中 x、y分别是:x_____________ ;y________________ 。
Ⅱ.若没有进行操作③,则所配溶液的浓度______ (填“偏高”、“偏低”或“不影响”,下同);操作④中定容时俯视刻度线,则所配溶液的浓度_________________ 。
(1)小苏打(碳酸氢钠)可用于中和过多的胃酸,写出该反应的离子方程式
(2)向蔗糖中加入浓硫酸时,蔗糖变黑,体积膨胀,变成海绵状的炭。蔗糖变黑,说明浓硫酸具有
(3)NO2是
(4)用10 mol·L—1 H2SO4配制 480mL 1mol·L—1 H2SO4,有如下几个操作:
①计算并用量筒量取 x mL10 mol·L—1 H2SO4,稀释;
②将稀释后的溶液转入规格为 y 的容量瓶中;
③用少量蒸馏水洗涤烧杯和玻璃棒2–3次,并转入容量瓶;
④继续向容量瓶中加蒸馏水至刻度线;⑤将容量瓶塞紧,充分摇匀。
Ⅰ.请填写上述步骤中 x、y分别是:x
Ⅱ.若没有进行操作③,则所配溶液的浓度
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】某兴趣小组设计以下装置进行铜与浓硫酸的反应,并检验生成产物。试管a中加入 浓硫酸,在烧杯中加入饱和的氢氧化钠溶液,将螺旋状的铜丝连接在2号注射器活塞的橡胶上,1号注射器配有较长的耐腐蚀的针头。
浓硫酸,在烧杯中加入饱和的氢氧化钠溶液,将螺旋状的铜丝连接在2号注射器活塞的橡胶上,1号注射器配有较长的耐腐蚀的针头。

请回答:
(1)试剂b为_______
(2)推动2号注射器活塞,将铜丝浸没在浓硫酸中,加热试管a,使反应开始进行,实验任务完成后,使反应停止的操作:_______
(3)利用1号注射器证明该实验中有 生成的具体操作和现象:
生成的具体操作和现象:_______
(4)实验结束后,如何检验烧杯中是否有硫酸根离子?_______
 浓硫酸,在烧杯中加入饱和的氢氧化钠溶液,将螺旋状的铜丝连接在2号注射器活塞的橡胶上,1号注射器配有较长的耐腐蚀的针头。
浓硫酸,在烧杯中加入饱和的氢氧化钠溶液,将螺旋状的铜丝连接在2号注射器活塞的橡胶上,1号注射器配有较长的耐腐蚀的针头。
请回答:
(1)试剂b为
(2)推动2号注射器活塞,将铜丝浸没在浓硫酸中,加热试管a,使反应开始进行,实验任务完成后,使反应停止的操作:
(3)利用1号注射器证明该实验中有
 生成的具体操作和现象:
生成的具体操作和现象:(4)实验结束后,如何检验烧杯中是否有硫酸根离子?
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】某工厂的固体废渣中主要含 和
和 ,还含有少量
,还含有少量 和
和 。利用该固体废渣制取
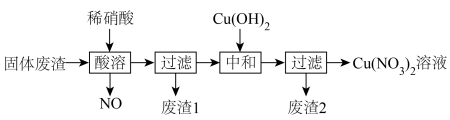
。利用该固体废渣制取 溶液的工艺流程如图所示:
溶液的工艺流程如图所示:
已知: 在酸性溶液中不稳定,会转变成
在酸性溶液中不稳定,会转变成 和
和 。
。___________ 写出 与稀硝酸反应的离子反应方程式
与稀硝酸反应的离子反应方程式___________ 。
(2)酸溶时,反应温度不宜超过 ,其主要原因是
,其主要原因是___________ 。
(3)废渣1主要成分为___________ 。
(4)酸溶时产生的NO在一定条件下可以用氨气转化为对环境无害的物质,该反应中氧化剂和还原剂的物质的量之比为___________ 。
 和
和 ,还含有少量
,还含有少量 和
和 。利用该固体废渣制取
。利用该固体废渣制取 溶液的工艺流程如图所示:
溶液的工艺流程如图所示:已知:
 在酸性溶液中不稳定,会转变成
在酸性溶液中不稳定,会转变成 和
和 。
。
 与稀硝酸反应的离子反应方程式
与稀硝酸反应的离子反应方程式(2)酸溶时,反应温度不宜超过
 ,其主要原因是
,其主要原因是(3)废渣1主要成分为
(4)酸溶时产生的NO在一定条件下可以用氨气转化为对环境无害的物质,该反应中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】为探究某不溶性固体X(仅含四种元素)的成分,设计并完成了如下实验:
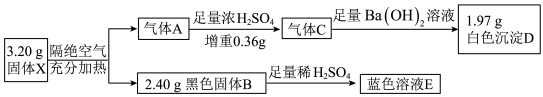
已知气体A是混合物,气体C是纯净物且无色无味。请回答:
(1)盐X中的4种元素是H、O和_______ (填元素符号),
(2)黑色固体B的化学式为_______ 。
(3)该流程中X隔绝空气加热分解的化学方程式为_______ 。
(4)向蓝色溶液E中加入KI溶液,有白色沉淀生成,溶液的颜色则由蓝色变为深黄色,经分析白色沉淀是CuI,写出该反应的离子方程式_______ 。

已知气体A是混合物,气体C是纯净物且无色无味。请回答:
(1)盐X中的4种元素是H、O和
(2)黑色固体B的化学式为
(3)该流程中X隔绝空气加热分解的化学方程式为
(4)向蓝色溶液E中加入KI溶液,有白色沉淀生成,溶液的颜色则由蓝色变为深黄色,经分析白色沉淀是CuI,写出该反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
(1)铜与浓硝酸反应的装置如图,A中反应的离子方程式为______ ,装置B的作用为______ 。
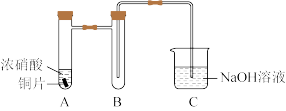
(2)铜与过量 反应的探究如下:
反应的探究如下:

实验②中Cu溶解的离子方程式为______ ;产生的气体为______ 。比较实验①和②,从氧化还原角度说明H⁺的作用是______ 。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰性氛围下加热,m g X完全分解为n g黑色氧化物Y,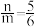 。X的化学式为
。X的化学式为______ 。
(4)取含X粗品0.0500 g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,用0.1000 mol⋅L
 标准溶液滴定,滴定终点时消耗
标准溶液滴定,滴定终点时消耗 标准溶液15.00 mL。(已知:
标准溶液15.00 mL。(已知: ,
, )粗品中X的百分含量
)粗品中X的百分含量______ %。
(1)铜与浓硝酸反应的装置如图,A中反应的离子方程式为

(2)铜与过量
 反应的探究如下:
反应的探究如下:
实验②中Cu溶解的离子方程式为
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰性氛围下加热,m g X完全分解为n g黑色氧化物Y,
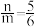 。X的化学式为
。X的化学式为(4)取含X粗品0.0500 g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,用0.1000 mol⋅L

 标准溶液滴定,滴定终点时消耗
标准溶液滴定,滴定终点时消耗 标准溶液15.00 mL。(已知:
标准溶液15.00 mL。(已知: ,
, )粗品中X的百分含量
)粗品中X的百分含量
您最近一年使用:0次




