常温下,甲、乙两杯醋酸稀溶液,甲的pH=a,乙的pH=a+1,下列关于溶液中量的关系判断正确的是
| A.H+浓度:10c (H+)甲 = c (H+)乙 |
| B.OH-浓度:c (OH-)甲 = 10 c (OH-)乙 |
| C.与等量NaOH反应耗酸体积:10V(甲)>V(乙) |
| D.溶液浓度: c(甲)>10c(乙) |
2012·上海徐汇·二模 查看更多[1]
(已下线)上海市徐汇区2012届高三4月学习能力诊断化学试题
更新时间:2020-03-30 19:51:19
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】pH=l的两种一元酸HZ和HY的溶液,分别取50 mL,加入足量的镁粉,充分反应后收集H2的体积分别为V(HZ)和V(HY),若V(HZ)>V(HY),下列说法正确的是
| A.HY一定是强酸 |
| B.HZ不一定为弱酸 |
| C.HZ的酸性强于HY的酸性 |
| D.反应开始时二者生成H2的速率相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,对于0.1mol/L的氨水,下列判断正确的是
| A.用相同浓度的硝酸中和该氨水,硝酸体积小于氨水时,溶液可能呈中性 |
| B.温度不变,加水稀释后溶液中c(NH4+)·c(OH-)不变 |
| C.加水稀释后,溶液中导电粒子的数目减少 |
| D.该溶液的pH=13 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,关于等体积、等pH的稀盐酸和稀醋酸两种溶液,下列说法正确的是
| A.两溶液中c(OH-):盐酸<醋酸 |
| B.c(Cl-)<c(CH3COO-) |
| C.中和同浓度NaOH溶液的能力:盐酸<醋酸 |
| D.分别用水稀释相同倍数后,两溶液pH仍相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】醋酸在水溶液中存在下列电离平衡:CH3COOH⇌CH3COO﹣+H+下列说法不正确的是
| A.加入醋酸钠,平衡向左移动 |
| B.加入碳酸钠,平衡向右移动 |
| C.加水稀释,c(H+)减小 |
| D.加水稀释,溶液中仅有的三种离子浓度都减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】醋酸的电离方程式为CH3COOH(aq)⇌H+(aq)+CH3COO-(aq) ΔH>0,25℃时,0.1mol/L醋酸溶液Ka=1.75×10-5(Ka表示酸的电离常数)。下列说法正确的是
| A.升高温度,c(H+)增大,Ka变大 |
| B.该溶液中加少量CH3COONa固体,平衡正向移动 |
| C.该温度下0.01mol/L醋酸溶液Ka<1.75×10-5 |
| D.向该溶液中滴加几滴浓盐酸,平衡逆向移动,c(H+)减小 |
您最近一年使用:0次

 溶液
溶液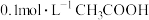 溶液
溶液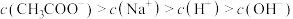
 不变
不变 固体,则
固体,则 减小
减小

