实验室用乙醇制取乙烯的装置如下图,回答下列问题。
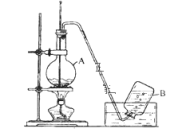
(1)仪器A的名称是________ ;A中加入沸石的目的是______ ;在烧杯中配制A中溶液的方法是____ ;在反应中浓硫酸的作用是_____ ;A中发生反应的化学方程式是____
(2)A中产生的气体除乙烯外,还可能混有少量__________ (填化学式)
(3)用乙烯制聚乙烯的化学方程式为__________

(1)仪器A的名称是
(2)A中产生的气体除乙烯外,还可能混有少量
(3)用乙烯制聚乙烯的化学方程式为
12-13高二上·云南德宏·期末 查看更多[4]
陕西省渭南市尚德中学2018-2019学年高二下学期期中考试化学试题陕西省吴起高级中学2018-2019学年高二下学期第二次月考基础卷化学试题河北省曲阳县一中2018-2019学年高二下学期3月月考化学试题(已下线)2011-2012学年云南省芒市中学高二上学期期末考试化学试卷
更新时间:2016-12-09 02:55:05
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯(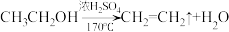 ),生成的气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应。乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量还原性的杂质气体,由此提出必须先除去杂质,再与溴水反应。请回答下列问题:
),生成的气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应。乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量还原性的杂质气体,由此提出必须先除去杂质,再与溴水反应。请回答下列问题:
(1)甲同学设计的实验___  填“能”或“不能”
填“能”或“不能” 验证乙烯与溴水发生了加成反应,其理由是
验证乙烯与溴水发生了加成反应,其理由是____  填字母
填字母 。
。
A.使溴水褪色的反应,未必是加成反应 B.使溴水褪色的反应,就是加成反应
C.使溴水褪色的物质,未必是乙烯 D.使溴水褪色的物质,就是乙烯
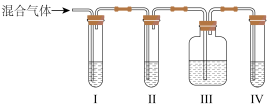
(2)乙同学推测此乙烯中必定含有一种杂质气体是_______ ,它与溴水反应的化学方程式是_______ ,在验证过程中必须全部除去。为此乙同学设计了如图所示的实验装置:_______ Ⅱ_______ Ⅲ_______ Ⅳ_______  选填序号
选填序号 。
。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液。
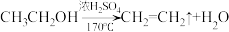 ),生成的气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应。乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量还原性的杂质气体,由此提出必须先除去杂质,再与溴水反应。请回答下列问题:
),生成的气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应。乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量还原性的杂质气体,由此提出必须先除去杂质,再与溴水反应。请回答下列问题:(1)甲同学设计的实验
 填“能”或“不能”
填“能”或“不能” 验证乙烯与溴水发生了加成反应,其理由是
验证乙烯与溴水发生了加成反应,其理由是 填字母
填字母 。
。A.使溴水褪色的反应,未必是加成反应 B.使溴水褪色的反应,就是加成反应
C.使溴水褪色的物质,未必是乙烯 D.使溴水褪色的物质,就是乙烯
(2)乙同学推测此乙烯中必定含有一种杂质气体是
 选填序号
选填序号 。
。A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液。
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】某有机物A的化学式为 ,其官能团的性质与一般链烃官能团性质相似,已知A具有下列性质:
,其官能团的性质与一般链烃官能团性质相似,已知A具有下列性质:
(1)能与HX作用;
(2) ;
;
(3)A不能使溴水褪色;
(4)A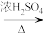 C
C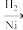
 ;
;
(5)
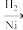 A。
A。
根据上述性质推断A、B、C的结构简式_______ 。
 ,其官能团的性质与一般链烃官能团性质相似,已知A具有下列性质:
,其官能团的性质与一般链烃官能团性质相似,已知A具有下列性质:(1)能与HX作用;
(2)
 ;
;(3)A不能使溴水褪色;
(4)A
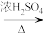 C
C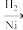
 ;
;(5)

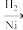 A。
A。根据上述性质推断A、B、C的结构简式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某校活动小组的同学拟用乙烯催化还原二氧化硫的方法来制取单质硫。
(1)甲组同学用乙醇脱水的反应来制取纯净的乙烯气体,其反应原理及制备装置如下:
主反应:C2H5OH CH2=CH2↑+H2O
CH2=CH2↑+H2O
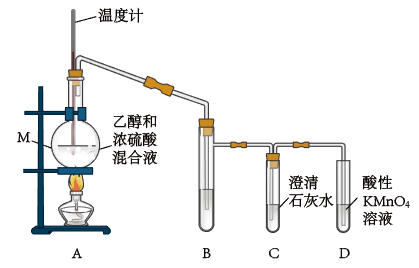
①仪器M的名称是_______ ;
②装置B中盛放的试剂可能是_______ ;
③装置C的作用是_______ 。
④证明产物中有乙烯气体的现象为_______ 。
(2)乙组同学用甲组同学制得的乙烯并结合如图装置进行乙烯催化还原二氧化硫的实验。

①装置E的作用是_______ ;装置G的作用是_______ 。
②玻璃管中有硫及二氧化碳生成,该反应的化学方程式为_______ 。
(1)甲组同学用乙醇脱水的反应来制取纯净的乙烯气体,其反应原理及制备装置如下:
主反应:C2H5OH
 CH2=CH2↑+H2O
CH2=CH2↑+H2O
①仪器M的名称是
②装置B中盛放的试剂可能是
③装置C的作用是
④证明产物中有乙烯气体的现象为
(2)乙组同学用甲组同学制得的乙烯并结合如图装置进行乙烯催化还原二氧化硫的实验。

①装置E的作用是
②玻璃管中有硫及二氧化碳生成,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】从分银渣(主要成分SnO2、Sb2O3、Ag、PbCl2)中提取金属的工艺流程如下:

已知:①“浆化熔炼”时,SnO2、Sb2O3转化为可溶性Na2SnS3和Na3SbS3、PbCl2转化为更难溶的PbS;②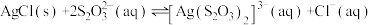 ;③滤液3中含大量[PbCl4]2-。
;③滤液3中含大量[PbCl4]2-。
回答下列问题:
(1)“溶浸”时为提高浸取速率,可以采取的方法有___________ (写出一种即可)。
(2)“沉锡”时调节pH过低,除导致沉淀不完全,还可能产生的问题有___________ ;证明“沉锡”后所得粗Sn(OH)4洗涤干净的具体操作为___________ 。
(3)“氧化分银”时,含Pb微粒转化的离子方程式为___________ ;向滤渣1中加入饱和NaCl的目的是___________ 。
(4)碱性环境下,加入足量甲醛得到粗Ag的离子方程式为___________ 。
(5)废液2经除杂、双氧水氧化处理后所得物质可循环入上述___________ 操作(填操作单元名称)。

已知:①“浆化熔炼”时,SnO2、Sb2O3转化为可溶性Na2SnS3和Na3SbS3、PbCl2转化为更难溶的PbS;②
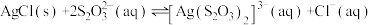 ;③滤液3中含大量[PbCl4]2-。
;③滤液3中含大量[PbCl4]2-。回答下列问题:
(1)“溶浸”时为提高浸取速率,可以采取的方法有
(2)“沉锡”时调节pH过低,除导致沉淀不完全,还可能产生的问题有
(3)“氧化分银”时,含Pb微粒转化的离子方程式为
(4)碱性环境下,加入足量甲醛得到粗Ag的离子方程式为
(5)废液2经除杂、双氧水氧化处理后所得物质可循环入上述
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】高铁酸钾(K2FeO4)为紫色固体,可用于饮用水的消毒和净化,微溶于KOH溶液,在酸性或中性溶液中产生O2,在碱性溶液中较稳定。实验室可用如下图所示装置制取K2FeO4溶液。

(1)高铁酸钾能用于消毒杀菌的原因是_______ 。
(2)浓盐酸和MnO2反应的离子方程式为_______ 。
(3)制取K2FeO4反应的化学方程式为_______ 。
(4)通过以下方法测定高铁酸钾样品的纯度:称取1.0000 g高铁酸钾样品,完全溶解于浓KOH溶液中,再加入足量亚铬酸钾KCr(OH)4反应后配成100.00 mL溶液;取上述溶液20.00 mL于锥形瓶中,加入稀硫酸调至pH=2,用0.1000 mol/L硫酸亚铁铵溶液滴定,消耗标准硫酸亚铁铵溶液24.00 mL。
测定过程中发生反应: 、
、
计算K2FeO4样品的纯度(写出计算过程)________

(1)高铁酸钾能用于消毒杀菌的原因是
(2)浓盐酸和MnO2反应的离子方程式为
(3)制取K2FeO4反应的化学方程式为
(4)通过以下方法测定高铁酸钾样品的纯度:称取1.0000 g高铁酸钾样品,完全溶解于浓KOH溶液中,再加入足量亚铬酸钾KCr(OH)4反应后配成100.00 mL溶液;取上述溶液20.00 mL于锥形瓶中,加入稀硫酸调至pH=2,用0.1000 mol/L硫酸亚铁铵溶液滴定,消耗标准硫酸亚铁铵溶液24.00 mL。
测定过程中发生反应:
 、
、
计算K2FeO4样品的纯度(写出计算过程)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。是目前国际上公认的新一代高效、广谱、安全的杀菌、保鲜剂,在水处理等方面有广泛应用的高效安全消毒剂。与Cl2相比,ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。某学生查得工业上可以在60℃时用潮湿的KClO3与草酸(H2C2O4)反应制取ClO2,用如图所示的装置模拟工业制取及收集ClO2,其中A为ClO2的发生装置,B为ClO2的凝集装置,C为尾气吸收装置。

请回答下列问题:
(1)装置A中产物有K2CO3、ClO2和CO2等,写出该反应的化学方程式:_______ ;装置A中还应安装的玻璃仪器是_______ 。
(2)如何检验虚框中A装置部分的气密性?_______ 。
(3)装置中还有一处明显不合理的是_______ (填“A”“B”或“C”),请指明改进方法:_______ 。
(4)ClO2需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10 mL,稀释成100 mL试样;量取V1 mL试样加入锥形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入淀粉指示剂,用c mol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。(已知2Na2S2O3+I2=Na2S4O6+2NaI)
①步骤2的目的是_______ (用离子方程式表示)。
②当_______ 时,可以判断此滴定操作达到终点。
③由以上数据可以计算原ClO2溶液的浓度为_______ g/L(用含字母的代数式表示)。

请回答下列问题:
(1)装置A中产物有K2CO3、ClO2和CO2等,写出该反应的化学方程式:
(2)如何检验虚框中A装置部分的气密性?
(3)装置中还有一处明显不合理的是
(4)ClO2需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10 mL,稀释成100 mL试样;量取V1 mL试样加入锥形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入淀粉指示剂,用c mol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。(已知2Na2S2O3+I2=Na2S4O6+2NaI)
①步骤2的目的是
②当
③由以上数据可以计算原ClO2溶液的浓度为
您最近一年使用:0次



