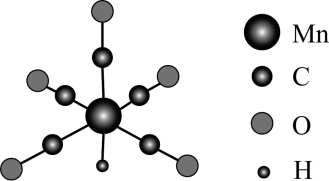
已知A原子的最外层电子数是次外层电子数的2倍,则基态A原子中,电子运动状态有 ____________ 种;电子占据的最高电子层符号为 ____________ ,该电子层含有的能级数为 ____________ ,该电子层含有 ____________ 个原子轨道。
更新时间:2020-04-09 07:44:45
|
相似题推荐
【推荐1】中国“奋斗者”号深潜器研制及海试的成功,在钛合金材料制备、锂离子电池等方面实现了重大突破。
(1)深潜器的壳体由含钛、铝等元素的Ti-62A钛合金材料制成,该合金材料的熔点比组成成分的金属___________ (选填“高”或“低”);铝元素的原子核外共有___________ 种不同能级的电子;以下方法可以比较钠和铝金属性强弱的方法___________ 。
a.比较两种金属单质的硬度和熔点
b.用钠置换氯化铝溶液中的铝
c.比较等物质的量的两种金属单质和足量盐酸反应失去的电子数
d.将空气中放置已久的这两种元素的单质分别和热水作用
e.在氯化铝溶液中逐滴滴加过量的氢氧化钠溶液
(2)氮氧化铝(AlON)是一种高硬度、耐高温的防弹材料,属于________ 晶体,Al、O、N三种元素的简单离子半径由大到小的排列顺序是___________ 。
(3)明矾[KAl(SO4)2·12H2O]溶液中离子浓度从大到小的顺序为_______ 。Mg(OH)2固体能除去镁盐溶液中的Al3+,原因是__________ ,(用离子方程式表达)
(4)在周期表中,锂的性质与镁相似,写出锂在氧气中燃烧产物的电子式________ 。
(5)已知:M(g)→M+(g)+Q(M代表碱金属元素)
从原子结构的角度解释上述金属Q值递变的原因:___________ 。
(1)深潜器的壳体由含钛、铝等元素的Ti-62A钛合金材料制成,该合金材料的熔点比组成成分的金属
a.比较两种金属单质的硬度和熔点
b.用钠置换氯化铝溶液中的铝
c.比较等物质的量的两种金属单质和足量盐酸反应失去的电子数
d.将空气中放置已久的这两种元素的单质分别和热水作用
e.在氯化铝溶液中逐滴滴加过量的氢氧化钠溶液
(2)氮氧化铝(AlON)是一种高硬度、耐高温的防弹材料,属于
(3)明矾[KAl(SO4)2·12H2O]溶液中离子浓度从大到小的顺序为
(4)在周期表中,锂的性质与镁相似,写出锂在氧气中燃烧产物的电子式
(5)已知:M(g)→M+(g)+Q(M代表碱金属元素)
| 元素 | Li | Na | K | Rb |
| Q(kJ) | -520 | -496 | -419 | -403 |
从原子结构的角度解释上述金属Q值递变的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为___________ ,Sm的价层电子排布式4f66s2,Sm3+的价层电子排布式为___________ 。
(2)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为___________ ,该能层具有的原子轨道数为___________ ,电子占据最高能级的电子云轮廓图为___________ 形。
②离子半径Li+___________ H-(填“>”“=”或“<”)。
(3)查表得知,元素X的电负性是1.5,元素Y的电负性是3.0,请判断X是___________ (填“金属”或“非金属”),该化合物中显负价的是___________ (填“X”或“Y”)。
(4) 的空间构型为
的空间构型为___________ ;O3是___________ 分子(填“极性”或“非极性”)。
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为
(2)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为
②离子半径Li+
(3)查表得知,元素X的电负性是1.5,元素Y的电负性是3.0,请判断X是
(4)
 的空间构型为
的空间构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。基态Fe2+与Fe3+离子中未成对的电子数之比为______ 。
(2)钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,基态Ti原子的核外电子排布式为____________ 。
(3)以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵((NH4)3Fe(C6H5O7)2)。Fe基态核外电子排布式为___________ ;
(4)钙和铜合金可用作电解制钙的阴极电极材料,基态铜原子的价电子排布式为________ 。
(5)基态Sn原子价层电子的空间运动状态有___ 种,基态氧原子的价层电子排布式不能表示为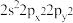 ,因为这违背了
,因为这违背了____ 原理(规则)。
(2)钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,基态Ti原子的核外电子排布式为
(3)以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵((NH4)3Fe(C6H5O7)2)。Fe基态核外电子排布式为
(4)钙和铜合金可用作电解制钙的阴极电极材料,基态铜原子的价电子排布式为
(5)基态Sn原子价层电子的空间运动状态有
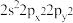 ,因为这违背了
,因为这违背了
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】我国硒储量居世界首位,硒广泛用于冶金、陶瓷、电子、太阳能等领域。工业上常将含硒废料处理得到亚硒酸( )和硒酸(
)和硒酸( ),进而制备单质硒。
),进而制备单质硒。
(1)基态硒原子核外电子的空间运动状态有________ 种。
(2)甲硒醇(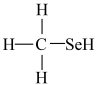 )的熔沸点低于甲醇(
)的熔沸点低于甲醇(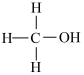 ),原因是
),原因是________________ 。
(3) 亚硒酸溶液中含硒微粒的分布系数
亚硒酸溶液中含硒微粒的分布系数 与溶液
与溶液 的关系如图所示。(分布系数即各组分的平衡浓度占总浓度的分数)
的关系如图所示。(分布系数即各组分的平衡浓度占总浓度的分数)
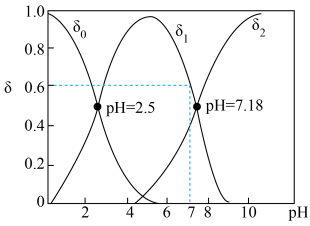
①曲线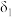 表示的含硒微粒是
表示的含硒微粒是________ 。
②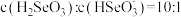 ,溶液
,溶液
________ 。
③向溶液中滴入氨水, 由5.5增大到7.3的过程中,主要反应的离子方程式为
由5.5增大到7.3的过程中,主要反应的离子方程式为________________ , 时,溶液中
时,溶液中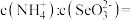
_______ 。
④在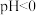 的酸性环境下,向溶液中通入
的酸性环境下,向溶液中通入 制得单质
制得单质 的离子方程式为
的离子方程式为________________ 。
(4) 可以用于测定粗硒中硒的含量,操作步骤如下:
可以用于测定粗硒中硒的含量,操作步骤如下:
Ⅰ.用浓 将样品中的
将样品中的 氧化为
氧化为 ;
;
Ⅱ.用 溶液还原
溶液还原 为
为 ,同时生成
,同时生成 ;
;
Ⅲ.以淀粉为指示剂,用 标准溶液滴定Ⅱ中生成的
标准溶液滴定Ⅱ中生成的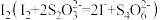 。
。
实验中准确称量 粗硒样品,滴定中消耗
粗硒样品,滴定中消耗 的
的 标准溶液
标准溶液 。
。
①滴定终点的现象为________ 。
②粗硒样品中硒的质量分数为________ 。
 )和硒酸(
)和硒酸( ),进而制备单质硒。
),进而制备单质硒。(1)基态硒原子核外电子的空间运动状态有
(2)甲硒醇(
 )的熔沸点低于甲醇(
)的熔沸点低于甲醇( ),原因是
),原因是(3)
 亚硒酸溶液中含硒微粒的分布系数
亚硒酸溶液中含硒微粒的分布系数 与溶液
与溶液 的关系如图所示。(分布系数即各组分的平衡浓度占总浓度的分数)
的关系如图所示。(分布系数即各组分的平衡浓度占总浓度的分数)
①曲线
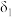 表示的含硒微粒是
表示的含硒微粒是②
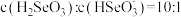 ,溶液
,溶液
③向溶液中滴入氨水,
 由5.5增大到7.3的过程中,主要反应的离子方程式为
由5.5增大到7.3的过程中,主要反应的离子方程式为 时,溶液中
时,溶液中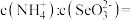
④在
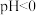 的酸性环境下,向溶液中通入
的酸性环境下,向溶液中通入 制得单质
制得单质 的离子方程式为
的离子方程式为(4)
 可以用于测定粗硒中硒的含量,操作步骤如下:
可以用于测定粗硒中硒的含量,操作步骤如下:Ⅰ.用浓
 将样品中的
将样品中的 氧化为
氧化为 ;
; Ⅱ.用
 溶液还原
溶液还原 为
为 ,同时生成
,同时生成 ;
;Ⅲ.以淀粉为指示剂,用
 标准溶液滴定Ⅱ中生成的
标准溶液滴定Ⅱ中生成的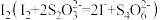 。
。实验中准确称量
 粗硒样品,滴定中消耗
粗硒样品,滴定中消耗 的
的 标准溶液
标准溶液 。
。①滴定终点的现象为
②粗硒样品中硒的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)碳原子2p亚层上的2个电子不相同的方面是____ (选填序号)。
a.能量 b.电子云形状 c.电子云伸展方向 d.自旋状态
14N 原子与12C原子比,质子数和中子数都更多,但原子半径却更小,请解释__________________ 。
(2)铍(Be)与铝性质相似。
①以下对铍及其化合物的推断肯定不正确的是______ (选填序号)。
a.铍会在浓硫酸中钝化 b.氯化铍固体会发生升华现象
c.氧化铍坚硬难熔 d.铍的熔点低于镁
②写出BeCl2溶液和Na2BeO2溶液混合后反应的离子方程式____________________________ 。
(3)将BeCl2溶液加热蒸干后灼热,再使其熔融,用直流电电解,可得到单质铍和一种单质气体,则该气体的化学式为_______ 。
(4)氮化铝(AlN)广泛应用于集成电路,其制备原理是将氧化铝与碳粉混合均匀,在持续流动的氮气流中加热至1750℃,发生如下反应:
2Al2O3(s) 4Al(g)+3O2(g) ①
4Al(g)+3O2(g) ①
2C(s)+ O2(g) 2CO(g) ②
2CO(g) ②
2Al(g)+N2(g) 2AlN(s) ③
2AlN(s) ③
试分析反应②对制备AlN的作用______________________________________________ 。
a.能量 b.电子云形状 c.电子云伸展方向 d.自旋状态
14N 原子与12C原子比,质子数和中子数都更多,但原子半径却更小,请解释
(2)铍(Be)与铝性质相似。
①以下对铍及其化合物的推断肯定不正确的是
a.铍会在浓硫酸中钝化 b.氯化铍固体会发生升华现象
c.氧化铍坚硬难熔 d.铍的熔点低于镁
②写出BeCl2溶液和Na2BeO2溶液混合后反应的离子方程式
(3)将BeCl2溶液加热蒸干后灼热,再使其熔融,用直流电电解,可得到单质铍和一种单质气体,则该气体的化学式为
(4)氮化铝(AlN)广泛应用于集成电路,其制备原理是将氧化铝与碳粉混合均匀,在持续流动的氮气流中加热至1750℃,发生如下反应:
2Al2O3(s)
 4Al(g)+3O2(g) ①
4Al(g)+3O2(g) ① 2C(s)+ O2(g)
 2CO(g) ②
2CO(g) ②2Al(g)+N2(g)
 2AlN(s) ③
2AlN(s) ③试分析反应②对制备AlN的作用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列问题。
(1)现用300mL0.5mol•L﹣1的NaOH溶液吸收2.24L(标准状况下)CO2,完全吸收反应后,所得溶液中离子浓度由大到小的顺序为:___________ 。
(2)现有含有 和
和 的混合溶液,若溶液中
的混合溶液,若溶液中 ,加入碳酸钠调节溶液的pH为
,加入碳酸钠调节溶液的pH为___________ 可使 恰好沉淀完全(离子浓度≤1.0×10-5mol/L),此时
恰好沉淀完全(离子浓度≤1.0×10-5mol/L),此时___________ (填“有”或“无”) 沉淀生成。(假设溶液体积不变,
沉淀生成。(假设溶液体积不变,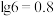 ;
;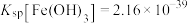 ,
, )
)
(3)生成 沉淀是利用反应
沉淀是利用反应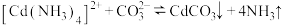 ,常温下,该反应平衡常数
,常温下,该反应平衡常数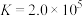 ,
,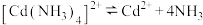 的平衡常数
的平衡常数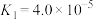 ,则
,则
___________ 。
(4)某小组同学探究饱和 和
和 溶液混合反应的实验,模拟泡沫灭火器的原理。向盛有
溶液混合反应的实验,模拟泡沫灭火器的原理。向盛有 溶液的烧瓶中加入饱和
溶液的烧瓶中加入饱和 溶液,产生大量的白色沉淀并迅速释放出大量气体。出现上述现象的原因是
溶液,产生大量的白色沉淀并迅速释放出大量气体。出现上述现象的原因是___________ (请用反应的离子方程式表示)。
(5)写出下列粒子的价电子排布式:
Fe2+:___________ ;As:___________ 。
(1)现用300mL0.5mol•L﹣1的NaOH溶液吸收2.24L(标准状况下)CO2,完全吸收反应后,所得溶液中离子浓度由大到小的顺序为:
(2)现有含有
 和
和 的混合溶液,若溶液中
的混合溶液,若溶液中 ,加入碳酸钠调节溶液的pH为
,加入碳酸钠调节溶液的pH为 恰好沉淀完全(离子浓度≤1.0×10-5mol/L),此时
恰好沉淀完全(离子浓度≤1.0×10-5mol/L),此时 沉淀生成。(假设溶液体积不变,
沉淀生成。(假设溶液体积不变, ;
;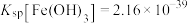 ,
, )
)(3)生成
 沉淀是利用反应
沉淀是利用反应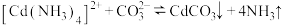 ,常温下,该反应平衡常数
,常温下,该反应平衡常数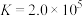 ,
,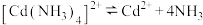 的平衡常数
的平衡常数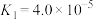 ,则
,则
(4)某小组同学探究饱和
 和
和 溶液混合反应的实验,模拟泡沫灭火器的原理。向盛有
溶液混合反应的实验,模拟泡沫灭火器的原理。向盛有 溶液的烧瓶中加入饱和
溶液的烧瓶中加入饱和 溶液,产生大量的白色沉淀并迅速释放出大量气体。出现上述现象的原因是
溶液,产生大量的白色沉淀并迅速释放出大量气体。出现上述现象的原因是(5)写出下列粒子的价电子排布式:
Fe2+:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】原子结构与元素周期表存在着内在联系。根据已学知识,请回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:第________ 周期第________ 族。
(2)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:____________ 。
(3)写出3p轨道上只有2个未成对电子的元素的符号:____________ 、____________ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:第
(2)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:
(3)写出3p轨道上只有2个未成对电子的元素的符号:
您最近一年使用:0次