有M、V、W、X、Y、Z六种元素,它们的核电荷数依次增大,且都小于20。其中只有X、Z是金属元素;M元素的一种核素原子核内无中子,Z元素原子的最外层只有一个电子;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素原子最外层电子数的一半。V的单质在空气中含量最高。回答下列问题:
(1)M的一种核素中质子数为中子数的 ,则该核素的名称为
,则该核素的名称为__ 。
(2)Z的元素符号为__ 。
(3)X元素的单质与Z的最高价氧化物对应的水化物反应的离子反应方程式为__ 。
(4)Y的单质在加热条件下与铁反应的化学方程式为__ 。
(5)非金属性W__ Y(填大于或小于)
(6)用一个方程式证明W和Y的非金属性强弱__ 。
(7)实验室中,V的最高价氧化物对应的水化物可用Y的最高价氧化物对应的水化物制得,写出相应的化学反应方程式___ 。
(1)M的一种核素中质子数为中子数的
 ,则该核素的名称为
,则该核素的名称为(2)Z的元素符号为
(3)X元素的单质与Z的最高价氧化物对应的水化物反应的离子反应方程式为
(4)Y的单质在加热条件下与铁反应的化学方程式为
(5)非金属性W
(6)用一个方程式证明W和Y的非金属性强弱
(7)实验室中,V的最高价氧化物对应的水化物可用Y的最高价氧化物对应的水化物制得,写出相应的化学反应方程式
更新时间:2020-04-07 15:16:08
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】在下图所示的物质转化中,A、C均为常见的金属单质, 并且在冷的H的浓溶液中均会发生钝化;E为固体非金属单质。B为红色固体氧化物;X为常见无色液体;L的焰色为黄色,且能使酚酞变红(反应过程中生成的水及其他产物已略去)。

回答以下问题:
(1)H的化学式为_________________ 。
(2)L的电子式为__________________ 。
(3)A与B反应的化学方程式为_______________________ 。
(4)K与足量的氨水反应的离子方程式为________________ 。

回答以下问题:
(1)H的化学式为
(2)L的电子式为
(3)A与B反应的化学方程式为
(4)K与足量的氨水反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】已知,短周期A、B、C、D、E、F六种主族元素,它们的原子序数依次增大,其中A的一种原子无中子,B的单质在空气中含量最高,它与A的单质在一定条件下反应生成易溶于水的化合物甲,C、E同主族,C原子的最外层电子数是其周期序数的3倍,D是短周期中原子半径最大的元素。回答下列问题:
(1)E在元素周期表中的位置_______ ,元素F最高价氧化物对应水化合物的化学式为_______ 。
(2)下列叙述中能够证明元素F非金属性强于元素E非金属性的事实为_______ 。
a.一定条件下E和F的单质都能与钠反应
b.F的单质能与E的氢化物反应生成E单质
c.F的氢化物比E的氢化物稳定
d.常温下E单质和F单质状态不同
(3)C的简单氢化物与E的简单氢化物沸点更高的是_______ ,原因是_______ 。
(4)X可能是由B、D、E三种元素中的一种组成的单质,能经图所示的过程转化为W(其它条件略去)。
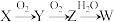
①若Z是淡黄色固体物质,则该物质的电子式为_______ 。
②若是能使品红溶液褪色的有刺激性气味的无色气体,则W的浓溶液与碳共热的化学方程式为_______ 。
③若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂的物质的量之比为_______ ,将铜加入W的稀溶液中发生反应的离子方程式为_______ 。
(1)E在元素周期表中的位置
(2)下列叙述中能够证明元素F非金属性强于元素E非金属性的事实为
a.一定条件下E和F的单质都能与钠反应
b.F的单质能与E的氢化物反应生成E单质
c.F的氢化物比E的氢化物稳定
d.常温下E单质和F单质状态不同
(3)C的简单氢化物与E的简单氢化物沸点更高的是
(4)X可能是由B、D、E三种元素中的一种组成的单质,能经图所示的过程转化为W(其它条件略去)。
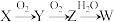
①若Z是淡黄色固体物质,则该物质的电子式为
②若是能使品红溶液褪色的有刺激性气味的无色气体,则W的浓溶液与碳共热的化学方程式为
③若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】已知A~H是中学化学中的常见物质,A、C、G是金属,E、F是氧化物,B溶于水得蓝色溶液,它们有如下图所示的关系(反应中生成的水已略去)。
试回答下列问题。
(1)推断填写物质化学式:A是_______ ,D是________ ,H是________ 。
(2)F的类别是________ (选填“酸性氧化物”、“碱性氧化物”或“两性氧化物”)。
(3)反应④的化学方程式为_________________ 。
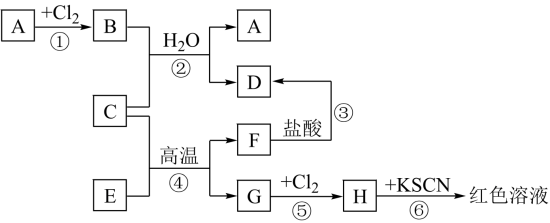
试回答下列问题。
(1)推断填写物质化学式:A是
(2)F的类别是
(3)反应④的化学方程式为

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】硝酸是氧化性酸,其本质是NO 有氧化性,某课外实验小组进行了下列有关NO
有氧化性,某课外实验小组进行了下列有关NO 氧化性的探究(实验均在通风橱中完成)。
氧化性的探究(实验均在通风橱中完成)。
(1)写出铜与稀硝酸反应的离子方程式___ 。
(2)实验Ⅰ中,铝片作___ (填“正”或“负”)极。液面上方产生红棕色气体的化学方程式是___ 。
(3)实验Ⅱ中电流计指针先偏向右边后偏向左边的原因是___ 。
★查阅资料:活泼金属与1mol·L-1稀硝酸反应有H2和NH 生成,NH
生成,NH 生成的原理是产生H2的过程中NO
生成的原理是产生H2的过程中NO 被还原。
被还原。
(4)用如图装置进行实验Ⅲ:溶液X为1mol·L-1稀硝酸溶液,观察到电流计指针向右偏转。反应后的溶液中含NH 。生成NH
。生成NH 的电极发生的反应是
的电极发生的反应是__ (填“氧化反应”或“还原反应”)。
(5)进一步探究碱性条件下NO 的氧化性,进行实验Ⅳ(如图):
的氧化性,进行实验Ⅳ(如图):

①观察到A中有NH3生成,B中无明显现象。A、B产生不同现象的原因是__ 。
②A中生成NH3的离子方程式是___ 。
 有氧化性,某课外实验小组进行了下列有关NO
有氧化性,某课外实验小组进行了下列有关NO 氧化性的探究(实验均在通风橱中完成)。
氧化性的探究(实验均在通风橱中完成)。| 实验装置 | 编号 | 溶液X | 实验现象 |
 | 实验Ⅰ | 6mol·L-1稀硝酸 | 电流计指针向右偏转,铜片表面产生无色气体,在液面上方变为红棕色。 |
| 实验Ⅱ | 15mol·L-1浓硝酸 | 电流计指针先向右偏转,很快又偏向左边,铝片和铜片表面产生红棕色气体,溶液变为绿色。 |
(2)实验Ⅰ中,铝片作
(3)实验Ⅱ中电流计指针先偏向右边后偏向左边的原因是
★查阅资料:活泼金属与1mol·L-1稀硝酸反应有H2和NH
 生成,NH
生成,NH 生成的原理是产生H2的过程中NO
生成的原理是产生H2的过程中NO 被还原。
被还原。(4)用如图装置进行实验Ⅲ:溶液X为1mol·L-1稀硝酸溶液,观察到电流计指针向右偏转。反应后的溶液中含NH
 。生成NH
。生成NH 的电极发生的反应是
的电极发生的反应是(5)进一步探究碱性条件下NO
 的氧化性,进行实验Ⅳ(如图):
的氧化性,进行实验Ⅳ(如图):
①观察到A中有NH3生成,B中无明显现象。A、B产生不同现象的原因是
②A中生成NH3的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】A、B、C、W均为中学常见的物质,它们之间有如图所示的转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行)。

(1)若A、B、C三种物质的焰色反应均为黄色,A俗称苛性钠,W为无色无味气体,C受热分解可转化为B。
①向B溶液中通入W生成C的离子方程式为__________________________________ 。
②A溶液与C溶液反应的化学方程式为______________________________________ 。
(2)若A、B、C三种物质都含有一种金属元素,且B为两性物质,W俗称苛性钠。
①A、B、C三种物质中所含有的金属元素单质与W反应的化学方程式为_____________ 。
②A溶液一步转化为C溶液的反应离子方程式为________________________________ 。
(3)若A、B、C、W四种物质均为气体,其中A、W为单质,C的摩尔质量为46g·mol-1。
①B的化学式为________________ 。
②实验室制取B时,_____________ (填“能”或“不能”)用向上排空气法收集B。
③一定条件下B与CO反应的化学方程式为_____________________________ 。
(4)若A为淡黄色固体单质,W为气体单质,B、C均为酸性氧化物。则C溶于水形成化合物D,在加热的情况下,D的浓溶液与A反应的化学方程式为________________________ 。

(1)若A、B、C三种物质的焰色反应均为黄色,A俗称苛性钠,W为无色无味气体,C受热分解可转化为B。
①向B溶液中通入W生成C的离子方程式为
②A溶液与C溶液反应的化学方程式为
(2)若A、B、C三种物质都含有一种金属元素,且B为两性物质,W俗称苛性钠。
①A、B、C三种物质中所含有的金属元素单质与W反应的化学方程式为
②A溶液一步转化为C溶液的反应离子方程式为
(3)若A、B、C、W四种物质均为气体,其中A、W为单质,C的摩尔质量为46g·mol-1。
①B的化学式为
②实验室制取B时,
③一定条件下B与CO反应的化学方程式为
(4)若A为淡黄色固体单质,W为气体单质,B、C均为酸性氧化物。则C溶于水形成化合物D,在加热的情况下,D的浓溶液与A反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D、E、F是元素周期表前四周期中原子序数依次增大的六种常见元素,其相关信息如下表:
回答下列问题:
(1)元素E在元素周期表中的位于第四周期第__ 族,其高价态离子核外有__ 个未成对电子。
(2)B、C、D三种元素的离子半径由小到大的顺序是______ (用离子符号表示)。
(3)A、D两元素的简单氢化物发生反应生成的化合物的电子式为_______ 。
(4)常温下AD3是一种淡黄色液体。以下关于AD3的说法中,正确的是___________
A.AD3分子中只有非极性键 B.AD3分子中各原子均达8e-稳定结构
C.AD3的晶体属于分子晶体 D.AD3液体气化时化学键被破坏
(5)金属C与E的黑色磁性晶体氧化物在高温下反应,该反应的化学方程式为____________________
(6)向F的硫酸盐溶液中通入AH3气体至过量,观察到的现象是__________ ;该过程总的离子反应式为________________ 向反应后的溶液中加入适量乙醇,析出深蓝色晶体,该晶体中不含有的化学键类型是________ 。
A.配位键 B.极性共价键 C.非极性共价键 D.离子键
元素 | 相 关 信 息 |
A | 原子核外有7种运动状态不同的电子 |
B | 外围电子排布式为nsnnpn+2 |
C | 常见的金属,在周期表中周期序数与族序数相等 |
D | 气态氢化物及最高价氧化物对应的水化物均为强酸 |
E | 一种核素的质量数为56,中子数为30 |
F | 单质紫红色,电缆材料,常见氧化物为黑色 |
(1)元素E在元素周期表中的位于第四周期第
(2)B、C、D三种元素的离子半径由小到大的顺序是
(3)A、D两元素的简单氢化物发生反应生成的化合物的电子式为
(4)常温下AD3是一种淡黄色液体。以下关于AD3的说法中,正确的是
A.AD3分子中只有非极性键 B.AD3分子中各原子均达8e-稳定结构
C.AD3的晶体属于分子晶体 D.AD3液体气化时化学键被破坏
(5)金属C与E的黑色磁性晶体氧化物在高温下反应,该反应的化学方程式为
(6)向F的硫酸盐溶液中通入AH3气体至过量,观察到的现象是
A.配位键 B.极性共价键 C.非极性共价键 D.离子键
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】元素周期表中前四周期元素R、W、X、Y、Z的原子序数依次增大,R基态原子中,电子占据的最高能层符号为L,最高能级上只有一个空的原子轨道;X单质是大气的主要成分之一;Y原子的最外层电子数与电子层数之积等于R、W、X三种元素的原子序数之和;Z基态原子的最高能层只有一个电子,其他能层均已充满电子。回答下列问题:
(1)往Z的硫酸盐溶液中通入过量的 ,可生成
,可生成 。
。
①基态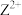 的价电子排布图是
的价电子排布图是_______ ,该络合物阴离子的空间构型是_______ 。
②该化合物加热时首先失去的组分是_______ (写化学式)。
③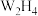 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被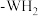 取代形成的另一种W的氢化物。
取代形成的另一种W的氢化物。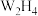 能与硫酸反应生成
能与硫酸反应生成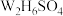 ,
,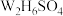 晶体类型为
晶体类型为_______ ,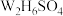 的晶体内存在
的晶体内存在_______ (填序号)。
a.离子键 b.配位键 c.共价键
(2)一种Y与Z形成的化合物的晶胞如图所示(黑点代表Z原子)。

①该晶体的化学式为_______ (用元素符号表示)。
②已知Z和Y的电负性分别为1.9和3.0,则Y与Z形成的化合物属于_______ (填“离子”或“共价”)化合物。
③ 难溶于水,易溶于氨水,原因是
难溶于水,易溶于氨水,原因是_______ 。
(1)往Z的硫酸盐溶液中通入过量的
 ,可生成
,可生成 。
。①基态
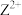 的价电子排布图是
的价电子排布图是②该化合物加热时首先失去的组分是
③
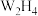 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被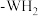 取代形成的另一种W的氢化物。
取代形成的另一种W的氢化物。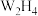 能与硫酸反应生成
能与硫酸反应生成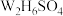 ,
,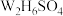 晶体类型为
晶体类型为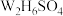 的晶体内存在
的晶体内存在a.离子键 b.配位键 c.共价键
(2)一种Y与Z形成的化合物的晶胞如图所示(黑点代表Z原子)。

①该晶体的化学式为
②已知Z和Y的电负性分别为1.9和3.0,则Y与Z形成的化合物属于
③
 难溶于水,易溶于氨水,原因是
难溶于水,易溶于氨水,原因是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】已知:A、B、C、D、E、F、G七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素.其中A原子在基态时p轨道半充满且电负性是同族元素中最大的;D、E原子核外的M层中均有两个未成对电子;G原子核外价电子数与B相同,其余各层均充满.B、E两元素组成化合物B2E的晶体为离子晶体.C、F的原子均有三个能层,C原子的第一至第四电离能(kJ·mol﹣1)分别为578、1 817、2 745、11 575;C与F能形成原子数目比为1:3、熔点为190℃的化合物Q.
(1)B的单质晶体为体心立方堆积模型,其配位数为_____ ;E元素的最高价氧化物分子的立体构型是______ .F元素原子的价电子排布图是_____ ,G的高价离子与A的简单氢化物形成的配离子的化学式为_____ .
(2)试比较B、D分别与F形成的化合物的熔点高低并说明理由__________ .
(3)A、G形成某种化合物的晶胞结构如图所示.若阿伏伽德罗常数为NA,该化合物晶体的密度为ag·cm﹣3,其晶胞的边长为_____ cm.

(4)在1.01×105 Pa、T1℃时,气体摩尔体积为53.4L·mol﹣1, 实验测得Q的气态密度为5.00g·L﹣1,则此时Q的组成为__________ .
(1)B的单质晶体为体心立方堆积模型,其配位数为
(2)试比较B、D分别与F形成的化合物的熔点高低并说明理由
(3)A、G形成某种化合物的晶胞结构如图所示.若阿伏伽德罗常数为NA,该化合物晶体的密度为ag·cm﹣3,其晶胞的边长为

(4)在1.01×105 Pa、T1℃时,气体摩尔体积为53.4L·mol﹣1, 实验测得Q的气态密度为5.00g·L﹣1,则此时Q的组成为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】Ⅰ. 已知A、B、C、D、E、F是短周期中六种非金属元素,它们的原子序数依次增大。A元素原子形成离子核外电子数为零,C、D在元素周期表中处于相邻的位置,B原子的最外层电子是内层电子数的2倍。D元素与E元素同主族;E的单质为黄色晶体,易溶于二硫化碳。
(1)请写出元素符号: A_____ B_____ C_____ D_____ E_____ F_______
(2)A的单质与C的单质在一定条件下反应生成化合物X,向X的水溶液中滴加酚酞溶液,可以观察到的实验现象是_______________________________ 。
(3)将9g B单质在足量的D单质中燃烧,所得气体通入1L 1 mol·L-1的NaOH溶液,完全吸收后,溶液中大量存在的离子是_______________ 。
Ⅱ. 下图中A—J分别代表有关反应中的一种物质,它们均为中学化学中的常见物质。已知A—E和F—J中分别含有同一种元素。反应E→A+O2的条件未标出。
请填写下列空白:
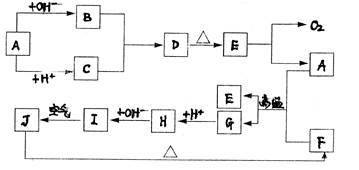
(1) 化合物H中的阳离子是_________ ;D的化学式是_________________ .
(2) A生成B反应的离子方程式是______________________________________ .
(3) B和C反应的离子方程式是________________________________________ .
(4) A和F反应的化学方程式是________________________________________ .
(5) I→J反应的化学方程式是___________________ ,该反应过程中发生的实验现象是______________________ 。
(1)请写出元素符号: A
(2)A的单质与C的单质在一定条件下反应生成化合物X,向X的水溶液中滴加酚酞溶液,可以观察到的实验现象是
(3)将9g B单质在足量的D单质中燃烧,所得气体通入1L 1 mol·L-1的NaOH溶液,完全吸收后,溶液中大量存在的离子是
Ⅱ. 下图中A—J分别代表有关反应中的一种物质,它们均为中学化学中的常见物质。已知A—E和F—J中分别含有同一种元素。反应E→A+O2的条件未标出。
请填写下列空白:

(1) 化合物H中的阳离子是
(2) A生成B反应的离子方程式是
(3) B和C反应的离子方程式是
(4) A和F反应的化学方程式是
(5) I→J反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】D、E、W、R、X、Y均为元素周期表前20号主族元素。根据所学知识,回答下列问题:
(1)化合物 是一种常见的干燥剂,其阳离子和阴离子的电子层结构相同,且
是一种常见的干燥剂,其阳离子和阴离子的电子层结构相同,且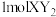 含有
含有 电子。则
电子。则 的化学式是
的化学式是_______ 。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是_______ ;D与E能形成一种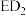 的三原子分子,且每个原子均达到了
的三原子分子,且每个原子均达到了 稳定结构,该分子的结构式为
稳定结构,该分子的结构式为_______ ,化学键类型为_______ (填“离子键”或“共价键”)。
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中反应时有两种产物:加热时生成_______ ,其化学键类型为_______ ,电子式为_______ 。元素R是地壳中含量最多的金属元素,写出R的单质与Z的最高价氧化物对应水化物反应的离子方程式:_______ 。
(1)化合物
 是一种常见的干燥剂,其阳离子和阴离子的电子层结构相同,且
是一种常见的干燥剂,其阳离子和阴离子的电子层结构相同,且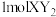 含有
含有 电子。则
电子。则 的化学式是
的化学式是(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是
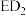 的三原子分子,且每个原子均达到了
的三原子分子,且每个原子均达到了 稳定结构,该分子的结构式为
稳定结构,该分子的结构式为(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中反应时有两种产物:加热时生成
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】已知A、B、C是中学化学常见物质,它们在一定条件下有如下转化关系:

(1)若A能使湿润的红色石蕊试纸变蓝;C为红棕色气体。则A转化为B反应的化学方程式为_____________ .
(2)若D是由地壳中含量最多的元素组成的非金属单质,A为短周期元素中金属性最强的金属单质,则C的电子式为_____________ .
(3)若D为氯碱工业的主要产品,B是一种两性氢氧化物,则B转化为C反应的离子方程式为____________________ .
(4)若D是一中常见金属,A为黄绿色气体,则C溶液在贮存时应加入少量D,其理由是(用必要的文字和离子方程式说明)___________ .
(5)若D 是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴阳离子均含10个电子,则B转化为C的离子方程式为_____________ .
(6)若A、B、C均为氧化物,D是一种黑色固态非金属单质,则B分子的结构式为_________ .

(1)若A能使湿润的红色石蕊试纸变蓝;C为红棕色气体。则A转化为B反应的化学方程式为
(2)若D是由地壳中含量最多的元素组成的非金属单质,A为短周期元素中金属性最强的金属单质,则C的电子式为
(3)若D为氯碱工业的主要产品,B是一种两性氢氧化物,则B转化为C反应的离子方程式为
(4)若D是一中常见金属,A为黄绿色气体,则C溶液在贮存时应加入少量D,其理由是(用必要的文字和离子方程式说明)
(5)若D 是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴阳离子均含10个电子,则B转化为C的离子方程式为
(6)若A、B、C均为氧化物,D是一种黑色固态非金属单质,则B分子的结构式为
您最近一年使用:0次


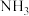 通过热的固体Z制备氮气,该反应的化学方程式是
通过热的固体Z制备氮气,该反应的化学方程式是

