山东省青岛市莱西市济南路中学2022-2023学年八年级上学期期中化学试题
山东
八年级
期中
2022-11-06
136次
整体难度:
适中
考查范围:
身边的化学物质、物质的化学变化、物质构成的奥秘、化学实验
一、选择题 添加题型下试题
| A.空气是一种宝贵的自然资源 | B.二氧化碳是导致酸雨的主要气体 |
| C.氧气的化学性质比较活泼,常温下能与所有物质发生反应 | D.空气质量报告中所列的空气质量级别数越大,说明空气的质量越好 |
| A.水果腐烂 | B.酥脆饼干久置变软 |
| C.木炭燃烧 | D.动植物呼吸 |
| A.“人造空气”比空气中的氮气含量高 |
| B.燃着的蜡烛在“人造空气”中会熄灭 |
C.可以利用反应2Cu+O2 2CuO,测定“人造空气”中O2的含量 2CuO,测定“人造空气”中O2的含量 |
| D.“人造空气”若只含有O2会更有益于人的呼吸 |
| A.空气是由多种单质、化合物组成的混合物 |
| B.拉瓦锡通过定量实验得出了空气主要由氧气和氮气组成的结论 |
| C.二氧化碳增多会引起温室效应,但它不是空气污染物 |
| D.自然界中的水循环和氧循环都是物理变化 |
| A.碳在氧气中燃烧发出白光,生成二氧化碳 |
| B.镁在空气中燃烧发出耀眼的白光,生成白色固体 |
| C.红色的铜粉在空气中加热变黑 |
| D.红磷在空气中燃烧冒出大量白烟 |
| A.工业上可采用分离液态空气法制取氧气 |
| B.氧气支持燃烧,生成白色固体 |
| C.在空气中不燃烧的物质,在氧气中可能会燃烧 |
| D.氧气可用排水法或向上排空气法收集 |

| A.I类反应放出热量,II类反应吸收热量 |
| B.I、II两类反应均体现了氧气的可燃性 |
| C.Fe在I、II两类反应中的剧烈程度不相同,产物也不相同 |
| D.它们发生的都是化合反应 |
| A.催化剂只能加快其他物质的化学反应速率 |
| B.实验室制氧气时,不加MnO2,过氧化氢就不分解 |
| C.反应后,催化剂的质量和化学性质均不发生改变 |
| D.在过氧化氢分解的实验中,若不加催化剂,生成氧气的总质量会减小 |
【知识点】 催化剂的概念、性质与用途解读 催化作用解读 过氧化氢制取氧气实验解读
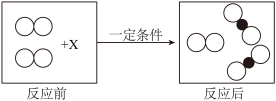
A. | B.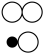 | C.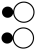 | D. |
【知识点】 质量守恒定律的微观解释解读
| A.质量守恒定律为定量揭示化学变化的规律提供了理论依据 |
| B.通过化学变化,只能改变世界上物质的种类,不能改变物质的总质量 |
| C.24g镁在空气中完全燃烧生成40g氧化镁,实际消耗空气的质量为16g |
| D.质量守恒定律揭示了化学变化中宏观物质之间的质量关系,与微观过程无关 |
| A.CO | B.CO2 | C.SO2 | D.NO2 |
【知识点】 用质量守恒定律确定物质组成解读 空气质量报告解读
①反应所需要的条件 ②化学反应速率的快慢 ③该反应中的反应物和生成物 ④各反应物和生成物的微粒个数比 ⑤反应中各物质的质量比 ⑥反应过程中的能量变化
| A.①③④⑤ | B.③④⑤⑥ | C.①②③⑥ | D.②③⑤⑥ |
 和
和 分别表示两种元素的原子。下列化学方程式符合图示反应关系的是
分别表示两种元素的原子。下列化学方程式符合图示反应关系的是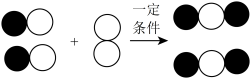
A.2CO+O2 2CO2 2CO2 |
B.N2+3H2 2NH3 2NH3 |
C.C +O2 CO2 CO2 |
D.2Mg +O2 2MgO 2MgO |

| A.甲是单质,乙、丙、丁均为氧化物 |
| B.生成物丙由1个碳原子、4个氢原子和1个氧原子构成 |
| C.参加反应的甲和乙的分子个数比为3:1 |
| D.生成物丙中碳、氢和氧元素的质量比为1:4:1 |
【知识点】 质量守恒定律的微观解释解读 根据化学方程式计算质量比解读
| 物质 | M | N | Q | P |
| 反应前质量(g) | 18 | 1 | 2 | 32 |
| 反应后质量(g) | X | 26 | 2 | 12 |
| A.该变化的基本反应类型是分解反应 | B.反应后物质M的质量为l3g |
| C.反应中N、P的质量比为5:4 | D.物质Q可能是该反应的催化剂 |
A.  | B.  |
C. | D. |
二、多选题 添加题型下试题

| A.饱和溶液和浓溶液属于包含关系 | B.化合物和氧化物属于包含关系 |
| C.单质和化合物属于交叉关系 | D.氧化反应和化合反应属于交叉关系 |
三、选择题 添加题型下试题
| 项目 物质 | X | Y | Q | R |
| 相对分子质量 | 18 | 44 | ||
| 参加反应或生成的物质的质量(g) | 1.6 | a | b | 4.4 |
| A.23:9 | B.46:9 | C.32:9 | D.16:9 |
【知识点】 有关质量守恒定律的计算解读 不含杂质的化学方程式计算解读
四、多选题 添加题型下试题
| A.一定含有碳、氢、氧元素 | B.一定含有碳、氢元素,可能含有氧元素 |
| C.柠檬醛的化学式为C5H8O | D.碳、氢元素的质量比为15:2 |
五、选择题 添加题型下试题
| 物资 | C3H8O | O2 | H2O | CO2 | X |
| 反应前质量/g | 6.0 | 12.8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 8.8 | a |
| A.X 不可能含有氢元素 | B.X 可能是该反应的催化剂 |
| C.表中 a 的值为 3.8 | D.若 O2 的质量是 15.4g,则 a 的值为 5.4 |
【知识点】 有关质量守恒定律的计算解读
六、填空与简答 添加题型下试题
空气中含量最多的气体是
【知识点】 空气各成分及其体积分数解读 空气中各成分的用途解读

(1)液氧和氧气属于同一种物质的原因是
(2)工业制取氧气属于
(3)能利用上述方法分离氧气和氮气的依据是
(4)储存在蓝色钢瓶里的“工业液氧”是
(5)用
(6)蓝色钢瓶中液氧的用途
七、实验题 添加题型下试题

(1)木炭在图②中燃烧比木炭在空气中更剧烈,请从微观角度解释其原因:
(2)在图③中的实验现象是
(3)图④中螺旋状铁丝的末端系一根火柴的作用是
(4)图⑥的现象:铁丝在
(5)实验完后图⑥中的集气瓶炸裂了,请说明原因
八、填空与简答 添加题型下试题
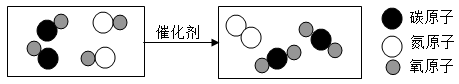
(1)该微观反应中出现了
(2)该反应的化学方程式为
(3)依据上图,试写出你能获得的关于化学变化的信息:宏观:
九、实验题 添加题型下试题
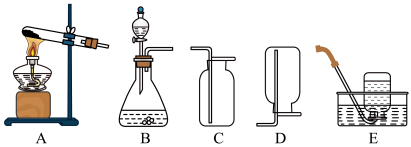
(1)实验室用过氧化氢溶液和二氧化锰固体制取氧气的化学方程式为
(2)一直常温常压下,氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,水溶液显碱性。下列两种反应原理均可用于实验室制备氨气。
第一方案:浓氨水和生石灰固体混合:
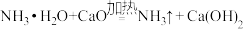
第二方案:氯化铵固体和氢氧化钙粉末混合加热:

若选用A装置制备氨气,应选择的反应原理是第
(3)实验室制取气体时,不需要考虑的因素是 (选填字母序号)。
| A.反应原理 | B.发生和收集装置 | C.检验和验满方法 | D.气体的颜色 |

(1)玻义耳实验中,金属灰增加的质量是
(2)从质量守恒定律的发现历史过程,带给我们的启示有 (填字母);
| A.要善于总结前人的成果和经验 | B.实验的成功与否,取决于药品的选择 |
| C.定量方法是科学研究的重要方法 | D.有效控制实验影响因素是实验准确计量的前提 |
(4)随后同学用白磷(白磷与红磷组成相同,白磷着火点为40℃)验证质量守恒定律,同学将橡皮塞上的细玻璃管下端放到酒精灯火焰上灼烧至红热后,迅速用橡皮塞讲锥形瓶塞紧,并引燃白磷,实验过程如下图所示。请回答问题:

①实验中气球的作用是:
②实验完毕要将C放到天平上称量,而不是B的原因是
【知识点】 实验探究质量守恒定律解读
第一步:讲集气瓶容积划为五等份,并做好标记。
第二步:点燃燃烧池内的红磷,伸入集气瓶中并把塞子塞紧。
第三步:待红磷熄灭并冷却后,打开弹簧夹,请回答下列问题:
(1)用图1当然少并停止冷却后打开弹簧夹,看到
(2)某同学对实验进行反思后,提出了改进方法(如图2所示),你认为改进后的优点是:

(3)测定空气中氧气含量还可以用下面的两套装置图,请结合图示回答有关问题。

①根据下表提供的实验数据,完成下表。
| 硬质玻璃管中空气的体积 | 反应前注射器中的空气体积 | 反应后注射器中气体体积 | 实验侧耳空气中氧气的体积分数 |
| 44mL | 36mL | 24mL |
②装置一盒装纸二中气球的位置不同,
③若实验测得的结果偏小(氧气的体积分数小于21%),可能的原因有哪些?(列举两条)
④实验完毕后,待装置冷却至室温后,若没有将气球中的气体全部挤出就读数,会使结果
十、计算题 添加题型下试题
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150g | 12g | 157.6g | |
已知反应的化学方程式为:
 。
。(1)生成二氧化碳的质量为
(2)求该石灰石中碳酸钙的质量分数。
【知识点】 有关质量守恒定律的计算解读 含杂质的化学方程式计算解读
试卷分析
试卷题型(共 30题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 空气中各成分的用途 空气的污染与防治 空气质量报告 物质与氧气反应的共性分析 | 单选题 |
| 2 | 0.85 | 证明空气及各成分的存在及性质 自然界的氧循环 木炭在氧气中燃烧及其实验 缓慢氧化 | 单选题 |
| 3 | 0.65 | 测定空气中氧气的含量实验的过程 证明空气及各成分的存在及性质 氧气助燃性及实验 | 单选题 |
| 4 | 0.65 | 化学变化与物理变化判断 单质和化合物的判断 拉瓦锡测定空气组成的实验 空气质量报告 | 单选题 |
| 5 | 0.85 | 空气质量报告 | 单选题 |
| 6 | 0.85 | 测定空气中氧气的含量实验的过程 木炭在氧气中燃烧及其实验 金属与氧气反应 镁在氧气中燃烧及其实验 | 单选题 |
| 7 | 0.85 | 氧气助燃性及实验 空气和氧气中的燃烧现象差异 工业制取氧气 氧气的制取中装置的选择 | 单选题 |
| 8 | 0.65 | 化合反应 铁在氧气中燃烧及其实验 缓慢氧化 钢铁的锈蚀 | 单选题 |
| 9 | 0.85 | 催化剂的概念、性质与用途 催化作用 过氧化氢制取氧气实验 | 单选题 |
| 10 | 0.65 | 实验探究质量守恒定律 | 单选题 |
| 11 | 0.94 | 质量守恒定律的微观解释 | 单选题 |
| 12 | 0.85 | 质量守恒定律内容及适用范围 质量守恒定律的微观解释 有关质量守恒定律的计算 用质量守恒定律解释现象 | 单选题 |
| 13 | 0.85 | 用质量守恒定律确定物质组成 空气质量报告 | 单选题 |
| 14 | 0.85 | 化学方程式含义 | 单选题 |
| 15 | 0.65 | 化合反应 化学方程式的书写 根据方程式推测化学式 | 单选题 |
| 16 | 0.65 | 质量守恒定律的微观解释 根据化学方程式计算质量比 | 单选题 |
| 17 | 0.65 | 催化剂的概念、性质与用途 分解反应 有关质量守恒定律的计算 | 单选题 |
| 18 | 0.85 | 质量守恒定律内容及适用范围 木炭在氧气中燃烧及其实验 | 单选题 |
| 20 | 0.65 | 有关质量守恒定律的计算 不含杂质的化学方程式计算 | 单选题 |
| 22 | 0.65 | 有关质量守恒定律的计算 | 单选题 |
| 二、多选题 | |||
| 19 | 0.65 | 氧化反应概念及判断 单质和化合物的判断 氧化物的定义 饱和溶液和不饱和溶液判断 | |
| 21 | 0.4 | 用质量守恒定律确定物质组成 根据化学式计算元素质量比 | |
| 三、填空与简答 | |||
| 23 | 0.85 | 空气各成分及其体积分数 空气中各成分的用途 | 填空题 |
| 24 | 0.65 | 纯净物和混合物的判断 分子、原子的区别与联系 空气中各成分的用途 工业制取氧气 | 填空题 |
| 26 | 0.65 | 质量守恒定律的微观解释 化学方程式的书写 氧化物的定义 化学式图示的分析 | 填空题 |
| 四、实验题 | |||
| 25 | 0.85 | 微粒的观点解释现象 铁在氧气中燃烧及其实验 木炭在氧气中燃烧及其实验 | |
| 27 | 0.65 | 氧气的检验及验满 实验室制取气体的一般思路 气体发生、收集装置 气体的收集方式 | |
| 28 | 0.65 | 实验探究质量守恒定律 | |
| 29 | 0.4 | 空气各成分及其体积分数 测定空气中氧气的含量实验的过程 测定空气中氧气含量的实验误差分析 测定空气中氧气含量实验的改进 | |
| 五、计算题 | |||
| 30 | 0.65 | 有关质量守恒定律的计算 含杂质的化学方程式计算 | |







