2023江苏省泰州市海陵区泰州中学附属初级中学中考考前必刷化学试题1
江苏
九年级
模拟预测
2023-04-29
203次
整体难度:
容易
考查范围:
物质的化学变化、身边的化学物质、物质构成的奥秘、化学与社会发展、化学实验
一、选择题 添加题型下试题
| A.火碱 、碳酸钠 、Na2CO3 | B.熟石灰 、氧化钙、 CaO |
| C.生石灰 、碳酸钙、 CaCO3 | D.烧碱、 氢氧化钠 、NaOH |
【知识点】 常见酸、碱的俗称及化学式解读
| A.打开盛浓盐酸的瓶塞有白烟生成 | B.小木条蘸取浓硫酸后,小木条变黑 |
| C.硫在空气中燃烧发出蓝紫色火焰 | D.稀硫酸能使紫色石蕊溶液变蓝 |
A.地壳中元素含量 | B.化合反应和分解反应关系模型 |
C.物质的组成构成 | D.物质分类模型 |
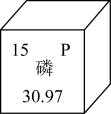
| A.磷元素为非金属元素 | B.磷原子核外有15个电子 |
| C.磷的原子序数为15 | D.相对原子质量为30.97g |
| A.浓硫酸 | B.浓盐酸 |
| C.烧碱溶液 | D.澄清石灰水 |
【知识点】 浓酸敞口放置的变化和现象解读 强碱露置在空气中的变质解读
 和氧气。下列对R的叙述中,正确的是
和氧气。下列对R的叙述中,正确的是| A.只含氧元素 | B.一定含有钙元素和氧元素 |
| C.只含钙元素 | D.一定含有钙元素,可能含有氧元素 |
【知识点】 质量守恒定律的微观解释解读 用质量守恒定律确定物质组成解读
| A.蚁酸是氧化物 |
| B.蚁酸是由碳、氢、氧三种原子构成 |
| C.蚁酸中碳、氧元素的质量比为1:2 |
| D.蚁酸中氢元素质量分数最小 |

| A.t1℃时,等质量的甲、乙溶液中所含溶质的质量为乙>甲 |
| B.t2℃时,20g丙能溶解于50g水中形成70g溶液 |
| C.若要将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法 |
| D.t3℃时,将甲、乙、丙三种物质的饱和溶液降温到t2℃,所得溶液溶质质量分数的大小关系为:乙>甲=丙 |
【知识点】 固体溶解度曲线的应用解读 图像分析溶质质量分数的变化解读
| A.铝片表面有致密的氧化物保护膜 |
| B.反应前CuCl2溶液中含有两种阳离子 |
| C.反应后Cu2+全部转化为Cu |
| D.铝的金属活动性比铜强 |
【知识点】 金属活动顺序理解和判断解读
A.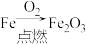 | B.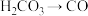 |
C.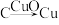 | D.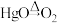 |
| A.活泼金属与盐酸反应有气体产生,则与盐酸反应产生气体的一定是活泼金属 |
| B.化学反应伴随能量变化,所以金属锈蚀过程中一定伴随能量变化 |
| C.通常情况下,物质燃烧需要氧气,所以有氧气参与的反应一定是燃烧 |
| D.单质一定是由同种元素组成的物质,则由同种元素组成的物质一定是单质 |
| A.1个 | B.2个 | C.3个 | D.4个 |
【知识点】 金属活动顺序理解和判断解读
选项 | 物质 | 杂质 | 试剂和操作方法 |
A | 二氧化碳 | 一氧化碳 | 将混合气体通过足量灼热的氧化铜 |
B | 碳酸钙 | 氧化钙 | 高温煅烧 |
C | 氯化铁溶液 | 稀盐酸 | 加入足量铁粉,充分反应后过滤 |
D | 硝酸钠溶液 | 硫酸钠溶液 | 滴加过量的硝酸钡溶液,过滤 |
| A.A | B.B | C.C | D.D |
二、多选题 添加题型下试题

A.高温煅烧石灰石的反应原理为 |
| B.流程图中操作①是“过滤”,操作②是“蒸发” |
| C.流程图中所有元素的化合价均没有发生改变 |
| D.为了验证溶液M与碳酸钠溶液是否恰好完全反应,可取反应后的上层清液,加入无色酚酞试液检验 |
【知识点】 碳酸氢钠、碳酸钠、碳酸钙解读
三、填空与简答 添加题型下试题
(1)标出氨气中氮元素的化合价
(2)氨气具有可燃性,存在燃烧而引发爆炸的可能性,燃烧的化学方程式为:
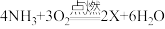 ,其中X的化学式为
,其中X的化学式为(3)氨气极易溶于水形成氨水,在水中电离形成铵根离子
(4)氨气可用稀硫酸吸收生成硫酸铵,硫酸铵属于化肥中的
(5)医生给胃酸过多的病人所开处方中,常包括含Al(OH)3的药物,试用化学方程式表示其治疗原理:
(6)正常雨水通常显酸性,请你用化学方程式解释其原理
四、实验题 添加题型下试题
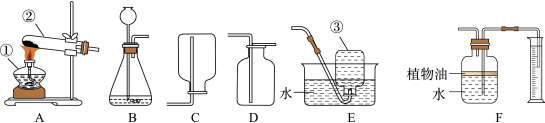
(1)写出带标号仪器的名称:①
(2)常温下,用过氧化氢溶液和二氧化锰反应制取氧气,应选用的发生装置是
(3)F装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是
(4)实验室也常用A装置制备甲烷(CH4)气体,推测其反应物是______(填序号)
| A.醋酸钠和碱石灰的固体混合物 | B.Na2CO3固体和水 | C.CO2和H2 |
五、填空与简答 添加题型下试题
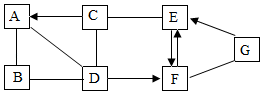
(1)写出B的化学式
(2)A和D反应的基本反应类型为
(3)写出C﹣E反应的化学方程式
(4)写出F→E反应的化学方程式
六、科学探究题 添加题型下试题
【实验探究】
实验一:如图1所,打开止水夹K,将注射器乙中气体全部注入到注射器甲中、关闭止水夹K,充分振荡。实验中注射器甲的活塞先向左、后向右移动,最后示数为仍2mL。
实验二:向盛有湿的CO2的密闭容器中加入NaOH固体,用湿度传感器测定容器内相对湿度的变化如图2(已知一定体积的密闭湿润气体,其温度越高相对湿度越低)。
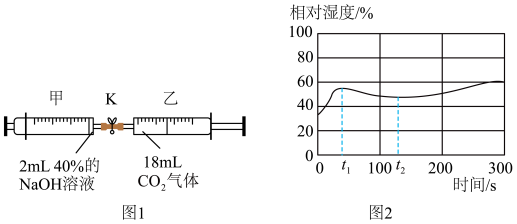
【实验分析】(1)CO2与NaOH反应的化学方程式为
(2)实验一中注射器甲的活塞向右移动是因为容器内压强变
(3)实验二中0~t1s内曲线上升的原因是
(4)实验一和实验二分别设想从
【总结反思】(1)可以采用多种手段从不同角度证明化学反应的进行。
(2)实验一要得出正确结论,还需做对比实验或查阅该温度时
(3)实验二中t1s后曲线先下降后上升,
【提出问题】气体的成分是什么?
【猜想假设】猜想一:只有SO2
猜想二:只有H2
猜想三:
【查阅资料】(Ⅰ)SO2可以使品红溶液褪色
(Ⅱ)SO2可以和碱性溶液反应
(Ⅲ)

【实验探究】用下图装置验证猜想(部分夹持仪器省略)

【方案设计】
| 主要实验步骤 | 主要现象 | 解释或结论 |
| ①打开止水夹,先通入一段时间N2 | ||
| ②关闭止水夹,将足量Zn条下放,浸入浓硫酸中,点燃E装置处酒精灯 | B装置处品红溶液褪色 E装置处 | 猜想三成立 |
| ③结束实验 |
(1)在步骤①中,通入N2的目的是:
(2)请你设计一个实验,用化学方法证明E装置中CuO未完全反应。
| 实验步骤 | 实验现象 | 结论 |
| CuO未完全反应 |
(1)请你根据上述实验探究,补充Zn与浓硫酸反应的化学方程式Zn+ 2H2SO4=ZnSO4+SO2↑+
(2)已知A1与H2一样,在加热条件下能与CuO发生化学反应,请写出该反应的化学方程式
【知识点】 金属与酸反应原理解读 设计实验探究物质的成分解读
七、综合应用题 添加题型下试题
①
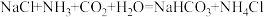
②
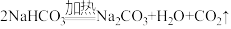
(1)侯氏制碱法所制的“碱”是指
(2)工业生产过程中,铵盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,在常温下,两者首先从溶液中结晶析出的是
下图是从海水中制备纯碱和金属镁的流程:

(3)第Ⅲ步反应的化学方程式为
(4)步骤V中所加试剂是
(5)结合上表分析,析出 NaHCO3晶体的原因可能有______(填序号)
| A.溶剂质量减少 |
| B.同温下NaHCO3溶解度小于 NaCl |
| C.生成的NaHCO3质量大于消耗的NaCl质量 |

①当滴入上述稀盐酸至图中B点时,烧杯中溶液里的溶质为
②在Na2CO3和NaCl的混合物样品中,含Na2CO3的质量为
③当滴入上述稀盐酸至图中A点时,试通过计算,求此温度时所得不饱和溶液中溶质的质量
试卷分析
试卷题型(共 21题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 化学性质和物理性质 | 单选题 |
| 2 | 0.85 | 常见酸、碱的俗称及化学式 | 单选题 |
| 3 | 0.94 | 硫在氧气中燃烧及其实验 浓硫酸的物理、化学性质 浓酸敞口放置的变化和现象 常见的酸碱指示剂及其变色情况 | 单选题 |
| 4 | 0.65 | 纯净物和混合物的判断 单质和化合物的判断 物质化学性质的决定因素 地壳中元素的含量 | 单选题 |
| 5 | 0.94 | 原子中各类微粒的数值关系 相对原子质量的概念及有关计算 元素周期表及元素分类 元素周期表信息示意图 | 单选题 |
| 6 | 0.65 | 浓酸敞口放置的变化和现象 强碱露置在空气中的变质 | 单选题 |
| 7 | 0.65 | 质量守恒定律的微观解释 用质量守恒定律确定物质组成 | 单选题 |
| 8 | 0.94 | 氧化物的定义 化学式、分子式及涵义 根据化学式计算元素质量分数 | 单选题 |
| 9 | 0.85 | 固体溶解度曲线的应用 图像分析溶质质量分数的变化 | 单选题 |
| 10 | 0.85 | 金属活动顺序理解和判断 | 单选题 |
| 11 | 0.85 | 铁在氧气中燃烧及其实验 其他制取氧气方法的相关考查 碳单质与某些氧化物的反应 碳及其化合物间相互转化 | 单选题 |
| 12 | 0.85 | 单质和化合物的判断 酸的通性 燃烧的定义及条件 能量转化与化学变化的关系 | 单选题 |
| 13 | 0.85 | 金属活动顺序理解和判断 | 单选题 |
| 14 | 0.65 | 一氧化碳还原氧化铜实验 金属与酸反应原理 碳酸氢钠、碳酸钠、碳酸钙 盐类参与的反应 | 单选题 |
| 二、多选题 | |||
| 15 | 0.4 | 碳酸氢钠、碳酸钠、碳酸钙 | |
| 三、填空与简答 | |||
| 16 | 0.65 | 根据方程式推测化学式 化合价代数和的计算与应用 空气的污染与防治 常见化肥的种类及性质 | 填空题 |
| 18 | 0.85 | 碳及其化合物间相互转化 金属与盐溶液反应 工业炼铁的原理及装置 酸的通性 | 推断题 |
| 四、实验题 | |||
| 17 | 0.65 | 过氧化氢制取氧气实验 氧气的制取中装置的选择 常见仪器及制材的辨认 气体发生、收集装置 | |
| 五、科学探究题 | |||
| 19 | 0.4 | 碱的通性 | |
| 20 | 0.65 | 金属与酸反应原理 设计实验探究物质的成分 | |
| 六、综合应用题 | |||
| 21 | 0.65 | 化学方程式的书写 溶质质量分数结合化学方程式的计算 碳酸氢钠、碳酸钠、碳酸钙 盐类参与的反应 | |




