小组同学收集了某种铝制易拉罐,剪成条状并打磨后进行如图所示实验,发现纯铝片表面有划痕。
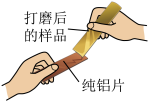
【发现问题】根据所学知识,合金的硬度比组成它的纯金属硬度更大,结合上述现象,可得出该易拉罐不是纯铝制作。那么易拉罐中除铝外,还含有什么金属呢?
【查阅资料】①铝制易拉罐中的主要成分是铝,可能还含有镁、铁。
②铝能与氢氧化钠溶液反应:2Al +2NaOH +2H2O=2NaAlO2 +3H2↑;镁和铁不能与氢氧化钠溶液反应。
【作出猜想】该易拉罐的金属组成除铝外,可能还含有镁、铁中的一种或两种。
【实验设计】小明取打磨后的铝制易拉罐样品按如下方案进行实验:
【实验结论】小明得出该易拉罐是由铝和铁组成。
【反思评价】其他同学分析后认为小明的实验方案不严谨,理由是______ ;大家认为应该补充下列实验:取步骤(1)中少量黑色粉末于试管中,加入某种金属化合物的溶液后,既能有明显现象,又能证明结论正确,你认为加入的这种金属化合物的溶液阳离子对应的金属,理论上可以是______ 。
【拓展应用】下图为国家颁布的“城市生活垃圾分类标志”,废弃易拉罐应放入标有______ (填序号)图标的垃圾桶内。


【发现问题】根据所学知识,合金的硬度比组成它的纯金属硬度更大,结合上述现象,可得出该易拉罐不是纯铝制作。那么易拉罐中除铝外,还含有什么金属呢?
【查阅资料】①铝制易拉罐中的主要成分是铝,可能还含有镁、铁。
②铝能与氢氧化钠溶液反应:2Al +2NaOH +2H2O=2NaAlO2 +3H2↑;镁和铁不能与氢氧化钠溶液反应。
【作出猜想】该易拉罐的金属组成除铝外,可能还含有镁、铁中的一种或两种。
【实验设计】小明取打磨后的铝制易拉罐样品按如下方案进行实验:
| 实验步骤 | 实验现象 | 解释与结论 |
| ①取一定量的样品于烧杯中,加入足量的 | 固体表面有大量气泡产生,过滤后得到黑色粉末。 | 样品中含铝 |
| ②取少量上述黑色粉末于试管中,加入足量的稀盐酸。 | 有气泡产生,溶液变成浅绿色。 | 样品中含铁 |
【反思评价】其他同学分析后认为小明的实验方案不严谨,理由是
【拓展应用】下图为国家颁布的“城市生活垃圾分类标志”,废弃易拉罐应放入标有

更新时间:2021-04-04 21:19:33
|
相似题推荐
【推荐1】学习小组对影响铁生锈的因素进行研究。
(1)如图所示,分别将浸过食醋的钢丝绒、浸过水的钢丝绒和干燥的钢丝绒放入试管A、B、C中,测得玻璃管中水上升的高度。实验结果记录如表,试回答下列问题:
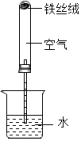
①从实验数据可知,影响铁生锈的因素有:______ (填写字母)。
a.试管中是否有水
b.烧杯中的水量
c.钢丝绒浸过的液体种类
d.实验消耗的时间
e.试管大小
②日常生产生活中可以用稀硫酸来除铁锈,铁锈的主要成分是_____________ (填化学式)。
③如果使用较细的玻璃管,则 A 试管内水面上升的高度将_________ (选填“增加”或“减小”);A 试管内水面上升的原因是_______ 。
④A、B、C三支试管内,钢丝绒生锈的速率由大到小的顺序为_________ 。
(2)对铁“发蓝”处理,其表面将形成致密氧化膜而有效避免腐蚀。为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质。由此可知该零件“发蓝”处理效果___ (填“好”或“不好”),因为_______ (用化学方程式表示)。
(1)如图所示,分别将浸过食醋的钢丝绒、浸过水的钢丝绒和干燥的钢丝绒放入试管A、B、C中,测得玻璃管中水上升的高度。实验结果记录如表,试回答下列问题:

| 时间/h | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| A上升高度/cm | 0 | 0.4 | 3.3 | 5.6 | 6.8 | 9.8 | 13.5 |
| B上升高度/cm | 0 | 0 | 0 | 0 | 0 | 0.5 | 1.0 |
| C上升高度/cm | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
a.试管中是否有水
b.烧杯中的水量
c.钢丝绒浸过的液体种类
d.实验消耗的时间
e.试管大小
②日常生产生活中可以用稀硫酸来除铁锈,铁锈的主要成分是
③如果使用较细的玻璃管,则 A 试管内水面上升的高度将
④A、B、C三支试管内,钢丝绒生锈的速率由大到小的顺序为
(2)对铁“发蓝”处理,其表面将形成致密氧化膜而有效避免腐蚀。为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质。由此可知该零件“发蓝”处理效果
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】古代铁匠常把烧红的铁器浸入水中急速冷却,以增加铁器的硬度,此法称为“淬火”。某兴趣小组的同学设计了如图所示的实验,用以探究铁与水蒸气在高温条件下反应后的产物(注:夹持仪器已省略)。
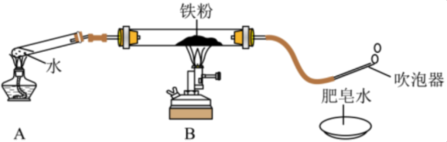
【查阅资料1】常温下没有氧气存在时,铁与水几乎不反应,但高温下铁与水蒸气能反应,生成一种固体和一种气体。
(1)A装置的作用是_____ 。
(2)探究生成的气体是什么?
猜测I:氧气;猜测II:二氧化硫;猜测III:氢气
小红认为不需要做实验就可以排除猜想II,她的理由是____ 。
【实验验证】如图所示,加热一段时间后,灰黑色的铁粉逐渐全部变黑,把导气管放入肥皂水中,吹出的肥皂泡上升飘到空中,用燃着的木条靠近肥皂泡,听到的爆鸣声,说明燃烧产生___ 。
(3)探究玻璃管中剩余黑色固体的成分?
同学们讨论后认为:铁与水蒸气反应生成的固体是“铁的一种氧化物”。玻璃管内的黑色固体中还可能含有“剩余的铁”。
【查阅资料2】
①铁的氧化物有三种:FeO、Fe2O3、Fe3O4,其中仅有Fe2O3为红棕色,FeO、Fe3O4均为黑色,但FeO一接触到空气会立即变成红棕色。
②铁的三种氧化物都不与硫酸铜溶液反应,铁能与硫酸铜溶液反应生成红色物质。
【实验探究】
【实验结论】铁与水蒸气发生反应的化学方程式为_____ 。

【查阅资料1】常温下没有氧气存在时,铁与水几乎不反应,但高温下铁与水蒸气能反应,生成一种固体和一种气体。
(1)A装置的作用是
(2)探究生成的气体是什么?
猜测I:氧气;猜测II:二氧化硫;猜测III:氢气
小红认为不需要做实验就可以排除猜想II,她的理由是
【实验验证】如图所示,加热一段时间后,灰黑色的铁粉逐渐全部变黑,把导气管放入肥皂水中,吹出的肥皂泡上升飘到空中,用燃着的木条靠近肥皂泡,听到的爆鸣声,说明燃烧产生
(3)探究玻璃管中剩余黑色固体的成分?
同学们讨论后认为:铁与水蒸气反应生成的固体是“铁的一种氧化物”。玻璃管内的黑色固体中还可能含有“剩余的铁”。
【查阅资料2】
①铁的氧化物有三种:FeO、Fe2O3、Fe3O4,其中仅有Fe2O3为红棕色,FeO、Fe3O4均为黑色,但FeO一接触到空气会立即变成红棕色。
②铁的三种氧化物都不与硫酸铜溶液反应,铁能与硫酸铜溶液反应生成红色物质。
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①将玻璃管中的黑色固体倒出,平铺于白纸上 | 黑色固体不变色 | 黑色固体中一定没有 |
| ②取少许上述黑色固体加入足量的硫酸铜溶液 | 黑色固体中一定有铁和四氧化三铁 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组为探究金属铝和铜的活动性强弱,开展了以下活动。
【查阅资料】经查阅,金属铝在常温下能与空气中的氧气反应生成致密的氧化铝薄膜。该反应的化学方程式为_________ 。
【对比实验】
(1)比较实验乙和实验_______________ (填“甲”或“丙”)可得知:打磨能破坏氧化铝薄膜。
(2)由实验乙可知:金属活动性Al比Cu____________ (填“强”或“弱”)。
(3)小明同学对实验丙的现象进行分析,认为H2O对氧化铝薄膜有破坏作用。但此观点马上被其他同学否定,否定的依据是_____________ 。
【猜测与探究】小组同学针对实验丙的现象,经讨论后猜测:Clˉ破坏了氧化铝薄膜。为检验此猜测是否正确,他们首先向两支试管中加入相同的CuSO4溶液,并均浸入表面未打磨的铝丝,然后进行了新的探究:
【得出结论】前述猜测正确。
【总结反思】本次探究充分运用了比较法和控制变量法。
【查阅资料】经查阅,金属铝在常温下能与空气中的氧气反应生成致密的氧化铝薄膜。该反应的化学方程式为
【对比实验】
| 编号 | 操作 | 现象 |
| 甲 | 将表面未打磨的铝丝浸入CuSO4溶液中 | 无明显现象 |
| 乙 | 将表面打磨后的铝丝浸入CuSO4溶液中 | 铝丝表面析出红色固体 |
| 丙 | 将表面未打磨的铝丝浸入CuCl2溶液中 | 铝丝表面析出红色固体 |
(1)比较实验乙和实验
(2)由实验乙可知:金属活动性Al比Cu
(3)小明同学对实验丙的现象进行分析,认为H2O对氧化铝薄膜有破坏作用。但此观点马上被其他同学否定,否定的依据是
【猜测与探究】小组同学针对实验丙的现象,经讨论后猜测:Clˉ破坏了氧化铝薄膜。为检验此猜测是否正确,他们首先向两支试管中加入相同的CuSO4溶液,并均浸入表面未打磨的铝丝,然后进行了新的探究:
| 操作 | 现象 | 结论 |
| (1)向一支试管中再加入NaCl固体 | 铝丝表面析出红色固体 | Na+或 |
| (2)向另一支试管中再加入 | 无明显现象 | Na+和SO 都不能破坏氧化铝薄膜 都不能破坏氧化铝薄膜 |
【得出结论】前述猜测正确。
【总结反思】本次探究充分运用了比较法和控制变量法。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】我国已成为易拉罐使用的大国。市场上常见易拉罐的主要材质为铝材和马口铁。
【查阅资料】马口铁,是一种镀锡钢板,具有一定强度和硬度,能被磁铁吸引。



【探究材质】
(1)“旺仔牛奶”罐的材质为马口铁,“雪碧”罐的材质为铝,鉴别两种易拉罐的简单方案是______ 。
(2)常见的碳酸饮料还有用塑料包装的,塑料属于______ (填“无机”或“合成”)材料。与铝制易拉罐相比,简单说明两种材料的优缺点(答一点即可)。
【探究性质】
(3)
【任务一】
(4)铝制易拉罐不需要进行防锈处理的原因是______ 。
【任务二】有同学提出质疑:铝罐能存放雪碧等碳酸饮料吗?
(5)根据金属的化学性质和标签内容,某同学认为铝罐不能存放雪碧等碳酸饮料的理由是:______ 。
于是他们走进实验室,完成了以下实验。
【步骤一】
(6)打开一瓶新买到的雪碧,将易拉罐拉环打开的瞬间,看到有大量的气泡冒出,这是因为______ 。
【步骤二】
(7)用剪刀剪下一块易拉罐,将其外表面用砂纸打磨干净,并浸入足量稀盐酸中,等特几个小时后,固体溶解,发现里面竟然还有一层塑料薄膜。那么加入这层薄膜所起的作用是______ 。
【实验结论】铝制易拉罐是可以存放碳酸饮料的。
【回收利用】
(8)易拉罐属于可回收利用物,回收易拉罐的好处是______ 。
【查阅资料】马口铁,是一种镀锡钢板,具有一定强度和硬度,能被磁铁吸引。



【探究材质】
(1)“旺仔牛奶”罐的材质为马口铁,“雪碧”罐的材质为铝,鉴别两种易拉罐的简单方案是
(2)常见的碳酸饮料还有用塑料包装的,塑料属于
【探究性质】
(3)
铝制易拉罐 | 塑料包装 | |
优点 | 避光性好 | |
缺点 | 透光,保质期相对短 |
【任务一】
(4)铝制易拉罐不需要进行防锈处理的原因是
【任务二】有同学提出质疑:铝罐能存放雪碧等碳酸饮料吗?
(5)根据金属的化学性质和标签内容,某同学认为铝罐不能存放雪碧等碳酸饮料的理由是:
于是他们走进实验室,完成了以下实验。
【步骤一】
(6)打开一瓶新买到的雪碧,将易拉罐拉环打开的瞬间,看到有大量的气泡冒出,这是因为
【步骤二】
(7)用剪刀剪下一块易拉罐,将其外表面用砂纸打磨干净,并浸入足量稀盐酸中,等特几个小时后,固体溶解,发现里面竟然还有一层塑料薄膜。那么加入这层薄膜所起的作用是
【实验结论】铝制易拉罐是可以存放碳酸饮料的。
【回收利用】
(8)易拉罐属于可回收利用物,回收易拉罐的好处是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】教育部从2018年开始,要求在学校普及垃圾分类回收处理的相关知识。某化学活动小组结合所学的知识对此进行一系列实践活动。
I活动探究
(1)学会识图分拣垃圾:下列垃圾应投入带有如图图标的垃圾箱内的是____ (填字母)。

A塑料瓶 B果皮 C碎瓷片
(2)学会检验有害气体:含氯塑料焚烧时会产生氯化氢等气体。
若要检验焚烧后的气体中有氯化氢,可将其通入加有稀硝酸的___________ 溶液中,有白色沉淀生成即可,反应的化学方程式为______________ ,反应的基本类型是_________________ 。
II.实验探究
[提出问题]如何回收处理废旧电池中的铬?
[查阅资料](1)废旧电池中含有镉、汞等元素,这些元素会危害人类健康。
(2)镉(Cd)从溶液中析出时呈海绵状固体。在化合物中通常表现为+2价。
(3)碳酸镉(CdCO3)、氢氧化镉[Cd(OH)2]都是白色固体。难溶于水。
[设计实验]同学们先将废旧电池进行处理以制得硫酸镉(CdSO4)溶液,然后设计了三种不同方案进行回收镉。
[回收处理]实验结束后,将反应后的混合物通过过滤,洗涤、加热,进而再制得镉。
[交流反思]请同学们基于化学视角说明垃圾分类回收处理的重要意义____________ (各一点即可)。
I活动探究
(1)学会识图分拣垃圾:下列垃圾应投入带有如图图标的垃圾箱内的是

A塑料瓶 B果皮 C碎瓷片
(2)学会检验有害气体:含氯塑料焚烧时会产生氯化氢等气体。
若要检验焚烧后的气体中有氯化氢,可将其通入加有稀硝酸的
II.实验探究
[提出问题]如何回收处理废旧电池中的铬?
[查阅资料](1)废旧电池中含有镉、汞等元素,这些元素会危害人类健康。
(2)镉(Cd)从溶液中析出时呈海绵状固体。在化合物中通常表现为+2价。
(3)碳酸镉(CdCO3)、氢氧化镉[Cd(OH)2]都是白色固体。难溶于水。
[设计实验]同学们先将废旧电池进行处理以制得硫酸镉(CdSO4)溶液,然后设计了三种不同方案进行回收镉。
| 实验设计 | 实验步骤 | 实验现象 | 实验结论 |
| 与金属反应 | 取少许溶液于试管中,加入足量的Zn粉,充分反应 | Zn可以置换出Cd | |
| 与碱反应 | 取少许溶液于试管中,加入足量的NaOH溶液, 充分反应 | 产生白色沉淀 | 该反应的化学方程 式 |
| 与盐反应 | 取少许溶液于试管中,加入足量的 | 产生白色沉淀 | 可用该试剂沉淀Cd2+ |
[交流反思]请同学们基于化学视角说明垃圾分类回收处理的重要意义
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】目前,全世界每年生产各种易拉罐约4000亿罐,中国人均年消费24罐。常见的食品金属罐通常有两种,一是铝材,二是马口铁。以下三个易拉罐样品,其罐底的回收标识如图所示,打磨掉三个易拉罐表面油漆,并裁成相同大小的碎片,备用。

活动一:探究3号易拉罐材质是铝材还是马口铁?
(1)以下方案中不可行的是__________(填写序号)
活动二:铝罐、铁罐等金属罐都能被酸腐蚀,饮料中又常含有碳酸、柠檬酸等酸性物质,为何商家用金属罐来盛放饮料呢?探究1号易拉罐能否盛放酸性物质。
(2)
【查阅资料】易拉罐的内壁喷有一层白色薄膜,这层白色薄膜是一种有机材料环氧树脂,其无毒无害,化学性质稳定,不与酸、碱溶液发生化学反应。
【实验小结】
(3)1号易拉罐能盛放酸性物质,原因是____________________
活动三:2号易拉罐的材质是否是纯铁?
取适量的2号易拉罐样品与足量稀硫酸充分反应后,测定生成氢气体积。通过计算逸出的氢气的质量对铁的质量进行计算。已知标准状况下,氢气的密度是0.0899g/L,浓硫酸具有吸水性。实验装置如下:
.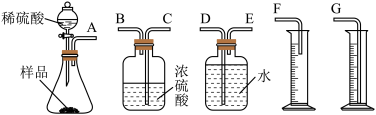
(4)写出导管正确的连接方式:A→__________ →__________ →__________ →__________ →__________ (填“F”或“G”)。
(5)依据表格中测得的实验数据,可以得到结论:2号易拉罐不是纯铁制成,理由:____________________ 。
(6)活动四:马口铁成分较为复杂,用它来再提炼成铁的成本较高,而铝罐的成分中铝要纯得多,容易再次提炼。100个易拉罐重量是1344g,能回收铝锭总重量是1116g。废弃的铝制易拉罐回收的意义是______________________________ (写一条)。

活动一:探究3号易拉罐材质是铝材还是马口铁?
(1)以下方案中不可行的是__________(填写序号)
| A.往易拉罐样品中加入硫酸铜溶液,观察是否有红色固体析出 |
| B.用磁铁吸引易拉罐样品 |
| C.用刀在易拉罐样品上刻出划痕,放在潮湿的空气中,放置一段时间,观察其变化 |
| D.易拉罐样品在火焰上灼烧,观察其变化 |
活动二:铝罐、铁罐等金属罐都能被酸腐蚀,饮料中又常含有碳酸、柠檬酸等酸性物质,为何商家用金属罐来盛放饮料呢?探究1号易拉罐能否盛放酸性物质。
(2)
| 实验步骤 | 实验现象 | 实验结论 |
| 取适量1号易拉罐样品放在试管中,向试管中滴加足量的稀盐酸 | 有气泡生成 | 反应的化学方程式为 |
| 待充分反应后取出样品。 | 只剩下一层白色薄膜 |
【查阅资料】易拉罐的内壁喷有一层白色薄膜,这层白色薄膜是一种有机材料环氧树脂,其无毒无害,化学性质稳定,不与酸、碱溶液发生化学反应。
【实验小结】
(3)1号易拉罐能盛放酸性物质,原因是
活动三:2号易拉罐的材质是否是纯铁?
取适量的2号易拉罐样品与足量稀硫酸充分反应后,测定生成氢气体积。通过计算逸出的氢气的质量对铁的质量进行计算。已知标准状况下,氢气的密度是0.0899g/L,浓硫酸具有吸水性。实验装置如下:
.

| 实验编号 | 样品质量/g | 氢气体积/mL |
| 1 | 0.205 | 75.2 |
| 2 | 0.210 | 76.5 |
| 3 | 0.207 | 76.0 |
(4)写出导管正确的连接方式:A→
(5)依据表格中测得的实验数据,可以得到结论:2号易拉罐不是纯铁制成,理由:
(6)活动四:马口铁成分较为复杂,用它来再提炼成铁的成本较高,而铝罐的成分中铝要纯得多,容易再次提炼。100个易拉罐重量是1344g,能回收铝锭总重量是1116g。废弃的铝制易拉罐回收的意义是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】蔗糖是我们经常接触的一种食品,生活中,我们偶尔会看见蔗糖在锅里,加热时间过长会变成黑色。
【提出问题】蔗糖是由哪些元素组成的?
【做出猜想】小明猜想蔗糖中含碳元素,或许还有其他元素,如氢元素等。
【收集资料】小明、小红在图书馆查到以下资料:
(1)蔗糖属于有机化合物,有机化合物一般可以燃烧,受热易分解,这属于有机化合物的____ (填“物理”或“化学”)性质。
【设计实验】小明、小红分别设计了如下方案进行实验探究:
小明:将蔗糖在空气中点燃。单独点燃蔗糖不易燃烧,但在蔗糖中掺入少量烟灰,蔗糖就很容易被点燃。将干冷的烧杯罩在火焰上方,观察现象。一段时间后向烧杯中倒入澄清石灰水振荡,再观察现象。
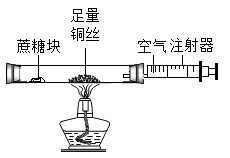
小红:用如图装置进行实验(夹持和支撑装置略去)来测定蔗糖的组成。先用酒精灯在玻璃管铜丝处加热,使之反应后,同时不断反复推拉注射器活塞,再将酒精灯移至蔗糖处进行加热。
【现象与结论】
小明的实验现象为:将干冷的烧杯罩在火焰上方时,观察到烧杯内壁有水珠。向烧杯中倒入澄清石灰水振荡,澄清石灰水(2)_______ ;发生化学反应的化学方程式_______
小红的实验现象为:玻璃管中蔗糖处留下黑色的固体,内壁有水珠。
结论:蔗糖是由碳、氢、氧三种元素组成的。
【反思与评价】
(3)小明的实验中烟灰在反应前后的质量和化学性质没有发生变化,因此烟灰可能起______ 作用。
(4)实验时反复推拉注射器活塞的作用是____ 。
(5)写出铜和氧气反应的化学方程式________ 。
(6)经过分析讨论,小红认为小明的实验并不能得出正确的结论,原因是____ 。

【提出问题】蔗糖是由哪些元素组成的?
【做出猜想】小明猜想蔗糖中含碳元素,或许还有其他元素,如氢元素等。
【收集资料】小明、小红在图书馆查到以下资料:
(1)蔗糖属于有机化合物,有机化合物一般可以燃烧,受热易分解,这属于有机化合物的
【设计实验】小明、小红分别设计了如下方案进行实验探究:
小明:将蔗糖在空气中点燃。单独点燃蔗糖不易燃烧,但在蔗糖中掺入少量烟灰,蔗糖就很容易被点燃。将干冷的烧杯罩在火焰上方,观察现象。一段时间后向烧杯中倒入澄清石灰水振荡,再观察现象。
小红:用如图装置进行实验(夹持和支撑装置略去)来测定蔗糖的组成。先用酒精灯在玻璃管铜丝处加热,使之反应后,同时不断反复推拉注射器活塞,再将酒精灯移至蔗糖处进行加热。
【现象与结论】
小明的实验现象为:将干冷的烧杯罩在火焰上方时,观察到烧杯内壁有水珠。向烧杯中倒入澄清石灰水振荡,澄清石灰水(2)
小红的实验现象为:玻璃管中蔗糖处留下黑色的固体,内壁有水珠。
结论:蔗糖是由碳、氢、氧三种元素组成的。
【反思与评价】
(3)小明的实验中烟灰在反应前后的质量和化学性质没有发生变化,因此烟灰可能起
(4)实验时反复推拉注射器活塞的作用是
(5)写出铜和氧气反应的化学方程式
(6)经过分析讨论,小红认为小明的实验并不能得出正确的结论,原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】近几年,我国有些城市酸雨污染较严重,主要原因是因为大量燃烧含硫量高的煤及机动车排放的尾气所造成的.
【提出问题】煤中是否含有硫元素和碳元素?
【查阅资料】1.二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),该反应的化学方程式为: 5SO2+2KMnO4+2x=K2SO4+2MnSO4+2H2SO4其中x的化学式为___________ ,
②二氧化碳、二氧化硫都能使澄清石灰水变浑浊,请写出二氧化碳与澄清石灰水反应的化学方程式_______
根据上述资料,甲、乙同学进如下实验探究
(1)甲同学进行了如图所示A、B两步实验,观察到的实验现象:

A中_________________ ,B中澄清石灰水变浑浊。
得出结论,煤燃烧生成二氧化硫和二氧化碳,证明煤中含有硫元素和碳元素
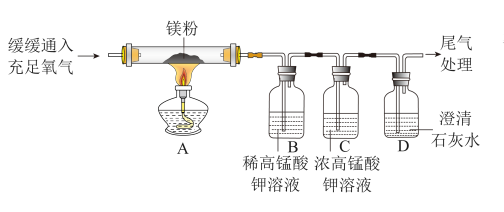
(2)乙同学认为甲同学的方案不合理,理由是_________________________ 他进行了如下图所示实验(夹持装置略去。)
【结论与反思】
(3)上图中C装置的作用是_______________ .
(4)乙同学的实验中证明煤中含有硫元素和碳元素的现象是,B中_____ C中____ D中____ .
【提出问题】煤中是否含有硫元素和碳元素?
【查阅资料】1.二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),该反应的化学方程式为: 5SO2+2KMnO4+2x=K2SO4+2MnSO4+2H2SO4其中x的化学式为
②二氧化碳、二氧化硫都能使澄清石灰水变浑浊,请写出二氧化碳与澄清石灰水反应的化学方程式
根据上述资料,甲、乙同学进如下实验探究
(1)甲同学进行了如图所示A、B两步实验,观察到的实验现象:

A中
得出结论,煤燃烧生成二氧化硫和二氧化碳,证明煤中含有硫元素和碳元素
(2)乙同学认为甲同学的方案不合理,理由是

【结论与反思】
(3)上图中C装置的作用是
(4)乙同学的实验中证明煤中含有硫元素和碳元素的现象是,B中
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某研究性小组在实验室用如图实验装置做木炭还原氧化铜的实验,实验中观察到试管a内发生的现象是 _____ ,试管b内澄清石灰水变浑浊,证明有 _____ 生成.
实验在高温条件下充分反应.兴趣小组对实验后试管a内的固体成分发生了兴趣,激发了探究热情.
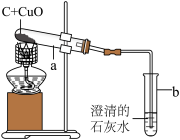
【提出问题】:“反应后试管a内的固体物质是什么?
【进行猜想】:小静同学认为该固体全部是铜;
小华同学认为该固体是铜与氧化铜两种物质的混合物;
小东同学认为该固体是铜与_____ 两种物质的混合物;
小明同学认为该固体可能是铜、木炭和氧化铜三种物质的混合物
小华认为因为是充分反应,所以_____ 同学的猜想明显不成立
【查阅资料】稀硫酸是无色液体:
木炭、铜都不与稀硫酸反应,氧化铜能与稀硫酸反应得到蓝色硫酸铜溶液
【实验设计】
【反思评价】: _____ 同学的评价是正确的;
【定量探究】:现取炭碳与氧化铜的混合物18g,高温条件下充分反应,剩余固体的质量为13.6g,经测定其中氧化铜有剩余,请通过计算确定原混合物中碳和氧化铜各有多少克_____ ?
实验在高温条件下充分反应.兴趣小组对实验后试管a内的固体成分发生了兴趣,激发了探究热情.

【提出问题】:“反应后试管a内的固体物质是什么?
【进行猜想】:小静同学认为该固体全部是铜;
小华同学认为该固体是铜与氧化铜两种物质的混合物;
小东同学认为该固体是铜与
小明同学认为该固体可能是铜、木炭和氧化铜三种物质的混合物
小华认为因为是充分反应,所以
【查阅资料】稀硫酸是无色液体:
木炭、铜都不与稀硫酸反应,氧化铜能与稀硫酸反应得到蓝色硫酸铜溶液
【实验设计】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体物质于试管中,加足量稀硫酸充分振荡 | 黑色固体溶解,溶液变成蓝色 | 固体中有 |
【定量探究】:现取炭碳与氧化铜的混合物18g,高温条件下充分反应,剩余固体的质量为13.6g,经测定其中氧化铜有剩余,请通过计算确定原混合物中碳和氧化铜各有多少克
您最近一年使用:0次
【推荐1】人教版新课标化学教材九年级上册“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【实验探究】
【实验结论】
(1)A中产生的气体是_______ 。
(2)实验II、III证明:氧化铁的_______ 和______ 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(3)写出氧化铁催化过氧化氢分解的文字表达式_______ 。
【实验评价】
(1)设计实验Ⅳ的目的是________ 。
(2)若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是____________ 。
【实验拓展】
查阅资料得知:CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是____________ 。
a.MnO2只能作为过氧化氢溶液分解的催化剂
b.同一个化学反应可以有多种催化剂
c.催化剂只能加快化学反应的速率
d.用作催化剂的物质不可能是其它反应的反应物或生成物
【实验探究】
| 实验步骤 | 实验现象 |
| I.分别量取5mL5%过氧化氢溶液放入A.B两支试管中向A试管中加入ag氧化铁粉末,并分别在A.B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
| II.待A试管中没有现象发生时,重新加入过氧化氢溶液并把带火星的木条伸入试管,如此反复多次实验,观察现象 | 试管中均产生气泡,带火星木条均复燃 |
| III.将实验Ⅱ中的剩余物小心过滤,并将所得虑渣进行洗涤、干燥、称量,所得固体质量仍为ag | / |
| IV.分别量取5mL5%过氧化氢溶液放入C.D两支试管中,向C试管中加入ag氧化铁粉末。向D试管中加入ag二氧化锰粉末,观察现象 | / |
【实验结论】
(1)A中产生的气体是
(2)实验II、III证明:氧化铁的
(3)写出氧化铁催化过氧化氢分解的文字表达式
【实验评价】
(1)设计实验Ⅳ的目的是
(2)若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是
【实验拓展】
查阅资料得知:CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是
a.MnO2只能作为过氧化氢溶液分解的催化剂
b.同一个化学反应可以有多种催化剂
c.催化剂只能加快化学反应的速率
d.用作催化剂的物质不可能是其它反应的反应物或生成物
您最近一年使用:0次
【推荐2】实验室有一瓶敞口放着的氢氧化钠固体,同学们想探究这瓶固体的成分,请你一同参与探究并回答有关问题。
【提出猜想】
猜想1:这瓶固体的成分是NaOH;
猜想2:这瓶固体的成分是Na2CO3;
猜想3:这瓶固体的成分是NaOH和Na2CO3的混合物。
【实验与结论】
(1)取少量样品于试管中,加入适量蒸馏水,振荡,样品全部溶于水,向其中加入无色酚酞溶液,溶液由无色变成红色。甲同学认为这瓶固体是NaOH,猜想1正确。乙同学认为甲同学的结论不正确,其理由是____ 。
(2)向(1)溶液中加入过量的BaCl2溶液,生成白色沉淀,沉淀后静置,溶液由红色变成无色。同学们认为猜想2是正确的。
【问题讨论】
(3)丙同学认为实验时也可以先加入过量的BaCl2溶液,振荡、静置,然后在上层清液中加入无色酚酞溶液,你认为丙同学的说法____ (填“正确”或“不正确”),此时反应的化学方程式为____ ;若猜想3正确,则现象为____ 。
(4)丁同学认为BaCl2溶液也可以改为Ba(OH)2溶液,你认为丁同学的说法____ (填“正确”或“不正确”),理由是_________ 。
【提出猜想】
猜想1:这瓶固体的成分是NaOH;
猜想2:这瓶固体的成分是Na2CO3;
猜想3:这瓶固体的成分是NaOH和Na2CO3的混合物。
【实验与结论】
(1)取少量样品于试管中,加入适量蒸馏水,振荡,样品全部溶于水,向其中加入无色酚酞溶液,溶液由无色变成红色。甲同学认为这瓶固体是NaOH,猜想1正确。乙同学认为甲同学的结论不正确,其理由是
(2)向(1)溶液中加入过量的BaCl2溶液,生成白色沉淀,沉淀后静置,溶液由红色变成无色。同学们认为猜想2是正确的。
【问题讨论】
(3)丙同学认为实验时也可以先加入过量的BaCl2溶液,振荡、静置,然后在上层清液中加入无色酚酞溶液,你认为丙同学的说法
(4)丁同学认为BaCl2溶液也可以改为Ba(OH)2溶液,你认为丁同学的说法
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究。
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变。
Ⅱ、CuO参与反应产生O2 ,反应前后质量和化学性质发生了改变。
Ⅲ、CuO是反应的催化剂,反应前后________________ 。
用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
(2)步骤①的目的是_____________________ 。
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、__________ 。
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为_____________________ 。
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变。
Ⅱ、CuO参与反应产生O2 ,反应前后质量和化学性质发生了改变。
Ⅲ、CuO是反应的催化剂,反应前后
用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
带火星的木条复燃。 | 溶液中有气泡放出, | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立。 |
(2)步骤①的目的是
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为
您最近一年使用:0次



