金属和金属材料与生活和社会发展的关系非常密切。
(1)下列生活用品利用金属良好导热性的是 (填序号)。
(2)铁制品表面刷漆,主要是为了防止其与_________ 、氧气接触而锈蚀。
(3)季梁学校化学兴趣小组同学将定量的锌粉加入到 A1(NO3)3、 Fe (NO3)2、AgNO3,三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。若滤液呈浅绿色,则滤液中一定含有的溶质是_______ (写出化学式)。
(4)淅河一中化学兴趣小组同学将40 g的铜锌合金放入烧杯中,逐渐加入稀硫酸至不再产生气泡时,恰好用去稀硫酸100 g,烧杯内剩余固体27g。 计算所用稀硫酸中溶质的质量分数为___________ 。
(1)下列生活用品利用金属良好导热性的是 (填序号)。
| A.镀铬水龙头 | B.铸铁暖气片 | C.黄铜钥匙 |
(3)季梁学校化学兴趣小组同学将定量的锌粉加入到 A1(NO3)3、 Fe (NO3)2、AgNO3,三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。若滤液呈浅绿色,则滤液中一定含有的溶质是
(4)淅河一中化学兴趣小组同学将40 g的铜锌合金放入烧杯中,逐渐加入稀硫酸至不再产生气泡时,恰好用去稀硫酸100 g,烧杯内剩余固体27g。 计算所用稀硫酸中溶质的质量分数为
更新时间:2022-04-24 15:22:38
|
相似题推荐
填空与简答-科普阅读题
|
适中
(0.65)
名校
解题方法
【推荐1】阅读以下科普短文
铝是当前世界上产量以及用量仅次于铁的金属,在日常生活中有着广泛的用途。铝具有一些特殊的性质,从而还有一些人们意想不到的用途。
金、银等金属由于化学性质不活泼所以在空气中不易被腐蚀,而铁制品一旦保养不善就容易被腐蚀生锈。铝化学性质非常活泼,在干燥的空气中会立即与氧气发生反应而生成一层致密的氧化铝薄膜,阻碍了铝进一步氧化,同时使铝隔绝了水。因此,铝常被制成铝箔用作薯片、坚果、香烟等在空气中易变质物品的包装。同时,由于铝粉保持了银白色的金属光泽(大多数金属粉末呈现黑色),铝粉常用作涂料(俗称“银粉”)在保护铁制品的同时还使其十分美观。
铝还能在一定条件下与一些化学性质稳定的金属氧化物反应,生成相应的金属单质并释放出大量的热。利用这一性质,人们将铝粉与金属氧化物粉末按一定比例混合制成铝热剂,如:铝粉与三氧化二铁混合制得的铁铝热剂。铝热剂是1893年德国的化学家汉斯·歌德史密斯在寻找不需要碳高温还原的方法制备高纯度金属的过程中发明的。歌德史密斯在研究中发现,铝热剂在反应过程中散发出大量的热,使置换出的金属熔化并能流出,从而实现了金属与熔渣的分离。因此,铝热剂在工业上常用来冶炼铬、锰等高熔点的金属,还用于金属焊接。
根据文章内容,回答下列问题:
(1)金、银的金属活动性比铝_________ (填“强”或“弱”)。
(2)某油漆叫做“银粉漆”,其中的“银粉”指的是_________ 。
(3)铝热剂在工业上常用于炼铬、锰等金属的原因_________ 。
(4)铝粉与三氧化二铁混合制得的铁铝热剂反应的化学方程式_________ 。
铝是当前世界上产量以及用量仅次于铁的金属,在日常生活中有着广泛的用途。铝具有一些特殊的性质,从而还有一些人们意想不到的用途。
金、银等金属由于化学性质不活泼所以在空气中不易被腐蚀,而铁制品一旦保养不善就容易被腐蚀生锈。铝化学性质非常活泼,在干燥的空气中会立即与氧气发生反应而生成一层致密的氧化铝薄膜,阻碍了铝进一步氧化,同时使铝隔绝了水。因此,铝常被制成铝箔用作薯片、坚果、香烟等在空气中易变质物品的包装。同时,由于铝粉保持了银白色的金属光泽(大多数金属粉末呈现黑色),铝粉常用作涂料(俗称“银粉”)在保护铁制品的同时还使其十分美观。
铝还能在一定条件下与一些化学性质稳定的金属氧化物反应,生成相应的金属单质并释放出大量的热。利用这一性质,人们将铝粉与金属氧化物粉末按一定比例混合制成铝热剂,如:铝粉与三氧化二铁混合制得的铁铝热剂。铝热剂是1893年德国的化学家汉斯·歌德史密斯在寻找不需要碳高温还原的方法制备高纯度金属的过程中发明的。歌德史密斯在研究中发现,铝热剂在反应过程中散发出大量的热,使置换出的金属熔化并能流出,从而实现了金属与熔渣的分离。因此,铝热剂在工业上常用来冶炼铬、锰等高熔点的金属,还用于金属焊接。
根据文章内容,回答下列问题:
(1)金、银的金属活动性比铝
(2)某油漆叫做“银粉漆”,其中的“银粉”指的是
(3)铝热剂在工业上常用于炼铬、锰等金属的原因
(4)铝粉与三氧化二铁混合制得的铁铝热剂反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】北斗系统的全面建成彰显了中国航天的力量,在航天科技中会用到大量金属材料。
(1)电器的电路板中多用铜质导线,这是利用了铜的延展性和______ 。
(2)铝在常温下耐腐蚀的原因是______ (用化学方程式表示)。
(3)为验证镁、锌、铁的金属活动性,下列试剂选择可以达到目的是______(填字母)。
(1)电器的电路板中多用铜质导线,这是利用了铜的延展性和
(2)铝在常温下耐腐蚀的原因是
(3)为验证镁、锌、铁的金属活动性,下列试剂选择可以达到目的是______(填字母)。
| A.镁、铁和硫酸锌溶液 | B.镁、锌和硫酸亚铁溶液 |
| C.硝酸镁溶液、锌和铁 | D.镁、硫酸锌溶液和硫酸亚铁溶液 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】要从X、银、铜、锌四种金属混合物中分离金属,流程如下:
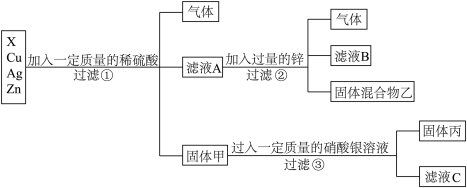
(1)四种金属的活动性顺序由强到弱的是_____ 。
(2)滤液A中所含溶质有_____ 种。
(3)写出③中反应的化学方程式_____ 。
(4)固体丙中所含金属的成分是_____ 。

(1)四种金属的活动性顺序由强到弱的是
(2)滤液A中所含溶质有
(3)写出③中反应的化学方程式
(4)固体丙中所含金属的成分是
您最近一年使用:0次
【推荐2】某化学兴趣小组向一定量氯化铜溶液中加入一定量的铁和锌,充分反应后过滤,得到滤液和滤渣,滤液为无色。
(1)滤液中一定含有什么金属离子?(写化学符号)
(2)请写出一定会发生的化学反应对应的化学方程式。
(1)滤液中一定含有什么金属离子?(写化学符号)
(2)请写出一定会发生的化学反应对应的化学方程式。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】人类的生产生活离不开金属。
(1)中华文明五千年,有着辉煌灿烂的历史。
①古代文献中记载了金、银、铁、锌等金属的冶炼方法,其中不能与稀盐酸反应的金属是________ (填化学式)。
②《神农本草经》中记载“石胆……能化铁为铜”(“石胆”主要成分是硫酸铜),该反应的化学方程式为__________ 。
(2)2022年北京冬奥会发行的冬奥币制作材料之一是铜合金,若用纯铜与其相互刻画,表面出现划痕的是_______________ (填“铜合金”或“纯铜”)。
(3)钢铁器件喷上油漆可隔绝O2和_______ (填化学式),以达到防锈的目的。
(4)为比较R、M、Q三种金属的活动性强弱,将一定质量的R加入到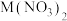 、QNO3的混合溶液中,充分反应后过滤,得到滤液和滤渣,滤渣质量大于R的质量,向滤液中加入足量M,有Q析出,据此
、QNO3的混合溶液中,充分反应后过滤,得到滤液和滤渣,滤渣质量大于R的质量,向滤液中加入足量M,有Q析出,据此______________ (填“能”或“不能”)比较出三种金属的活动性强弱。
(5)已知:①金属活动性顺序X>Y,且均在氢之前;②X、Y在生成物中均为+2价;③相对原子质量X>Y。将等质量的金属X、Y分别放入到等质量且质量分数相同的稀盐酸中充分反应。下列图像可能与实验相符的是 (填字母)。
(1)中华文明五千年,有着辉煌灿烂的历史。
①古代文献中记载了金、银、铁、锌等金属的冶炼方法,其中不能与稀盐酸反应的金属是
②《神农本草经》中记载“石胆……能化铁为铜”(“石胆”主要成分是硫酸铜),该反应的化学方程式为
(2)2022年北京冬奥会发行的冬奥币制作材料之一是铜合金,若用纯铜与其相互刻画,表面出现划痕的是
(3)钢铁器件喷上油漆可隔绝O2和
(4)为比较R、M、Q三种金属的活动性强弱,将一定质量的R加入到
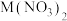 、QNO3的混合溶液中,充分反应后过滤,得到滤液和滤渣,滤渣质量大于R的质量,向滤液中加入足量M,有Q析出,据此
、QNO3的混合溶液中,充分反应后过滤,得到滤液和滤渣,滤渣质量大于R的质量,向滤液中加入足量M,有Q析出,据此(5)已知:①金属活动性顺序X>Y,且均在氢之前;②X、Y在生成物中均为+2价;③相对原子质量X>Y。将等质量的金属X、Y分别放入到等质量且质量分数相同的稀盐酸中充分反应。下列图像可能与实验相符的是 (填字母)。
A.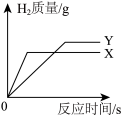 | B. |
C.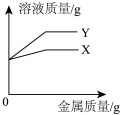 | D.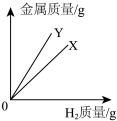 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】材料是人类社会物质文明进步的重要标志,请回答问题。

(1)新型镁锂合金用于制造火星车的车结构,体现了镁锂合金具有密度小、耐腐蚀、______ 的优良性能。
(2)我国高铁飞速发展,已成为世界上唯一高铁成网的国家。
①高铁电路多用铜制导线,这是利用铜的延展性和______ 性。
②制作高铁的材料中使用了铝合金等铝制品,铝在空气中耐腐蚀的原因是______ (用化学反应方程式表示)。
③车体表面烤漆不仅美观,还能起到防锈作用,其防锈的原理是______ 。
(3)中国首款完全自主知识产权民用客机C919飞机的钛合金用量达9.3%。工业上利用钛白粉制备海绵钛的工艺流程如下图:

①反应Ⅱ发生置换反应生成海锦钛,则物质X的化学式为______ 。
②该工艺流程中,可以循环使用的物质有______ 。

(1)新型镁锂合金用于制造火星车的车结构,体现了镁锂合金具有密度小、耐腐蚀、
(2)我国高铁飞速发展,已成为世界上唯一高铁成网的国家。
①高铁电路多用铜制导线,这是利用铜的延展性和
②制作高铁的材料中使用了铝合金等铝制品,铝在空气中耐腐蚀的原因是
③车体表面烤漆不仅美观,还能起到防锈作用,其防锈的原理是
(3)中国首款完全自主知识产权民用客机C919飞机的钛合金用量达9.3%。工业上利用钛白粉制备海绵钛的工艺流程如下图:

①反应Ⅱ发生置换反应生成海锦钛,则物质X的化学式为
②该工艺流程中,可以循环使用的物质有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】金属是一类重要的材料,人类的生活和生产都离不开金属。请依据所学的知识填空。
(1)下列环境中的铁制品最容易生锈的是_______(填字母)。
(2)为了防止铁制品生锈,常在其表面喷漆或镀一层其他金属,其防锈原理是_______ 。
(3)保护金属资源的有效途径除防止金属腐蚀外,还有_______ (写出一条即可)。
(1)下列环境中的铁制品最容易生锈的是_______(填字母)。
| A.有水未擦干的铁锅 | B.涂油漆的栏杆 | C.盛植物油的不锈钢油壶 |
(3)保护金属资源的有效途径除防止金属腐蚀外,还有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】2023年,中国的创新动力、发展活力勃发奔涌,都高不开金属材料的应用:C919大飞机实现商飞,国产大型邮轮完成试航,神舟家族太空接力,“奋斗者”号极限深潜。
(1)C919大飞机的机身主体材料是铝合金,使用铝合金的优点主要体现在其______ 大于纯铝;铝有很好抗腐蚀性原因是______ 。
(2)金属矿物资源的储量有限,而且不能再生,我们需要保护金属资源。下列关于铁制品的防锈措施合理的是 (填字母)。
(1)C919大飞机的机身主体材料是铝合金,使用铝合金的优点主要体现在其
(2)金属矿物资源的储量有限,而且不能再生,我们需要保护金属资源。下列关于铁制品的防锈措施合理的是 (填字母)。
| A.经常用水冲洗自行车链条 |
| B.在铁制栏杆表面刷油漆 |
| C.用不锈钢等合金代替铁制部件 |
| D.对铁制零件进行“烤蓝”处理 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】硫酸和盐酸是实验室常用的试剂,也是重要的化工原料。
(1)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是盛有______________ 的试剂瓶。
(2)从微观角度看,硫酸和盐酸具有相似化学性质的原因是_______________________ 。
(3)在盛有少量氧化铜粉末的试管中加入足量稀硫酸,观察到的实验现象是_________ ,反应的化学方程式为_________________________ 。
(4)写出把硫酸转化为盐酸的化学方程式________________________ 。
(5)某工厂利用废铁屑与废硫酸反应来制取硫酸亚铁。现有废硫酸 49t(H2SO4的质量分数为10%),与足量废铁屑起反应,可生产硫酸亚铁的质量是______________ t。
(1)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是盛有
(2)从微观角度看,硫酸和盐酸具有相似化学性质的原因是
(3)在盛有少量氧化铜粉末的试管中加入足量稀硫酸,观察到的实验现象是
(4)写出把硫酸转化为盐酸的化学方程式
(5)某工厂利用废铁屑与废硫酸反应来制取硫酸亚铁。现有废硫酸 49t(H2SO4的质量分数为10%),与足量废铁屑起反应,可生产硫酸亚铁的质量是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】我们处在一个色彩斑斓的物质世界中。化学社团针对物质开展“颜之有物”的探究。
Ⅰ.物质有自己独特颜色
(1)下列物质与水能形成有色溶液的是________。
(2)氯化铁溶液呈黄色。为探究是哪种粒子使溶液呈黄色,同学们设计了如图所示的对比实验,可选择用作对比的试剂是________ 溶液。
(3)向某溶液中滴加紫色石蕊试剂,溶液变红色,说明该溶液pH________ 7(填“>”、“=”或“<”)。
Ⅲ.颜色变化可作为化学反应发生的一种证据
(4)有些化学反应中伴随着颜色的变化。如实验室模拟炼铁,高温下CO还原氧化铁,观察到固体的颜色变化是________ 。
(5)自然界中无明显现象的反应远多于有明显现象的反应,比如稀盐酸和氢氧化钠反应。为验证该反应的发生,设计了如图所示的实验:________ (现象),即可证明两者发生了化学反应。请写出该反应的化学方程式________ 。
(6)颜料可从植物中获取。唐代流行服饰石榴裙因其颜色类似石榴花的红色而得名。古法染色工艺记载:“取石榴之花,入臼细杵之,得厚汁,以之染布,不可加热,可为石榴裙也”。请写出在此染布过程中需要注意的事项________________ (一条即可)。
(7)为测定某生锈铁钉中未生锈的铁的质量,取50g该铁钉放入溶质质量分数为7.3%的稀盐酸中,当表面的铁锈完全除去时恰好消耗300g稀盐酸溶液。请计算该铁钉中未生锈的铁的质量。
Ⅰ.物质有自己独特颜色
(1)下列物质与水能形成有色溶液的是________。
| A.酒精 | B.硫酸铜 | C.牛奶 | D.碳酸钙 |
(2)氯化铁溶液呈黄色。为探究是哪种粒子使溶液呈黄色,同学们设计了如图所示的对比实验,可选择用作对比的试剂是

(3)向某溶液中滴加紫色石蕊试剂,溶液变红色,说明该溶液pH
Ⅲ.颜色变化可作为化学反应发生的一种证据
(4)有些化学反应中伴随着颜色的变化。如实验室模拟炼铁,高温下CO还原氧化铁,观察到固体的颜色变化是
(5)自然界中无明显现象的反应远多于有明显现象的反应,比如稀盐酸和氢氧化钠反应。为验证该反应的发生,设计了如图所示的实验:
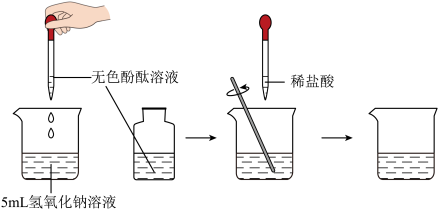
(6)颜料可从植物中获取。唐代流行服饰石榴裙因其颜色类似石榴花的红色而得名。古法染色工艺记载:“取石榴之花,入臼细杵之,得厚汁,以之染布,不可加热,可为石榴裙也”。请写出在此染布过程中需要注意的事项
(7)为测定某生锈铁钉中未生锈的铁的质量,取50g该铁钉放入溶质质量分数为7.3%的稀盐酸中,当表面的铁锈完全除去时恰好消耗300g稀盐酸溶液。请计算该铁钉中未生锈的铁的质量。
您最近一年使用:0次





