将含杂质的铁粉分成质量相等的A、B两份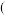 杂质不溶于水且不参与任何置换反应
杂质不溶于水且不参与任何置换反应 。在A中加入足量的稀硫酸,充分反应后得到不溶物
。在A中加入足量的稀硫酸,充分反应后得到不溶物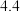 克。在B中加入足量硫酸铜,充分反应后得到固体
克。在B中加入足量硫酸铜,充分反应后得到固体 克,求混和物中铁的质量分数。
克,求混和物中铁的质量分数。
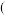 杂质不溶于水且不参与任何置换反应
杂质不溶于水且不参与任何置换反应 。在A中加入足量的稀硫酸,充分反应后得到不溶物
。在A中加入足量的稀硫酸,充分反应后得到不溶物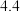 克。在B中加入足量硫酸铜,充分反应后得到固体
克。在B中加入足量硫酸铜,充分反应后得到固体 克,求混和物中铁的质量分数。
克,求混和物中铁的质量分数。
更新时间:2019-03-08 10:13:44
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】化学实验小组同学为研究某公共场所铁制护栏锈蚀的程度,将 6.4g 已生锈的铁片,放入一浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如下图 所示(假设铁片除有 Fe2O3 外,不含其他杂质)。
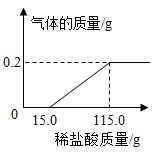
(1)生成氢气的质量为_____g。
(2)求稀盐酸中溶质的质量分数_______?求该铁片中 Fe2O3 的质量分数为多少_________?(写出计算过程,结果精确到到0.1%)

(1)生成氢气的质量为_____g。
(2)求稀盐酸中溶质的质量分数_______?求该铁片中 Fe2O3 的质量分数为多少_________?(写出计算过程,结果精确到到0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】某化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与稀盐酸反应)中碳酸钙的质量分数,进行如图所示的实验。根据以上信息计算:(方程式为: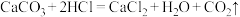 )
)

(1)生成二氧化碳的质量为__________ g;
(2)样品中碳酸钙的质量分数是多少?(写出计算过程)
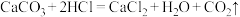 )
)
(1)生成二氧化碳的质量为
(2)样品中碳酸钙的质量分数是多少?(写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】为测定实验室某瓶盐酸的溶质质量分数是否与标签相符,小华做了如下实验:将该盐酸滴加到大理石中至恰好反应不再产生气泡(其中杂质不参与反应,也不溶于水),数据记录如下表。
(1)通过计算,判断测定结果与试剂瓶标签上溶质的质量分数是否相符。(计算结果精确到0.1%)
(2)恰好完全反应后所得溶液的溶质质量分数?

| 反应前物质的质量 | 充分反应后物质的质量 | |
| 盐酸样品 | 大理石 | 剩余固体+液体 |
| 53.0g | 6.0g | 56.8g |
(1)通过计算,判断测定结果与试剂瓶标签上溶质的质量分数是否相符。(计算结果精确到0.1%)
(2)恰好完全反应后所得溶液的溶质质量分数?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】实验室有一份在空气中潮解变质的氢氧化钠样品,质量为1.5g。某实验小组将这份样品完全溶解,配成50g溶液。然后缓慢滴入7.3%的稀盐酸,同时进行搅拌,使二氧化碳全部逸出。滴加过程中,多次测得溶液pH和溶液总质量,部分数据如下表所示:
请分析计算:
(1)第 次测量时,溶液中只有一种溶质。
(2)表中m= 。
(3)样品中碳酸钠的质量分数。(计算结果精确到0.1%)
(4)1.5g样品中氢氧化钠固体的质量。
| 测量次数 | 第1次 | 第6次 | 第16次 | 第21次 | 第26次 |
| 滴加的盐酸总质量/g | 0 | 5 | 15 | 20 | 25 |
| 溶液总质量/g | 50 | 55 | m | 69.78 | 74.78 |
| 溶液pH | 12.4 | 12.1 | 7.0 | 2.2 | 2.1 |
请分析计算:
(1)第 次测量时,溶液中只有一种溶质。
(2)表中m= 。
(3)样品中碳酸钠的质量分数。(计算结果精确到0.1%)
(4)1.5g样品中氢氧化钠固体的质量。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】为探究酸式盐的化学性质,小开将 Ba(HCO3)2溶液慢慢加入 240 g 质量分数为10%的 NaHSO4溶液中,恰好不再有气泡产生时(假设生成的气体全部逸出),所加 Ba(HCO)2溶液的质量为 502.1 g。反应原理为:2NaHSO4+Ba(HCO3)2=Na2SO4+2CO2↑+2H2O+BaSO4↓试计算:
(1)现用质量分数为 25%的NaHSO4溶液配制实验所用的NaHSO4溶液,需加入水的质量为______ g。
(2)最后所得溶液中Na2SO4的质量分数。
(1)现用质量分数为 25%的NaHSO4溶液配制实验所用的NaHSO4溶液,需加入水的质量为
(2)最后所得溶液中Na2SO4的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】为测定某纯碱(Na2CO3)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出)。产生气体的质量与滴入稀盐酸的质量关系如图所示,
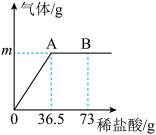
(1)A点产生气体的质量m为_______, 此时所得溶液的溶质质量为 ______。
(2)B点时,烧杯内溶液中粒子有__________________________。(写粒子符号)

(1)A点产生气体的质量m为_______, 此时所得溶液的溶质质量为 ______。
(2)B点时,烧杯内溶液中粒子有__________________________。(写粒子符号)
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐2】某化学兴趣小组对胃药“碳酸氢钠片”进行了探究,具体做法如下:
Ⅰ.取1片胃药研碎,加水完全溶解得到100g溶液;
Ⅱ.配制100g 0.365%的稀盐酸作为模拟胃酸;
Ⅲ.取上述一种溶液20g于锥形瓶中,再将另一种溶液逐滴加入锥形瓶内,反应后溶液的pH变化情况如图所示.
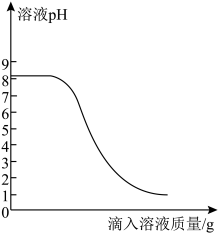
请回答下列问题:
(1)碳酸氢钠属于______(填“酸”“碱”或“盐”);
(2)步骤Ⅲ中,当滴入另一种溶液的质量为10g时,锥形瓶内物质恰好完全反应(胃药中其它成分不参加反应),请根据实验数据计算每片胃药中碳酸氢钠的质量,写出必要的计算过程__________________。
Ⅰ.取1片胃药研碎,加水完全溶解得到100g溶液;
Ⅱ.配制100g 0.365%的稀盐酸作为模拟胃酸;
Ⅲ.取上述一种溶液20g于锥形瓶中,再将另一种溶液逐滴加入锥形瓶内,反应后溶液的pH变化情况如图所示.

请回答下列问题:
(1)碳酸氢钠属于______(填“酸”“碱”或“盐”);
(2)步骤Ⅲ中,当滴入另一种溶液的质量为10g时,锥形瓶内物质恰好完全反应(胃药中其它成分不参加反应),请根据实验数据计算每片胃药中碳酸氢钠的质量,写出必要的计算过程__________________。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】黄铜是铜锌合金。取10g黄铜于烧杯中,将120g稀硫酸分六次加入烧杯中,测得加入的稀硫酸质量和烧杯中剩余物的质量如下表:
(1)该合金属于___________ 。(填物质类别)
(2)表中m=___________ 。
(3)所用稀硫酸的溶质质量分数(请根据化学方程式写出规范的计算步骤)
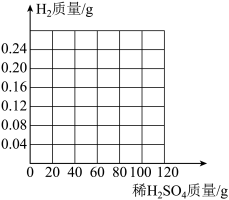
(4)请在下图画出:往10g黄铜加入稀硫酸,生成氢气质量的图像。
| 次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 |
| 加入硫酸的质量/g | 20 | 20 | 20 | 20 | 20 | 20 |
| 剩余物的质量/g | 129.96 | 149.92 | m | 189.84 | 209.80 | 229.80 |
(2)表中m=
(3)所用稀硫酸的溶质质量分数(请根据化学方程式写出规范的计算步骤)
(4)请在下图画出:往10g黄铜加入稀硫酸,生成氢气质量的图像。

您最近一年使用:0次



