试选用“>”或“<”或“=”填空,
(1)酸雨的pH________ 蒸馏水的pH;
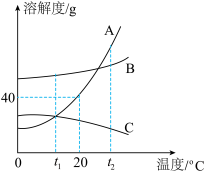
(2)20℃时氢氧化钙的溶解度_________ 40℃时氢氧化钙的溶解度;
(3)镁的金属活动性_________ 铝的金属活动性;
(4)一般情况下,合金的硬度________ 其成分金属的硬度;
(5)将5碳酸钠粉末加到95g溶质质量分数为10%的盐酸中,充分混合后液的质量_______ 100g;
(6)相同的两段细铁丝:用蒸馏水浸过的铁丝生锈的速率_______ 用食盐水浸过的铁丝生锈的速率。
(1)酸雨的pH
(2)20℃时氢氧化钙的溶解度
(3)镁的金属活动性
(4)一般情况下,合金的硬度
(5)将5碳酸钠粉末加到95g溶质质量分数为10%的盐酸中,充分混合后液的质量
(6)相同的两段细铁丝:用蒸馏水浸过的铁丝生锈的速率
更新时间:2020-02-03 14:15:58
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】下列是初中化学中的一些重要实验,请回答下列问题:
A.细铁丝在氧气中燃烧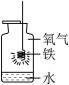
B.倾倒二氧化碳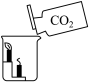
C.反应前后质量的测定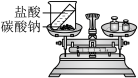
D.
(1)A中集气瓶底留有少量水的原因是:______ 。
(2)B实验得出的结论是:______ 。
(3)C中反应后天平______ (填“平衡”或“不平衡”)请你从原子的角度说明该反应遵守质量守恒定律的原因______ 。
(4)铁生锈的条件______ ,D中铁钉最易生锈的部位是______ (填“a”“b”或“c”)。
A.细铁丝在氧气中燃烧

B.倾倒二氧化碳

C.反应前后质量的测定

D.

(1)A中集气瓶底留有少量水的原因是:
(2)B实验得出的结论是:
(3)C中反应后天平
(4)铁生锈的条件
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】中国的高铁也已经成为国家名片,请用所学化学知识回答以下小题。
(1)高铁车身喷漆不仅为了美观,更是为了防锈,铁生锈原理是铁与空气中的___________ 反应(填化学式)。
(2)制造铁轨的锰钢是一种铁合金,现将某铁合金(只含铁和碳)8.7g放入盛有100g稀盐酸的烧杯中,恰好完全反应,得到108.1g溶液,则该样品中碳的质量分数为3.4%。该铁合金属于___________ (填“钢”或“生铁”)。
(3)早在春秋战国时期,我国就开始生产和使用铁器。炼铁原理是利用一氧化碳与氧化铁在高温条件下反应,该反应的化学方程式为___________ 。
(4)向AgNO3和Mg(NO3)2溶液中加入一定量Fe粉和Cu粉,充分反应后过滤,往滤渣加酸无气泡。滤渣中一定有___________ (填化学式,下同);滤液中一定有溶质___________ 。
(1)高铁车身喷漆不仅为了美观,更是为了防锈,铁生锈原理是铁与空气中的
(2)制造铁轨的锰钢是一种铁合金,现将某铁合金(只含铁和碳)8.7g放入盛有100g稀盐酸的烧杯中,恰好完全反应,得到108.1g溶液,则该样品中碳的质量分数为3.4%。该铁合金属于
(3)早在春秋战国时期,我国就开始生产和使用铁器。炼铁原理是利用一氧化碳与氧化铁在高温条件下反应,该反应的化学方程式为
(4)向AgNO3和Mg(NO3)2溶液中加入一定量Fe粉和Cu粉,充分反应后过滤,往滤渣加酸无气泡。滤渣中一定有
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐3】李娜同学在探究铁生锈的条件时,将铁钉浸没在试管里的食盐水中,一段时间后,发现试管底部出现了黑色粉末。李娜同学对此黑色粉末的组成做了如下几种猜测:①Fe;②Fe2O3;③Fe3O4;④数种物质的混合物。
请回答下列问题:
(1)你认为李娜同学的上述猜测中,不做实验就可以排除的是___ (填序号),理由是_____ ,你认为黑色粉末还可能是_____ ,理由是_______ 。
(2)设计一个实验方案,用化学方法验证黑色粉末是否为Fe粉:_____ 。
(3)李娜同学将黑色粉末干燥后,用磁铁靠近,发现粉末能被磁铁吸引,于是得出结论:黑色粉末一定是Fe粉,你认为李娜同学的结论对吗?_______ ,理由是________ 。
(4)请你根据不同原理,提出防止钢铁锈蚀的两条合理措施:①_____ ,②______ 。
请回答下列问题:
(1)你认为李娜同学的上述猜测中,不做实验就可以排除的是
(2)设计一个实验方案,用化学方法验证黑色粉末是否为Fe粉:
(3)李娜同学将黑色粉末干燥后,用磁铁靠近,发现粉末能被磁铁吸引,于是得出结论:黑色粉末一定是Fe粉,你认为李娜同学的结论对吗?
(4)请你根据不同原理,提出防止钢铁锈蚀的两条合理措施:①
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】下图为A、B、C三种固体物质的溶解度曲线图,根据曲线图回答下列问题。
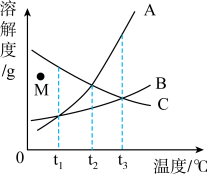
(1)t1℃时,溶解度最大的物质是_________ ;
(2)若t2℃时A的溶解度为50g,则该温度下A的饱和溶液中溶质和溶剂的质量之比是_______ ;
(3)若将M点处C的不饱和溶液变成饱和溶液,可以选择的方法______ (填序号);
①降低温度 ②增加溶质 ③蒸发溶剂
(4)t2℃时,将等质量的A,B,C的饱和溶液都升温到t3℃,此时溶液中溶剂质量最大的是_________ (忽略水的挥发)。

(1)t1℃时,溶解度最大的物质是
(2)若t2℃时A的溶解度为50g,则该温度下A的饱和溶液中溶质和溶剂的质量之比是
(3)若将M点处C的不饱和溶液变成饱和溶液,可以选择的方法
①降低温度 ②增加溶质 ③蒸发溶剂
(4)t2℃时,将等质量的A,B,C的饱和溶液都升温到t3℃,此时溶液中溶剂质量最大的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】结合下表给出的NaCl、KNO3两种固体物质的溶解度,回答有关问题。
(1)70℃时,NaCl的溶解度范围是______ g;
(2)20℃时,KNO3的溶解度约为31.6g,则在该温度下,将15.8gKNO3溶解在40g水中,若将其变成该温度下的饱和溶液,至少需要再加入H2O______ g;
(3)将100gKNO3和37 g NaCl的混合物放入100g60℃的水中,充分搅拌,再降温到20℃,有大量晶体析出,有同学说无法判断溶液析出晶体情况原因是缺少______ 和________ 的溶解度数据。
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
(2)20℃时,KNO3的溶解度约为31.6g,则在该温度下,将15.8gKNO3溶解在40g水中,若将其变成该温度下的饱和溶液,至少需要再加入H2O
(3)将100gKNO3和37 g NaCl的混合物放入100g60℃的水中,充分搅拌,再降温到20℃,有大量晶体析出,有同学说无法判断溶液析出晶体情况原因是缺少
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】实验是科学探究的重要方法。请根据下列装置图,回答问题。
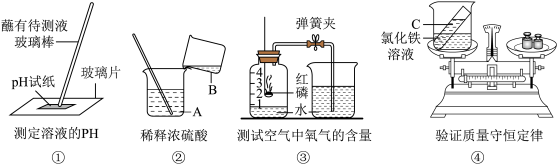
(1)现要测定某酸性溶液的 pH 如图①,若先将玻璃棒润湿,会导致测定值与实际值比较_____ (填“偏大’·或“偏小”或“无法确定”)。
(2)利用图②装置稀释浓硫酸时,为确保实验安全,倾倒的B为_____ (填“浓硫酸”或“水”)。
(3)利用图③装置测得空气中氧气的体积分数小于 21%,可能的原因是_____ (任写一条 )。
(4)利用图④装置验证质量守恒定律时,烧杯内盛有氯化铁溶液,为达到实验 目的,试管中可放入一种与氯化铁溶液反应的 C物质,请写出发生反应的化学方程式_____ (只写一个)。

(1)现要测定某酸性溶液的 pH 如图①,若先将玻璃棒润湿,会导致测定值与实际值比较
(2)利用图②装置稀释浓硫酸时,为确保实验安全,倾倒的B为
(3)利用图③装置测得空气中氧气的体积分数小于 21%,可能的原因是
(4)利用图④装置验证质量守恒定律时,烧杯内盛有氯化铁溶液,为达到实验 目的,试管中可放入一种与氯化铁溶液反应的 C物质,请写出发生反应的化学方程式
您最近一年使用:0次
【推荐2】水是人类生命活动离不开的物质,生命的活动离不开水
(1)自来水厂在净化过程中使用活性炭是利用它的________ 性。
(2)酸碱度过大或硬度过大的水都不宜饮用,实验室可用_____ 测定水的酸碱度;生活中可通过________ 降低水的硬度。
(3)A、B、C三种物质的溶解度曲线如图所示,根据如图给的信息回答问题
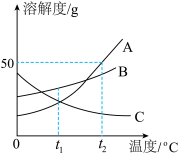
①在t2℃时,A、B、C三种饱和溶液,降温到t1℃时仍然是饱和溶液的是________ ;
②若A中混有少量B ,分离的方法是________ 。
③在t2℃时,30gA溶解在50g水中所得溶液的质量分数为________ (精确到0.1%)。
(1)自来水厂在净化过程中使用活性炭是利用它的
(2)酸碱度过大或硬度过大的水都不宜饮用,实验室可用
(3)A、B、C三种物质的溶解度曲线如图所示,根据如图给的信息回答问题

①在t2℃时,A、B、C三种饱和溶液,降温到t1℃时仍然是饱和溶液的是
②若A中混有少量B ,分离的方法是
③在t2℃时,30gA溶解在50g水中所得溶液的质量分数为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】分类、类比是学习化学的常用方法。
(1)上述化学实验中都用到了玻璃棒,根据实验中所用玻璃棒的作用将C组与_______ 组(填“A或B”)归为一类,理由是_______ ;
(2)“酸酐”是指某含氧元素的酸脱去一分子或几分子水所得到的化合物,如硫酸的酸酐是三氧化硫。据此,我们可以推测硅酸(H2SiO3)的酸酐是_______ (填化学式),请写出该酸酐与氢氧化钠溶液混合时发生反应的化学方程式_______ 。
| A组 | B组 | C组 | ||
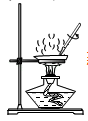 | 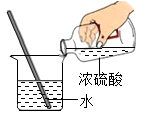 | 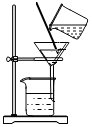 | 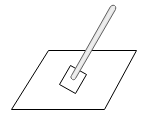 | 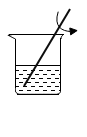 |
| 蒸发 | 浓硫酸稀释 | 过滤 | 测定溶液的 pH | 物质的溶解 |
(2)“酸酐”是指某含氧元素的酸脱去一分子或几分子水所得到的化合物,如硫酸的酸酐是三氧化硫。据此,我们可以推测硅酸(H2SiO3)的酸酐是
您最近一年使用:0次