解题方法
1 . 现有A~F六种物质的稀溶液,分别是硫酸钠溶液、氢氧化钠溶液、氢氧化钡溶液、稀盐酸、氯化钠溶液、酚酞溶液中的一种,把他们两两混合,其部分现象如下表所示。(已知:硫酸钠溶液显中性)
(1)B溶液中溶质的化学式______ ,E为______ 溶液。
(2)A与C混合发生反应的化学方程式为______ 。
(3)对还没有确定的稀溶液,下列鉴别方法中正确的是______(填字母序号)。
(4)相同质量、相同溶质质量分数的氢氧化钠溶液与盐酸相混合后,滴加紫色石蕊溶液,溶液呈______ 色。
| B | C | D | E | |
| A | 无明显变化 | 白色沉淀 | 无明显变化 | 液体变红色 |
| B | …… | 无明显变化 | 无明显变化 | 液体变红色 |
(2)A与C混合发生反应的化学方程式为
(3)对还没有确定的稀溶液,下列鉴别方法中正确的是______(填字母序号)。
A.分别滴加 溶液,观察现象 溶液,观察现象 | B.分别滴加 溶液,观察现象 溶液,观察现象 |
您最近一年使用:0次
2024·江西·一模
解题方法
2 . 某小组以“探究气体制取和气体性质”为主题展开可视化的项目式学习。
(1)如图所示为实验室中常见的气体制备和收集装置。请回答下列问题:

①实验室用A装置制取氧气,反应的化学方程式为_______ 。
②若用装置E收集二氧化碳,检验其是否收集满的方法是_______ ,用装置C制氢气,此装置相比B装置其突出优点是_______ 。
(2)某研究小组同学对超市里的污渍爆炸盐产生了兴趣,污渍爆炸盐溶于水,有许多气泡产生。
【提出问题】污渍爆炸盐(如图)溶于水,产生气体的成分是什么?

【形成假设】
①该气体可能是CO2、O2、H2、N2。
②根据爆炸盐的有效成分推测,该气体中不可能含有N2,因为_______ 。
③从使用安全角度考虑,该气体中应该不含有H2,因为_______ 。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【实施实验】
【形成结论】
④由实验Ⅰ可知,该气体中肯定含有_______ 。
(3)化学课堂上老师演示了如图所示的几个实验:
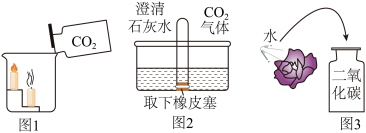
①图1中下层蜡烛先熄灭,上层蜡烛后熄灭,据此说明二氧化碳的物理性质为_______ 。
②图2所示实验中,应观察到的实验现象是_______ (填字母)。
a.试管内液面上升 b.试管内液体变红 c.试管内液体变浑浊
③图3所示实验中,使紫色干花(用石蕊溶液浸泡过)变红的原因是_______ 。
(1)如图所示为实验室中常见的气体制备和收集装置。请回答下列问题:

①实验室用A装置制取氧气,反应的化学方程式为
②若用装置E收集二氧化碳,检验其是否收集满的方法是
(2)某研究小组同学对超市里的污渍爆炸盐产生了兴趣,污渍爆炸盐溶于水,有许多气泡产生。
【提出问题】污渍爆炸盐(如图)溶于水,产生气体的成分是什么?

【形成假设】
①该气体可能是CO2、O2、H2、N2。
②根据爆炸盐的有效成分推测,该气体中不可能含有N2,因为
③从使用安全角度考虑,该气体中应该不含有H2,因为
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【实施实验】
| 实验编号 | 实验操作 | 实验现象 |
| I | 将该气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| Ⅱ | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
④由实验Ⅰ可知,该气体中肯定含有
(3)化学课堂上老师演示了如图所示的几个实验:

①图1中下层蜡烛先熄灭,上层蜡烛后熄灭,据此说明二氧化碳的物理性质为
②图2所示实验中,应观察到的实验现象是
a.试管内液面上升 b.试管内液体变红 c.试管内液体变浑浊
③图3所示实验中,使紫色干花(用石蕊溶液浸泡过)变红的原因是
您最近一年使用:0次
解题方法
3 . 化学小组同学在实验室里用下列实验仪器或装置进行实验,请你一起回答下列问题。

(1)甲图中仪器⑦的名称为_______ 。
(2)实验室制取并收集一瓶二氧化碳,需要用到甲图的仪器有______ (填序号),该反应的化学方程式为_______ 。
(3)若用氯酸钾和二氧化锰反应,通过以上仪器制取并收集一瓶纯净的氧气,用于铁丝燃烧实验,需要补充的仪器为30度玻璃弯管、单孔塞、橡胶管和_______ 。
(4)若收集的二氧化碳要干燥,则将气体从_______ (选填“左”或“右”)导管通入装有浓硫酸的乙图装置。

(1)甲图中仪器⑦的名称为
(2)实验室制取并收集一瓶二氧化碳,需要用到甲图的仪器有
(3)若用氯酸钾和二氧化锰反应,通过以上仪器制取并收集一瓶纯净的氧气,用于铁丝燃烧实验,需要补充的仪器为30度玻璃弯管、单孔塞、橡胶管和
(4)若收集的二氧化碳要干燥,则将气体从
您最近一年使用:0次
解题方法
4 . 下面是我们在初中化学课本经历的实验:请回答下列问题:

(1)A实验中集气瓶内水的作用是______ 。
(2)B实验中玻璃管上气球的作用是______ 。
(3)D中木炭还原氧化铜的化学方程式为______ 。

(1)A实验中集气瓶内水的作用是
(2)B实验中玻璃管上气球的作用是
(3)D中木炭还原氧化铜的化学方程式为
您最近一年使用:0次
5 . 有一种工业废水,其中含有大量的硫酸亚铁,少量的银离子以及污泥。某同学设计了一个既经济又合理的方法回收银和硫酸亚铁晶体。方案流程如下,回答下列问题:
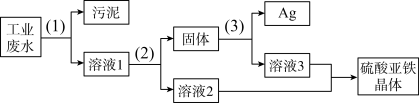
(1)步骤(2)中,分离混合物的方法是_____ ,需加入的物质是_____ (填化学式)。
(2)步骤(2)后,得到的固体物质不是纯银,含的杂质是_____ ,(填化学式)。
(3)溶液2和溶液3是什么物质_____ 。(填化学式)
(4)写出(3)发生的化学方程式_____ 。

(1)步骤(2)中,分离混合物的方法是
(2)步骤(2)后,得到的固体物质不是纯银,含的杂质是
(3)溶液2和溶液3是什么物质
(4)写出(3)发生的化学方程式
您最近一年使用:0次
6 . 金属材料发展突飞猛进,其对人类生产、生活和社会发展有着极其重要作用。人类制得并利用金属历史悠久,研究金属发展过程为:存在形式→冶炼方法→性质应用。
【冶炼方法】
(1)《淮南万毕术》中有“曾青得铁则化为铜”的记载,意思是铁在硫酸铜溶液中能反应,其化学方程式为_______ ,基本反应类型是_______ 。
(2)如图为工业炼铁高炉结构图和实验室模拟工业炼铁的部分仪器与装置。


①工业炼铁时所需原料有铁矿石、_______ 、石灰石、热空气。
②实验产生的尾气不能直接排放,你选择的处理装置是_______ 。
③模拟炼铁时,A装置a口需要与B装置的_______ (填字母)口相连接,模拟炼铁的化学反应方程式为_______ 。
【性质用途】
(3)用铁制锅铲需要加上木柄或塑料柄,这是因为铁具有______ 。
【冶炼方法】
(1)《淮南万毕术》中有“曾青得铁则化为铜”的记载,意思是铁在硫酸铜溶液中能反应,其化学方程式为
(2)如图为工业炼铁高炉结构图和实验室模拟工业炼铁的部分仪器与装置。


①工业炼铁时所需原料有铁矿石、
②实验产生的尾气不能直接排放,你选择的处理装置是
③模拟炼铁时,A装置a口需要与B装置的
【性质用途】
(3)用铁制锅铲需要加上木柄或塑料柄,这是因为铁具有
您最近一年使用:0次
解题方法
7 . 电解水制氢联合碳酸钙分解制备氧化钙的新方法的示意图如下图1所示。

(1)传统方法:CaCO3在高温时分解生成CaO,同时还会生成一种常见的温室气体是______ 。
(2)新方法:
①反应器1:一定条件下,CaCO3可与H2反应生成CaO、CO和H2O,该反应的化学方程式为___ 。
②CaCO3还可以直接分解。反应器1中CO、CO2的含量随反应温度的变化如图2所示,抑制CO2生成的效果最好的最佳温度是_______ ℃。
③反应器2:一定条件下,CO与H发生化合反应生成甲醇(CH3OH),CO与H2的分子个数比为_____ 。
(3)与传统方法相比,新方法的优点有_______ 。

(1)传统方法:CaCO3在高温时分解生成CaO,同时还会生成一种常见的温室气体是
(2)新方法:
①反应器1:一定条件下,CaCO3可与H2反应生成CaO、CO和H2O,该反应的化学方程式为
②CaCO3还可以直接分解。反应器1中CO、CO2的含量随反应温度的变化如图2所示,抑制CO2生成的效果最好的最佳温度是
③反应器2:一定条件下,CO与H发生化合反应生成甲醇(CH3OH),CO与H2的分子个数比为
(3)与传统方法相比,新方法的优点有
您最近一年使用:0次
解题方法
8 . Na2O2具有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测Na2O2与H2能发生反应。为了验证此推测结果,该同学设计并进行如图实验。
实验探究:

步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K1、K2,在产生的氢气流经装有Na2O2的硬质玻璃管的过程中,未观察到明显现象。
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色。
已知:常温下Na2O2为淡黄色粉末状固体,Na2O2与HCl、CO2、H2O均会发生反应,Na2O2需密封保存。
(1)写出A装置中发生的反应的离子方程式_______ 。
(2)B装置中所盛放的试剂是_______ ,其作用是_______ 。
(3)步骤3中的必要操作为打开K1、K2,_______ (请按正确的顺序填入下列步骤的字母)。
A. 加热至Na2O2逐渐熔化,反应一段时间
B. 用小试管收集气体并检验其纯度
C. 关闭K1
D. 停止加热,充分冷却
(4)由上述实验可推出Na2O2与H2反应的化学方程式为_______ 。
(5)实验证明将Na2O2粉末投入滴有酚酞的水中,水溶液有出现变红的现象,同时产生了能使带火星的木条复燃的气体,那么将Na2O2投入到FeCl3溶液中,有关现象说法正确的是_______ 。
(6)向酸性KMnO4溶液中加入Na2O2粉末。观察到溶液褪色,发生如下反应:
_______MnO +_______Na2O2+_______=_______Mn2++_______Na++_______+_______
+_______Na2O2+_______=_______Mn2++_______Na++_______+_______
补全方程式并配平_______ 。
实验探究:

步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K1、K2,在产生的氢气流经装有Na2O2的硬质玻璃管的过程中,未观察到明显现象。
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色。
已知:常温下Na2O2为淡黄色粉末状固体,Na2O2与HCl、CO2、H2O均会发生反应,Na2O2需密封保存。
(1)写出A装置中发生的反应的离子方程式
(2)B装置中所盛放的试剂是
(3)步骤3中的必要操作为打开K1、K2,
A. 加热至Na2O2逐渐熔化,反应一段时间
B. 用小试管收集气体并检验其纯度
C. 关闭K1
D. 停止加热,充分冷却
(4)由上述实验可推出Na2O2与H2反应的化学方程式为
(5)实验证明将Na2O2粉末投入滴有酚酞的水中,水溶液有出现变红的现象,同时产生了能使带火星的木条复燃的气体,那么将Na2O2投入到FeCl3溶液中,有关现象说法正确的是
| A.生成红褐色沉淀 | B.没有气体产生 |
| C.生成白色沉淀 | D.有无色气体产生 |
(6)向酸性KMnO4溶液中加入Na2O2粉末。观察到溶液褪色,发生如下反应:
_______MnO
 +_______Na2O2+_______=_______Mn2++_______Na++_______+_______
+_______Na2O2+_______=_______Mn2++_______Na++_______+_______补全方程式并配平
您最近一年使用:0次
解题方法
9 . 为了研究水的组成,某学习小组制作了如图所示的简易电解水装置,并进行了实验(注:该装置气密性良好,且反应一段时间后停止通电,A、B管内液面均高于图中D线)。请根据要求回答问题:

闭合开关后观察。
(1)反应后,A、B管内的液面更接近于D线的是___________ (选填“A”或“B”)管。
(2)该反应的化学方程式为___________ 。
(3)若检验A管内生成的气体应该用___________ ,用点燃的方法检验B管气体,所产生的现象是___________ 。

闭合开关后观察。
(1)反应后,A、B管内的液面更接近于D线的是
(2)该反应的化学方程式为
(3)若检验A管内生成的气体应该用
您最近一年使用:0次
23-24九年级上·全国·假期作业
10 . 铁及其化合物在生产生活中应用广泛,化学学习小组的同学以“铁的锈蚀与防护以及铁的冶炼”为主题开展项目式学习。
小组同学设计了图1所示装置进行铁钉生锈的有关实验。

(1)一段时间后,C、D中的铁钉生锈,A、B中的铁钉无明显锈蚀,由A、B、C的现象可知,铁的锈蚀是铁跟______ (填化学式)等物质作用的过程。D中铁钉比C中铁钉锈蚀程度严重,说明______ 。
(2)为防止铁生锈,可对铁制品进行“发蓝”处理,使其表面生成致密的氧化物(其中Fe、O元素质量比为21:8)保护膜,该氧化物的化学式为______ 。
小组同学设计了图1所示装置进行铁钉生锈的有关实验。

(1)一段时间后,C、D中的铁钉生锈,A、B中的铁钉无明显锈蚀,由A、B、C的现象可知,铁的锈蚀是铁跟
(2)为防止铁生锈,可对铁制品进行“发蓝”处理,使其表面生成致密的氧化物(其中Fe、O元素质量比为21:8)保护膜,该氧化物的化学式为
您最近一年使用:0次



