1 . 读图回答问题:
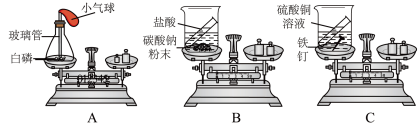
(1)如图,A、B、C三个实验用于验证质量守恒定律,其中不能达到目的的实验是______ ;
(2)图A中白磷燃烧的现象是______ 、放出热量,该反应的化学方程式为______ ;燃烧后恢复至室温时测量,若发现天平指针偏右,则造成的原因可能是______ ;
(3)图C中反应的化学方程式为______ ;
(4)由上述实验可知,在化学反应前后,一定不变的是______ (填数字序号)。
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤物质总质量

(1)如图,A、B、C三个实验用于验证质量守恒定律,其中不能达到目的的实验是
(2)图A中白磷燃烧的现象是
(3)图C中反应的化学方程式为
(4)由上述实验可知,在化学反应前后,一定不变的是
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤物质总质量
您最近一年使用:0次
解题方法
2 . 质量守恒定律的发现,对科学的发展作出了重要贡献。
(1)为了验证质量守恒定律,实验小组分别选取以下三组药品,通过称量比较各组物质在密闭容器内混合前后的总质量,不能达到目的的有______。
(2)在一定条件下,甲和乙反应生成丙,微粒变化如图所示( 、
、 表示不同原子):
表示不同原子):

则参加反应的甲、乙物质的分子数之比为______ ,甲、乙、丙中属于单质的是______ ,下列对反应前后的分析错误的是______ 。
A.元素种类没有改变 B.原子种类没有改变
C.原子个数没有改变 D.分子种类没有改变
(3)12g的碳在不同质量的氧气中燃烧,数据如表。
其中燃烧产物完全是一氧化碳的是______ (填标号)。
(1)为了验证质量守恒定律,实验小组分别选取以下三组药品,通过称量比较各组物质在密闭容器内混合前后的总质量,不能达到目的的有______。
| A.铁和硫酸铜溶液 | B.铜和稀盐酸 | C.白磷和空气 |
 、
、 表示不同原子):
表示不同原子):
则参加反应的甲、乙物质的分子数之比为
A.元素种类没有改变 B.原子种类没有改变
C.原子个数没有改变 D.分子种类没有改变
(3)12g的碳在不同质量的氧气中燃烧,数据如表。
| A | B | C | |
| 碳 | 12g | 12g | 12g |
| 氧气 | 6g | 16g | 80g |
您最近一年使用:0次
2022-02-26更新
|
125次组卷
|
3卷引用:福建省三明市尤溪县2021-2022学年九年级下学期开学考试化学试题
福建省三明市尤溪县2021-2022学年九年级下学期开学考试化学试题福建省三明市明溪县2021-2022学年九年级上学期综合练习化学试题(已下线)第五单元 化学方程式B卷-2023-2024学年九年级化学上册同步测试优选卷(人教版)
解题方法
3 . 拉瓦锡用定量的方法研究空气的成分。某兴趣小组利用氧气传感器测定足量红磷燃烧过程中氧气的含量,结果如图所示,下列判断正确的是
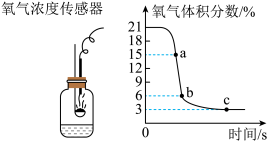
| A.a 点时容器内氮气体积分数为85% |
| B.容器内物质的总质量为:b 点>c 点 |
| C.此实验说明物质燃烧时氧气必须达到一定浓度 |
| D.此实验分析得出空气中氧气的质量分数为18% |
您最近一年使用:0次
解题方法
4 . 下列实验不能达到实验目的的是( )
A. 检验氢气纯度 检验氢气纯度 |
B. 探究石墨导电性 探究石墨导电性 |
C. 用肥皂水区分软水和硬水 用肥皂水区分软水和硬水 |
D. 探究化学反应是否遵循质量守恒定律 探究化学反应是否遵循质量守恒定律 |
您最近一年使用:0次
5 . 化学课堂中,老师演示了“吹气生火”实验,他向包有过氧化钠(Na2O2)粉末的脱脂棉上用导管吹气,脱脂棉燃烧了起来。同学们对该实验产生了浓厚兴趣,进行了如下探究。
探究一:脱脂棉燃烧的原因。
[作出猜想]
(1)根据燃烧条件分析:
①脱脂棉是可燃物;
②吹出的气体可能与过氧化钠反应生成了氧气;
③反应放出热量,满足了温度达到脱脂棉的________ 。
[进行实验]
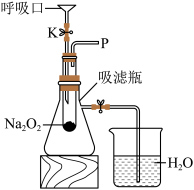
(2)在如图所示装置中,向过氧化钠粉末中不断吹气,观察到过氧化钠粉末由淡黄色逐渐变为白色,在导管口P处放置_______ ,木条复燃,说明试管内生成了氧气。同时还观察到_____ ,说明反应还放出了热量。
探究二:试管内残留白色固体的成分。
[查阅资料]①吹出的气体主要成分有氮气、二氧化碳和水蒸气;② 过氧化钠与氮气不反应。
[作出猜想]
(3)猜想1:CO2参加反应,固体成分是Na2CO3;
猜想2:H2O参加反应,固体成分是NaOH;
猜想3:CO2和H2O均参加反应,固体成分是_____ 。
[实验验证]
(4)实验过程如下:
[实验结论]
(5)过氧化钠与二氧化碳、水蒸气都能反应,猜想3正确。请写出过氧化钠与二氧化碳反应的化学方程式:_____ 。
[拓展延伸]
(6)化工厂存有过氧化钠时,一旦失火,应选用________灭火(填字母序号)。
探究一:脱脂棉燃烧的原因。
[作出猜想]
(1)根据燃烧条件分析:
①脱脂棉是可燃物;
②吹出的气体可能与过氧化钠反应生成了氧气;
③反应放出热量,满足了温度达到脱脂棉的
[进行实验]
(2)在如图所示装置中,向过氧化钠粉末中不断吹气,观察到过氧化钠粉末由淡黄色逐渐变为白色,在导管口P处放置
探究二:试管内残留白色固体的成分。
[查阅资料]①吹出的气体主要成分有氮气、二氧化碳和水蒸气;② 过氧化钠与氮气不反应。
[作出猜想]
(3)猜想1:CO2参加反应,固体成分是Na2CO3;
猜想2:H2O参加反应,固体成分是NaOH;
猜想3:CO2和H2O均参加反应,固体成分是
[实验验证]
(4)实验过程如下:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取残留白色固体于试管中配成溶液, 向其中加入足量的氯化钡溶液,静置 | 产生白色沉淀 | 固体成分含有碳酸钠 |
| ②取适量①的上层清液于试管中,向其 中滴加少量氯化铜溶液 | 产生蓝色沉淀 | 固体成分含有 |
[实验结论]
(5)过氧化钠与二氧化碳、水蒸气都能反应,猜想3正确。请写出过氧化钠与二氧化碳反应的化学方程式:
[拓展延伸]
(6)化工厂存有过氧化钠时,一旦失火,应选用________灭火(填字母序号)。
| A.二氧化碳灭火器 | B.细沙 | C.水基型灭火器 |
您最近一年使用:0次
解题方法
6 . 拉瓦锡用定量的方法研究了空气的成分。某兴趣小组利用氧气传感器来检测足量红磷燃烧过程中氧气的含量,如图所示,下列判断正确的是


| A.a点时容器内氮气体积分数为85% |
| B.容器内物质总质量:b点大于c点 |
| C.氧气有剩余,说明物质燃烧时氧气必须达到一定浓度 |
| D.此实验测得空气中氧气的质量分数为21% |
您最近一年使用:0次
解题方法
7 . 化学课堂上,老师如图1演示了教材中两个实验,用于验证质量守恒定律。
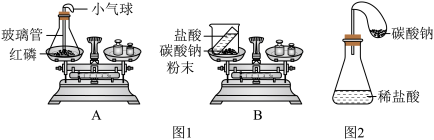
(1)图A实验中,发生的反应化学方程式是___________ 。
(2)同学们对AB实验分别进行了两次称量得如下数据,其中一定有误的是____ (填序号)。
(3)为达到验证量守恒定律的目的,小林更换了B实验中的药品,以下改进正确的是_____ (填序号)。
①换成双氧水和二氧化锰 ②换成氢氧化钠溶液和硫酸铜溶液 ③换成白糖和蒸馏水
(4)为达到验证质量守恒定律的目的,小郭更换了B实验的装置,如图2所示,此装置中气球的作用是________ (填序号)。
①控制气体的总量 ②盛放、添加固体药品 ③调节装置的压强 ④调节装置的容积
改变装置后进行实验,最终发现天平示数变小,原因是______________ 。

(1)图A实验中,发生的反应化学方程式是
(2)同学们对AB实验分别进行了两次称量得如下数据,其中一定有误的是
| 序号 | ① | ② | ③ | ④ |
| 实验类别 | A实验 | A实验 | B实验 | B实验 |
| 反应前称量/g | 280 | 283.5 | 250.3 | 255.2 |
| 反应后称量/g | 280 | 283 | 250.9 | 254.l |
①换成双氧水和二氧化锰 ②换成氢氧化钠溶液和硫酸铜溶液 ③换成白糖和蒸馏水
(4)为达到验证质量守恒定律的目的,小郭更换了B实验的装置,如图2所示,此装置中气球的作用是
①控制气体的总量 ②盛放、添加固体药品 ③调节装置的压强 ④调节装置的容积
改变装置后进行实验,最终发现天平示数变小,原因是
您最近一年使用:0次
解题方法
8 . 探究实验也要“数字化”。某同学利用足量红磷在空气中燃烧,通过氧气传感器来监测燃烧

| A.a点时容器内氮气体积分数为85% | B.容器内物质总质量b点>c点 |
| C.此实验测得空气中氧气的质量分数为18% | D.氧气有剩余,说明燃烧时氧气必须达到一定浓度 |
您最近一年使用:0次
解题方法
9 . 质量守恒定律对科学发展具有重大意义。用如图所示的2个实验装置进行验证质量守恒定律的实验,其中B不能达到实验目的的原因是__________ ;写出A中反应的化学方程式___________ 。


您最近一年使用:0次
10 . 下列是初中化学中的-些常见的实验。请回答:

(1)A是电解水成功的实验:分析M端是电源的______ (选填“正极”或“负极”)。
(2)B是验证铜、银活动性的实验:该实验反应足够时间后,溶液会变为______ 色。
(3)C是验证CO2的性质的实验:本实验得出CO2的化学性质是______ 。
(4)D是小欣设计的短时间内验证质量守恒定律的实验:请你分析,她的设计______ (选填“能”或“不能”)达到实验目的。

(1)A是电解水成功的实验:分析M端是电源的
(2)B是验证铜、银活动性的实验:该实验反应足够时间后,溶液会变为
(3)C是验证CO2的性质的实验:本实验得出CO2的化学性质是
(4)D是小欣设计的短时间内验证质量守恒定律的实验:请你分析,她的设计
您最近一年使用:0次



