解题方法
1 . 葡萄糖(化学式 )在人体组织里经过酶的催化,转变成水、二氧化碳,同时放出能量,供机体活动和维持恒定体温。计算:
)在人体组织里经过酶的催化,转变成水、二氧化碳,同时放出能量,供机体活动和维持恒定体温。计算:
(1)葡萄糖的相对分子质量是______ ;
(2)葡萄糖中碳、氢元素质量比是______ (填最简比);
(3)葡萄糖中碳元素质量分数是______ 。
 )在人体组织里经过酶的催化,转变成水、二氧化碳,同时放出能量,供机体活动和维持恒定体温。计算:
)在人体组织里经过酶的催化,转变成水、二氧化碳,同时放出能量,供机体活动和维持恒定体温。计算:(1)葡萄糖的相对分子质量是
(2)葡萄糖中碳、氢元素质量比是
(3)葡萄糖中碳元素质量分数是
您最近一年使用:0次
解题方法
2 . 燃气泄漏不易察觉,家用煤气一般加入了有特殊气味的乙硫醇(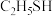 )。空气中乙硫醇含量达五百亿分之一时,就会被人闻到。下列有关乙硫醇说法正确的是
)。空气中乙硫醇含量达五百亿分之一时,就会被人闻到。下列有关乙硫醇说法正确的是
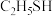 )。空气中乙硫醇含量达五百亿分之一时,就会被人闻到。下列有关乙硫醇说法正确的是
)。空气中乙硫醇含量达五百亿分之一时,就会被人闻到。下列有关乙硫醇说法正确的是| A.乙硫醇由2个碳原子、6个氢原子、1个硫原子构成 |
| B.乙硫醇中C、H元素质量比1∶3 |
| C.乙硫醇属于有机物 |
| D.乙硫醇中碳元素质量分数最大 |
您最近一年使用:0次
3 . 阅读下列短文并回答相关问题。
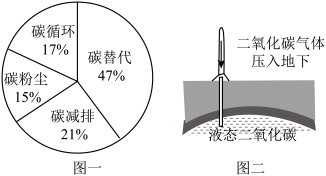
I、【资料一】排入大气中的CO2越来越多,导致温室效应增强。减少CO2排放,实现碳中和,已成为全球共识。碳替代、碳减排、碳封存、碳循环是实现碳中和的四种主要途径。科学家预测,到2050年,四种途径对全球碳中和的贡献率如图一所示。
(1)到2050年,对全球碳中和贡献最大的途径为______ 。
(2)某实验基地的图二技术属于图一中的碳中和途径;用分子的观点解释图二的碳中和过程:______ 。
(3)在20℃时,Ca(OH)2和NaOH的溶解度分别为0.165g和109g。用NaOH溶液喷淋“捕捉”空气中的CO2,可实现碳循环。已知CO2也能与氢氧化钙溶液反应,但该过程不适合选用Ca(OH)2溶液代替NaOH溶液,你认为主要原因为______ 。
(4)碳中和是指CO2的排放量和减少总量相当。下列做法中,有利于实现此目标的为______(填标号)。
Ⅱ、【资料二】氢气是21世纪正在开发利用的一种清洁能源,使用氢能源能有效减少CO2的排放。我国科学家研究的一种储氢、释氢材料为固体AlH3,其中释放氢能原理是利用AlH3与H2O发生反应,生成Al(OH)3和氢气。
由资料二可知;
(5)释放氢能的化学方程式为______ ;该反应生成物中氢元素的化合价为______ 。
(6)氢气被视为清洁能源的原因为______ 。
(7)释氢材料AlH3中,氢元素的质量分数为______ 。
I、【资料一】排入大气中的CO2越来越多,导致温室效应增强。减少CO2排放,实现碳中和,已成为全球共识。碳替代、碳减排、碳封存、碳循环是实现碳中和的四种主要途径。科学家预测,到2050年,四种途径对全球碳中和的贡献率如图一所示。
(1)到2050年,对全球碳中和贡献最大的途径为
(2)某实验基地的图二技术属于图一中的碳中和途径;用分子的观点解释图二的碳中和过程:
(3)在20℃时,Ca(OH)2和NaOH的溶解度分别为0.165g和109g。用NaOH溶液喷淋“捕捉”空气中的CO2,可实现碳循环。已知CO2也能与氢氧化钙溶液反应,但该过程不适合选用Ca(OH)2溶液代替NaOH溶液,你认为主要原因为
(4)碳中和是指CO2的排放量和减少总量相当。下列做法中,有利于实现此目标的为______(填标号)。
| A.用太阳能、风能等清洁能源代替化石燃料的使用 |
| B.大规模开采可燃冰 |
| C.大力植树造林,严禁乱砍滥伐 |
Ⅱ、【资料二】氢气是21世纪正在开发利用的一种清洁能源,使用氢能源能有效减少CO2的排放。我国科学家研究的一种储氢、释氢材料为固体AlH3,其中释放氢能原理是利用AlH3与H2O发生反应,生成Al(OH)3和氢气。
由资料二可知;
(5)释放氢能的化学方程式为
(6)氢气被视为清洁能源的原因为
(7)释氢材料AlH3中,氢元素的质量分数为
您最近一年使用:0次
解题方法
4 .  的捕集与资源化利用是化学研究的热点之一。
的捕集与资源化利用是化学研究的热点之一。
 的捕集
的捕集
一种利用CaO捕集 的流程如图-1所示。
的流程如图-1所示。
(1)大气中 含量上升会导致的主要环境问题是
含量上升会导致的主要环境问题是______ 。
(2)“煅烧炉”中发生的反应的化学方程式为______ 。
(3)研究发现,加热 也可获得CaO,反应方程式为
也可获得CaO,反应方程式为
 ,该反应所制得的CaO比石灰石分解制得的CaO捕集
,该反应所制得的CaO比石灰石分解制得的CaO捕集 的效果更好,主要原因是
的效果更好,主要原因是______ 。
Ⅱ. 的资源化利用
的资源化利用
(4)以二氧化碳为原料制取炭黑的太阳能工艺如图-2所示。反应①过程中铁元素的质量分数______ (填“增大”“减小”或“不变”),反应②属于基本类型的______ 反应。
(5)以ZnO― 为催化剂,以
为催化剂,以 和
和 为原料合成甲醇,主要反应的微观过程如图-3所示,同时发生副反应:
为原料合成甲醇,主要反应的微观过程如图-3所示,同时发生副反应: 。
。
① 中Zr的化合价为
中Zr的化合价为______ 。
②图-3所示的合成反应中,生成物丙和丁的质量比为______ 。
③合成过程中, 转化率(
转化率(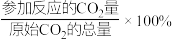 )及甲醇选择性(
)及甲醇选择性(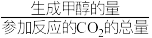
 ,且甲醇选择性+CO选择性=100%)随温度的变化如题25图-4所示。随温度升高,
,且甲醇选择性+CO选择性=100%)随温度的变化如题25图-4所示。随温度升高, 转化率升高,但产物中甲醇含量降低,原因是
转化率升高,但产物中甲醇含量降低,原因是______ 。
 的捕集与资源化利用是化学研究的热点之一。
的捕集与资源化利用是化学研究的热点之一。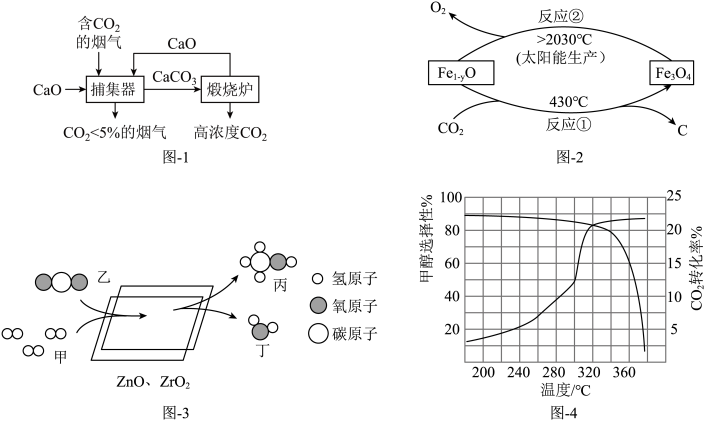
 的捕集
的捕集一种利用CaO捕集
 的流程如图-1所示。
的流程如图-1所示。(1)大气中
 含量上升会导致的主要环境问题是
含量上升会导致的主要环境问题是(2)“煅烧炉”中发生的反应的化学方程式为
(3)研究发现,加热
 也可获得CaO,反应方程式为
也可获得CaO,反应方程式为
 ,该反应所制得的CaO比石灰石分解制得的CaO捕集
,该反应所制得的CaO比石灰石分解制得的CaO捕集 的效果更好,主要原因是
的效果更好,主要原因是Ⅱ.
 的资源化利用
的资源化利用(4)以二氧化碳为原料制取炭黑的太阳能工艺如图-2所示。反应①过程中铁元素的质量分数
(5)以ZnO―
 为催化剂,以
为催化剂,以 和
和 为原料合成甲醇,主要反应的微观过程如图-3所示,同时发生副反应:
为原料合成甲醇,主要反应的微观过程如图-3所示,同时发生副反应: 。
。①
 中Zr的化合价为
中Zr的化合价为②图-3所示的合成反应中,生成物丙和丁的质量比为
③合成过程中,
 转化率(
转化率(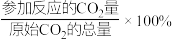 )及甲醇选择性(
)及甲醇选择性(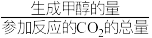
 ,且甲醇选择性+CO选择性=100%)随温度的变化如题25图-4所示。随温度升高,
,且甲醇选择性+CO选择性=100%)随温度的变化如题25图-4所示。随温度升高, 转化率升高,但产物中甲醇含量降低,原因是
转化率升高,但产物中甲醇含量降低,原因是
您最近一年使用:0次
解题方法
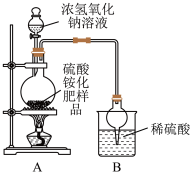
5 . 某兴趣小组设计如图所示装置对硫酸铵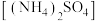 化肥进行等级测定(该化肥中没有其它含氮物质)。
化肥进行等级测定(该化肥中没有其它含氮物质)。
已知:
①氨气极易溶于水,氨水呈碱性,不稳定,易挥发。
②碱石灰是一种常见的干燥剂,其主要成分是CaO和NaOH固体混合物。
③硫酸铵化肥等级指标如表:
 逸出,其反应方程式为:
逸出,其反应方程式为: 。X的化学式为
。X的化学式为______ 。
(2)同学们认为用该实验装置测得的硫酸铵化肥含氮量可能偏高,应在实验装置A、B之间增加一个装有______ (填“浓硫酸”或“碱石灰”)的干燥装置。
(3)经同学们充分讨论,改进实验装置,排除可能产生误差的因素,重新实验。取硫酸铵化肥样品27.0g进行实验,测得B装置增重6.8g。请通过计算判断该化肥的等级。(写出计算过程)______ 。
(4)若B中的稀硫酸用浓硫酸代替,测得的硫酸铵质量分数将______ (填“偏大”“不变”或“偏小”),原因是______ 。
(5)下列关于化肥的说法中正确的是______ 。
a.化肥对农业增产增收有重要作用
b.滥用化肥可能引起环境污染
c.根据颜色可将常见化肥鉴别开来
d.硫酸铵可与草木灰等碱性肥料混合施用
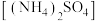 化肥进行等级测定(该化肥中没有其它含氮物质)。
化肥进行等级测定(该化肥中没有其它含氮物质)。已知:
①氨气极易溶于水,氨水呈碱性,不稳定,易挥发。
②碱石灰是一种常见的干燥剂,其主要成分是CaO和NaOH固体混合物。
③硫酸铵化肥等级指标如表:
| 指标项目 | 优等品 | 合格品 |
| 氮(N)含量 | ≥21.0% | ≥20.5% |
 逸出,其反应方程式为:
逸出,其反应方程式为: 。X的化学式为
。X的化学式为(2)同学们认为用该实验装置测得的硫酸铵化肥含氮量可能偏高,应在实验装置A、B之间增加一个装有
(3)经同学们充分讨论,改进实验装置,排除可能产生误差的因素,重新实验。取硫酸铵化肥样品27.0g进行实验,测得B装置增重6.8g。请通过计算判断该化肥的等级。(写出计算过程)
(4)若B中的稀硫酸用浓硫酸代替,测得的硫酸铵质量分数将
(5)下列关于化肥的说法中正确的是
a.化肥对农业增产增收有重要作用
b.滥用化肥可能引起环境污染
c.根据颜色可将常见化肥鉴别开来
d.硫酸铵可与草木灰等碱性肥料混合施用
您最近一年使用:0次
解题方法
6 . “侯氏制碱法”是我国著名制碱专家侯德榜做出的杰出贡献,原理可表示为:NH3+NaCl+NaHCO3=NH4Cl+Na2CO3,其最大的优点是降低了成本,提高了NaCl的利用率。
(1)氨气中氮元素的质量分数为______ 。(结果精确至0.1%)
(2)用117 t NaCl(其利用率在96%以上)制碱,至少能生成的Na2CO3质量是多少?(写出计算过程)
(1)氨气中氮元素的质量分数为
(2)用117 t NaCl(其利用率在96%以上)制碱,至少能生成的Na2CO3质量是多少?(写出计算过程)
您最近一年使用:0次
解题方法
7 . “清明插柳,端午插艾”。艾草中含有丰富的黄酮类物质,其中矢车菊黄素的化学式为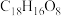 。下列关于
。下列关于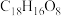 的说法错误的是
的说法错误的是
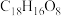 。下列关于
。下列关于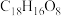 的说法错误的是
的说法错误的是| A.矢车菊黄素是有机物 |
| B.矢车菊黄素中碳元素的质量分数最大 |
| C.矢车菊黄素由碳、氢、氧三种元素组成 |
| D.一个矢车菊黄素分子中含有8个水分子 |
您最近一年使用:0次
解题方法
8 . 醋酸钙虽然钙含量较低.但具有水溶性好、易吸收,胃肠道反应小的特点。因此.肠胃功能欠佳的患者通常建议选用作补钙剂。通常醋酸钙可由以下方法制得: 。
。
(1)醋酸钙中钙元素的质量分数是______ (结果保留两位小数)。
(2)取20g质量分数为30%的醋酸加入足量的氢氧化钙可制得多少醋酸钙?
 。
。(1)醋酸钙中钙元素的质量分数是
(2)取20g质量分数为30%的醋酸加入足量的氢氧化钙可制得多少醋酸钙?
您最近一年使用:0次
解题方法
9 . 木糖醇( )是一种天然甜味剂,食用时有清凉感,因其代谢不受胰岛素调节,可作为蔗糖替代品供糖尿病患者食用。下列关于木糖醇的说法正确的是
)是一种天然甜味剂,食用时有清凉感,因其代谢不受胰岛素调节,可作为蔗糖替代品供糖尿病患者食用。下列关于木糖醇的说法正确的是
 )是一种天然甜味剂,食用时有清凉感,因其代谢不受胰岛素调节,可作为蔗糖替代品供糖尿病患者食用。下列关于木糖醇的说法正确的是
)是一种天然甜味剂,食用时有清凉感,因其代谢不受胰岛素调节,可作为蔗糖替代品供糖尿病患者食用。下列关于木糖醇的说法正确的是| A.木糖醇属于氧化物 |
| B.木糖醇组成中碳元素的质量分数最大 |
| C.木糖醇由碳、氢、氧三种元素组成 |
| D.木糖醇由5个碳原子、12个氢原子、5个氧原子构成 |
您最近一年使用:0次
解题方法
10 . 炒糖色主要利用蔗糖(C12H22O11)发生焦糖化反应给食物上色。下列说法正确的是
| A.蔗糖属于氧化物 |
| B.蔗糖中氢元素的质量分数最大 |
| C.蔗糖分子中的氢、氧原子个数比与水分子中的氢、氧原子个数比相同 |
| D.蔗糖溶于水后“消失”不见的原因是蔗糖分子变小了 |
您最近一年使用:0次



