解题方法
1 . 硫是一种常见的非金属元素,其化合价与物质类别之间的关系如图。
【查阅资料】1 SO2:熔点-72℃,沸点:-10℃;SO3熔点:16.8℃,沸点:44.8℃
2 同温同压下,气体体积比等于分子个数比
【提出问题】硫与足量的O2反应是否生成:SO3?
【猜想与假设】
猜想1:硫与足量的O2反应会生成SO3
猜想2:硫与足量的O2反应不会直接生成SO3。
(1)从图的“价类”二维图中,SO2和SO3对应的点是_____ 、____ (选填“A、B、C、D、E”)。

(2)从碳与氧气反应的角度,阐述猜想1的合理性______ 。
【实验验证】
取0.1g硫粉放入500mL圆底烧瓶中(保证氧气充足且容器压强在安全值内),实验装置如图1。加热,用传感器测得烧瓶内压强的变化,测得数据如图2。

(3)本实验取得成功的关键操作是______ 。
(4)图2中加热至B点(硫即将完全气化)熄灭酒精灯,到C点时间压强达到峰值,可判断该反应是_____ (选填“吸热”或“放热”)反应。
(5)通过图2数据分析,可认为没有SO3产生,其依据是______ 。
(6)写出硫在氧气中燃烧的化学方程式_______ 。
【拓展延伸】
(7)空气中的SO2在粉尘等催化作用下生成SO3,SO3与雨水结合形成酸雨,写出SO2转化为SO3的化学方程式______ 。
【查阅资料】1 SO2:熔点-72℃,沸点:-10℃;SO3熔点:16.8℃,沸点:44.8℃
2 同温同压下,气体体积比等于分子个数比
【提出问题】硫与足量的O2反应是否生成:SO3?
【猜想与假设】
猜想1:硫与足量的O2反应会生成SO3
猜想2:硫与足量的O2反应不会直接生成SO3。
(1)从图的“价类”二维图中,SO2和SO3对应的点是

(2)从碳与氧气反应的角度,阐述猜想1的合理性
【实验验证】
取0.1g硫粉放入500mL圆底烧瓶中(保证氧气充足且容器压强在安全值内),实验装置如图1。加热,用传感器测得烧瓶内压强的变化,测得数据如图2。

(3)本实验取得成功的关键操作是
(4)图2中加热至B点(硫即将完全气化)熄灭酒精灯,到C点时间压强达到峰值,可判断该反应是
(5)通过图2数据分析,可认为没有SO3产生,其依据是
(6)写出硫在氧气中燃烧的化学方程式
【拓展延伸】
(7)空气中的SO2在粉尘等催化作用下生成SO3,SO3与雨水结合形成酸雨,写出SO2转化为SO3的化学方程式
您最近一年使用:0次
解题方法
2 . 为测定空气中氧气的含量,化学兴趣小组同学在老师的指导下进行创新设计。

(1)第一小组先仿照课本如图1装置进行实验:
①红磷燃烧时,可观察到产生大量的______ 。
②红磷燃烧停止,冷却到室温后,打开止水夹,可观察到烧杯中的水会回流进入集气瓶,水位大约上升到刻度______ 处。
③请写出红磷燃烧的文字表达式为______ 。
(2)第二小组对实验进行了小小的改进并取得成功,装置如图2所示:
①其中放大镜的作用是______ ;
②请指出该装置的一个优点:______ 。
(3)第三小组利用图3所示装置测量空气中氧气的体积分数也取得成功。
【实验准备】锥形瓶内空气体积为230 mL,注射器中水的体积为50 mL,该装置气密性良好。
【实验探究】装入药品,按图连好仪器,夹紧弹簧夹。先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。
【现象分析】①足量的白磷在锥形瓶中未能全部燃烧,说明瓶内剩余气体______ (填“支持”或“不支持”)燃烧。
②在整个实验过程中,可观察到气球的变化是______ 。
③待白磷熄灭锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象是:
a、注射器中的水自动喷出来;
b、当注射器中的水还剩下约______ mL时停止往下流。
【得出结论】氧气体积约占空气总体积的______ 。
【反思与交流】
以上三个小组测定氧气含量的实验装置不同,但原理相同。其原理是利用化学反应消耗密闭容器内的氧气而不产生其他气体,导致密闭容器内的压强______ ,在大气压的作用下,部分水回流到密闭容器内。上图中,烧杯或注射器中水的作用是______ 。因此,实验时红磷______ (填“能”或“不能”) 用木炭或硫代替。

(1)第一小组先仿照课本如图1装置进行实验:
①红磷燃烧时,可观察到产生大量的
②红磷燃烧停止,冷却到室温后,打开止水夹,可观察到烧杯中的水会回流进入集气瓶,水位大约上升到刻度
③请写出红磷燃烧的文字表达式为
(2)第二小组对实验进行了小小的改进并取得成功,装置如图2所示:
①其中放大镜的作用是
②请指出该装置的一个优点:
(3)第三小组利用图3所示装置测量空气中氧气的体积分数也取得成功。
【实验准备】锥形瓶内空气体积为230 mL,注射器中水的体积为50 mL,该装置气密性良好。
【实验探究】装入药品,按图连好仪器,夹紧弹簧夹。先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。
【现象分析】①足量的白磷在锥形瓶中未能全部燃烧,说明瓶内剩余气体
②在整个实验过程中,可观察到气球的变化是
③待白磷熄灭锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象是:
a、注射器中的水自动喷出来;
b、当注射器中的水还剩下约
【得出结论】氧气体积约占空气总体积的
【反思与交流】
以上三个小组测定氧气含量的实验装置不同,但原理相同。其原理是利用化学反应消耗密闭容器内的氧气而不产生其他气体,导致密闭容器内的压强
您最近一年使用:0次
3 . 某校化学实验小组开展制取氧气和探究氧气性质的实验活动与评价。
【实验Ⅰ】你是甲实验小组成员,参与实验室制取氧气的活动。
(1)选择实验方案。实验室可提供三种制取氧气的方案。
A. 加热高锰酸钾 B. 加热混有二氧化锰的氯酸钾 C. 二氧化锰催化分解过氧化氢
你所选方案对应反应的文字表达式为________ 。小组讨论决定选用A方案。
(2)进行实验活动。小组同学分工协作完成如下任务:
①A同学负责选择组装制取气体装置的仪器。

她选择了铁架台、带有导管的橡胶塞、水槽、试管,还应根据如图所提供的仪器,选择_________ 、___________ (填仪器名称)。
②B同学负责取用药品。他先检查装置________ ,再用纸槽小心地把高锰酸钾粉末送至试管________ (填“中部”或“底部”)后直立试管,抽出纸槽。
③C同学负责组装仪器。他按“从下到上、从左到右”的顺序组装制取装置,固定试管时注意到试管口应略 ________ ,其目的是_________ 。
④你负责排水法收集氧气。开始收集的时机是_________ 。收集到两瓶气体,均呈紫红色。
⑤实验结束,待试管冷却,将残余物倒入指定容器,用__________ (填仪器名称)洗涤试管;洗涤干净的试管应________ 于试管架上;整理好实验台,报告老师后离开实验室。
(3)评价与反思。小组同学都认为体验到了实验活动的乐趣,但因实验过程存在不足,同意本次活动表现评价为“有待改进”。针对存在的不足,你提出的一条实验改进意见是_________ 。
【实验Ⅱ】乙实验小组探究氧气的性质
(4)该小组同学利用甲组制取的氧气进行氧气性质等探究实验。实验装置如图。

①实验1反应的文字表达式________ 。
②实验2是铁丝在氧气中燃烧,能说明该变化是化学变化的现象是_________ ,该反应的文字表达式________ 。铁丝在空气中不能燃烧却可以在氧气中燃烧,说明氧气的化学性质比较______ ,也说明物质在空气中燃烧的剧烈程度与________ 有关。
③实验3的目的是测定_________ ,红磷燃烧的文字表达式为________ 。
【实验Ⅲ】拓展与应用
(5)丙实验小组查阅资料得知:镁不仅能与氧气反应,还可在氮气中燃烧生成氮化镁(Mg3N2),且燃烧时会发出暗红色火焰。同学们很好奇,设计了如下方案进行探究。
步骤1:用盛水的水槽、无底的废广口瓶、燃烧匙、蒸发皿、橡胶塞等组装成如上图实验4所示的装置。另准备一个同型号的橡胶塞,用铜丝穿过胶塞并在末端系牢一根镁条。
步骤2:引燃燃烧匙中足量的红磷,塞好橡胶塞。待充分冷却,观察到广口瓶内水面上升的体积约占瓶内水面原上方空间的1/5左右。
步骤3:往水槽中加水使广口瓶内外水面相平。将镁条点燃,迅速更换并塞紧橡胶塞,观察到镁条在广口瓶内继续燃烧,发出暗红色火焰,放热。待冷却后广口瓶内水位继续上升。
[表达与交流] ①步骤2的目的是_____ 。
②步骤3“待冷却后广口瓶内水位继续上升”是由于瓶内气压____ (填“大于”或“小于”)外界气压。
③根据上述实验和你所学的知识,请写出镁在氮气中燃烧的文字表达式:________ 。
[反思与评价]小组内有同学说:“镁还能在二氧化碳中燃烧,期待下次再进行相关探究!”
【实验Ⅰ】你是甲实验小组成员,参与实验室制取氧气的活动。
(1)选择实验方案。实验室可提供三种制取氧气的方案。
A. 加热高锰酸钾 B. 加热混有二氧化锰的氯酸钾 C. 二氧化锰催化分解过氧化氢
你所选方案对应反应的文字表达式为
(2)进行实验活动。小组同学分工协作完成如下任务:
①A同学负责选择组装制取气体装置的仪器。

她选择了铁架台、带有导管的橡胶塞、水槽、试管,还应根据如图所提供的仪器,选择
②B同学负责取用药品。他先检查装置
③C同学负责组装仪器。他按“从下到上、从左到右”的顺序组装制取装置,固定试管时注意到试管口应
④你负责排水法收集氧气。开始收集的时机是
⑤实验结束,待试管冷却,将残余物倒入指定容器,用
(3)评价与反思。小组同学都认为体验到了实验活动的乐趣,但因实验过程存在不足,同意本次活动表现评价为“有待改进”。针对存在的不足,你提出的一条实验改进意见是
【实验Ⅱ】乙实验小组探究氧气的性质
(4)该小组同学利用甲组制取的氧气进行氧气性质等探究实验。实验装置如图。

①实验1反应的文字表达式
②实验2是铁丝在氧气中燃烧,能说明该变化是化学变化的现象是
③实验3的目的是测定
【实验Ⅲ】拓展与应用
(5)丙实验小组查阅资料得知:镁不仅能与氧气反应,还可在氮气中燃烧生成氮化镁(Mg3N2),且燃烧时会发出暗红色火焰。同学们很好奇,设计了如下方案进行探究。
步骤1:用盛水的水槽、无底的废广口瓶、燃烧匙、蒸发皿、橡胶塞等组装成如上图实验4所示的装置。另准备一个同型号的橡胶塞,用铜丝穿过胶塞并在末端系牢一根镁条。
步骤2:引燃燃烧匙中足量的红磷,塞好橡胶塞。待充分冷却,观察到广口瓶内水面上升的体积约占瓶内水面原上方空间的1/5左右。
步骤3:往水槽中加水使广口瓶内外水面相平。将镁条点燃,迅速更换并塞紧橡胶塞,观察到镁条在广口瓶内继续燃烧,发出暗红色火焰,放热。待冷却后广口瓶内水位继续上升。
[表达与交流] ①步骤2的目的是
②步骤3“待冷却后广口瓶内水位继续上升”是由于瓶内气压
③根据上述实验和你所学的知识,请写出镁在氮气中燃烧的文字表达式:
[反思与评价]小组内有同学说:“镁还能在二氧化碳中燃烧,期待下次再进行相关探究!”
您最近一年使用:0次
4 . 某研究小组在学习氧气的化学性质时发现:碳在氧气中燃烧没有火焰,而蜡烛在氧气中燃烧却有明亮的火焰。该小组同学进行了如下探究。
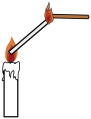
(1)①探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示)。由此可知:蜡烛燃烧产生的火焰是由_______ (填“固态”或“气态”)物质燃烧形成的。
(2)②探究二:物质燃烧产生火焰的根本原因是什么?
【查阅资料】
由上表可知:物质燃烧能否产生火焰与其_________ (填“熔点”或“沸点”)和燃烧时温度有关。通过上表中石蜡、铁的数据对比,你认为物质燃烧时,什么情况下能产生火焰?________ 。由此推测:钠在燃烧时______ (填“有”或“没有”)火焰产生。
(3)③根据硫在空气或氧气中燃烧的实验事实,请你推测硫沸点______ 硫燃烧时的温度(填“>”或“<”或“=”)

(1)①探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示)。由此可知:蜡烛燃烧产生的火焰是由
(2)②探究二:物质燃烧产生火焰的根本原因是什么?
【查阅资料】
物质 | 熔点/℃ | 沸点/℃ | 燃烧时温度/℃ |
石蜡 | 50~70 | 300~550 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |
(3)③根据硫在空气或氧气中燃烧的实验事实,请你推测硫沸点
您最近一年使用:0次
2022-11-05更新
|
71次组卷
|
4卷引用:福建省厦门市第五中学2023-2024学年九年级上学期第一次月考化学试题
解题方法
5 . 验室中常用分解过氧化氢来简便快速的制备氧气,化学小组进一步探究外界条件对过氧化氢分解速率的影响,并进行了氧气的性质实验。
[查阅资料]有些水果、蔬菜对过氧化氢的分解有催化作用。
[实验探究 1]探究苹果和土豆对过氧化氢分解是否有催化作用及催化效果:各量取 6ml 的过氧化氢溶液,分别倒入 1、2、3 号三支试管中,取大小、形状基本相同的苹果块和土豆块,分别放入 2、3 号试管中,并把带火星的木条分别同时伸入三支试管口内,观察现象并记录如下:
[实验探究 2]探究浓度对过氧化氢分解速率的影响:取 10ml 30%的过氧化氢三份,将其中两份分别稀释为不同浓度的溶液,同时测定收集到 100ml 氧气所用的时间,(其它实验条件均相同)记录如下:
[实验探究 3]用上述收集的氧气与不同物种进行反应,其中有一固体能在氧气中燃烧,发出明亮的蓝紫色火焰,产生刺激性气味的气体,该反应的化学符号表达式为:____________________ 。
[查阅资料]有些水果、蔬菜对过氧化氢的分解有催化作用。
[实验探究 1]探究苹果和土豆对过氧化氢分解是否有催化作用及催化效果:各量取 6ml 的过氧化氢溶液,分别倒入 1、2、3 号三支试管中,取大小、形状基本相同的苹果块和土豆块,分别放入 2、3 号试管中,并把带火星的木条分别同时伸入三支试管口内,观察现象并记录如下:
试管编号 | 1 | 2 | 3 | |
材料名称 | 无 | 苹果 | 土豆 | |
实验现象 | 反应速率 | 很慢 | 稍快 | 较快 |
产生气泡 | 很少 | 比 1 中多 | 较多 | |
复燃情况 | 不复燃 | 复燃 | 很快复燃 | |
实验结论 | | |||
[实验探究 2]探究浓度对过氧化氢分解速率的影响:取 10ml 30%的过氧化氢三份,将其中两份分别稀释为不同浓度的溶液,同时测定收集到 100ml 氧气所用的时间,(其它实验条件均相同)记录如下:
实验编号 | 1 | 2 | 3 |
过氧化氢溶液浓度 | 5% | 15% | 30% |
所用时间(秒) | 205 | 25 | 3 |
实验结论 | | ||
[实验探究 3]用上述收集的氧气与不同物种进行反应,其中有一固体能在氧气中燃烧,发出明亮的蓝紫色火焰,产生刺激性气味的气体,该反应的化学符号表达式为:
您最近一年使用:0次
2021-09-30更新
|
67次组卷
|
2卷引用:福建省厦门市湖里区蔡塘学校2019-2020学年九年级上学期期中化学试题



