解题方法
1 . 下列实验设计不能达到目的的是
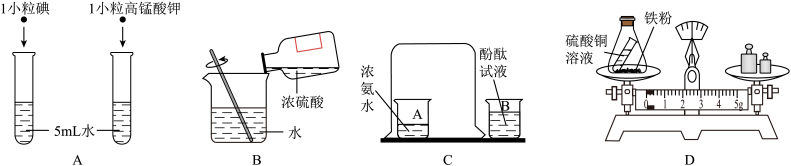

| A.比较不同溶质在同种溶剂中的溶解性 | B.稀释浓硫酸 |
| C.探究分子在不断运动 | D.验证质量守恒定律 |
您最近一年使用:0次
解题方法
2 . 归纳法是学习化学的重要方法。下列选项正确的
A.化学性质相似 | B.物质的溶解性分类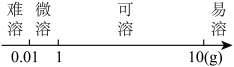 |
C.石蕊试液显色 | D.化学反应基本类型 |
您最近一年使用:0次
3 . 下列实验设计能达到实验主要目的是
| 选项 | 实验目的 | 实验设计 |
| A | 探究温度对分子运动快慢的影响 |
|
| B | 探究氧气对铁钉锈蚀的影响 |
|
| C | 比较Zn和Fe的金属活动性强弱 |
|
| D | 探究影响物质溶解性的因素 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 结合下图回答问题。

(1)甲实验:集气瓶中放少量水的目的是_______ 。铁丝在氧气中燃烧的化学方程式为_______ 。
(2)乙实验:通过对比实验得出结论:铁生锈需要和_______ 接触。
(3)丙实验:得出的实验结论是_______ 。

(1)甲实验:集气瓶中放少量水的目的是
(2)乙实验:通过对比实验得出结论:铁生锈需要和
(3)丙实验:得出的实验结论是
您最近一年使用:0次
解题方法
5 . 下列探究实验能达到目的的是
| A.探究温度对分子运动速率的影响,只将少量品红加入到热水中 |
| B.探究不同物质在同一溶剂中的溶解性不同,可将0.1克碘和0.1克高锰酸钾分别放入5mL水中 |
| C.探究MnO2是否是H2O分解的催化剂,比较MnO2加到H2O2溶液前后产生气泡快慢 |
| D.探究吸入空气和呼出气体中O2含量不同,将带火星的木条分别伸入等体积两种气体中 |
您最近一年使用:0次
解题方法
6 . 下列四个实验不能达到实验目的的是
A. 探究铁生锈的条件 探究铁生锈的条件 |
B. 探究质量守恒定律 探究质量守恒定律 |
C. 探究不同物质在同种溶剂中的溶解性 探究不同物质在同种溶剂中的溶解性 |
D. 比较锌和铁的活泼性 比较锌和铁的活泼性 |
您最近一年使用:0次
解题方法
7 . 下列物质的用途是利用其化学性质的是
| A.铁粉用于食品保存 | B.用汽油洗去衣服上的油污 |
| C.稀有气体可制成电光源 | D.铜丝用于制导线 |
您最近一年使用:0次
解题方法
8 . 下列有关实验现象的描述不正确的是
| A.红磷燃烧,发光、放热、产生大量白烟 |
| B.碘放入足量水中,几乎不溶解 |
| C.硝酸铵溶于水,放出大量的热 |
| D.稀盐酸除铁钉上的铁锈,铁钉逐渐变得光亮,溶液由无色变成黄色 |
您最近一年使用:0次
2023-11-22更新
|
30次组卷
|
2卷引用:黑龙江省哈尔滨市香坊区2022—2023学年九年级上学期期末理综试卷
解题方法
9 . 某化学探究小组的同学在学习《溶液》这一单元时,进行下列探究活动,请你参与他们的探究并回答相关问题:
(一)用控制变量方法探究影响物质溶解性的因素:
(1)实验一是探究溶剂种类对物质溶解性的影响,实验现象为氯化钠溶于水,氯化钠几乎不溶于酒精。由此得出的实验结论是______ 。
(2)实验二的目的是探究______ 对硝酸钾溶解性的影响,该实验中需要保持不变的因素是______ 。
(二)下图是配制溶质质量分数为 的
的 溶液的实验操作示意图:
溶液的实验操作示意图:

(3)用上图表示的序号表示配制溶液的正确操作顺序______ 。
(4)图③中玻璃棒的作用是______ 。
(5)称量 时,天平平衡后的状态如图⑤所示,游码标尺示数如下图,则称取
时,天平平衡后的状态如图⑤所示,游码标尺示数如下图,则称取 的实际质量为
的实际质量为______  。
。

(6)根据计算配制的溶液质量应为______  ,需要量取水的体积是
,需要量取水的体积是______  。(水的密度为
。(水的密度为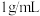 )。
)。
(7)反思:经检测,所配制氯化钠溶液的溶质质量分数偏小,其原因可能是______ (填序号)。
①用量筒量取水时,俯视读数
②转移已称好的氯化钠固体时,部分洒落在烧杯外
③用于溶解的烧杯中有少量的蒸馏水
④转移已配好的溶液时,有少量溶液溅出
(一)用控制变量方法探究影响物质溶解性的因素:
| 实验一 | 实验二 |
 |  |
(2)实验二的目的是探究
(二)下图是配制溶质质量分数为
 的
的 溶液的实验操作示意图:
溶液的实验操作示意图:
(3)用上图表示的序号表示配制溶液的正确操作顺序
(4)图③中玻璃棒的作用是
(5)称量
 时,天平平衡后的状态如图⑤所示,游码标尺示数如下图,则称取
时,天平平衡后的状态如图⑤所示,游码标尺示数如下图,则称取 的实际质量为
的实际质量为 。
。
(6)根据计算配制的溶液质量应为
 ,需要量取水的体积是
,需要量取水的体积是 。(水的密度为
。(水的密度为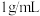 )。
)。(7)反思:经检测,所配制氯化钠溶液的溶质质量分数偏小,其原因可能是
①用量筒量取水时,俯视读数
②转移已称好的氯化钠固体时,部分洒落在烧杯外
③用于溶解的烧杯中有少量的蒸馏水
④转移已配好的溶液时,有少量溶液溅出
您最近一年使用:0次
解题方法
10 . 铁红(Fe2O3)是中国传统红色颜料的重要着色剂,以FeSO4为原料制备铁红的一种方法如图1:


图1 图2
(1)“溶解”时能加快溶解的方法有_____ (写一种)。
(2)“沉淀”时的主要反应为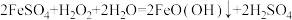 ,则FeO(OH)中铁元素的化合价为
,则FeO(OH)中铁元素的化合价为 _____ 。
(3)实验室进行过滤操作时需要的玻璃仪器有烧杯、玻璃棒和_____ ,其中玻璃棒的作用是 _____ 。
(4)“煅烧” FeO(OH) 时生成两种氧化物,写出“煅烧”时的化学方程式_____ 。
(5)如图2为其他条件相同时不同煅烧温度对产品中Fe2O3质量分数的影响。
①最适宜的煅烧温度为_____ ℃。
②当煅烧温度过高时,产品中Fe2O3质量分数降低,所得产品开始发黑,且铁元素质量分数升高,其可能原因是_____ 。


图1 图2
(1)“溶解”时能加快溶解的方法有
(2)“沉淀”时的主要反应为
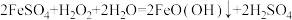 ,则FeO(OH)中铁元素的化合价为
,则FeO(OH)中铁元素的化合价为 (3)实验室进行过滤操作时需要的玻璃仪器有烧杯、玻璃棒和
(4)“煅烧” FeO(OH) 时生成两种氧化物,写出“煅烧”时的化学方程式
(5)如图2为其他条件相同时不同煅烧温度对产品中Fe2O3质量分数的影响。
①最适宜的煅烧温度为
②当煅烧温度过高时,产品中Fe2O3质量分数降低,所得产品开始发黑,且铁元素质量分数升高,其可能原因是
您最近一年使用:0次







