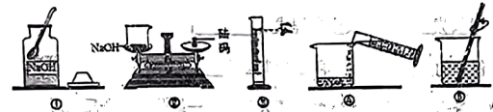
1 . 某同学配制50g6%氢氧化钠溶液,整个操作过程如图所示,回答下列问题:______ ,需称取氢氧化钠______ g,配制时应选用______ mL(选填“10”、20”、“50”、“100”)的量筒量取蒸馏水。
(2)经检测,该同学配制的溶液溶质质量分数偏大,可能的原因是______(填序号)。
(3)欲测定此NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH______ (填“偏大”、“偏小”或“不受影响”)。
(4)向80gNaOH溶液中加入5 g NaOH固体或蒸发掉20g水后,恢复到原温度后均可得到相同溶质质量分数的不饱和NaOH溶液,则原NaOH溶液中溶质的质量分数为______ 。
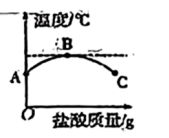
(5)室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度随加入盐酸质量而变化的曲线如图所示。______ (填化学式)。
②在C点溶液中加入碳酸钙,反应的化学方程式为______ 。
(2)经检测,该同学配制的溶液溶质质量分数偏大,可能的原因是______(填序号)。
| A.氢氧化钠固体不纯 | B.用生锈砝码称量 |
| C.装瓶时有少量溶液洒出 | D.溶解时有少量氢氯化钠洒落在烧杯外面 |
(4)向80gNaOH溶液中加入5 g NaOH固体或蒸发掉20g水后,恢复到原温度后均可得到相同溶质质量分数的不饱和NaOH溶液,则原NaOH溶液中溶质的质量分数为
(5)室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度随加入盐酸质量而变化的曲线如图所示。
②在C点溶液中加入碳酸钙,反应的化学方程式为
您最近一年使用:0次
2 . 下列说法正确的是
| A.洗洁精和汽油均可清洗油污,其原理相同 |
| B.同种元素的原子和离子具有相同的质子数 |
| C.燃烧需要同时满足三个条件,所以灭火也要同时破坏三个条件 |
| D.20%的蔗糖溶液中,蔗糖与水的质量比为1:5 |
您最近一年使用:0次
名校
解题方法
3 . 甲、乙物质的溶解度曲线如图所示。则下列说法正确的是

| A.甲的溶解度大于乙的溶解度 |
B. 时,甲和乙溶液的溶质质量分数相等 时,甲和乙溶液的溶质质量分数相等 |
C.将 等质量的甲、乙饱和溶液降温至 等质量的甲、乙饱和溶液降温至 ,忽略析出晶体所带的结晶水,所得溶剂质量甲<乙 ,忽略析出晶体所带的结晶水,所得溶剂质量甲<乙 |
| D.甲溶液中混有少量的乙可用蒸发结晶的方式提纯甲 |
您最近一年使用:0次
2024-04-22更新
|
140次组卷
|
3卷引用:2024年安徽省合肥市肥东县第三中学中考一模化学试题
4 . “天气瓶”是瓶内晶体随气温变化的装饰品。制作步骤为:
Ⅰ、配制溶质质量分数为24%的樟脑的酒精溶液。
Ⅱ、配制硝酸钾、氯化铵和水的混合溶液。
Ⅲ、将上述两种溶液混合装瓶,并密封。______ (填“变大”或“变小”)。
(2)将樟脑的酒精饱和溶液滴入水中,出现了明显的浑浊,说明樟脑在水中的溶解能力______ (填“强于”或“弱于”)其在酒精中的溶解能力。
(3)图1为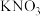 和
和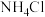 的溶解度曲线。
的溶解度曲线。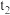 ℃时,分别将等质量的
℃时,分别将等质量的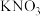 和
和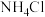 饱和溶液降温到
饱和溶液降温到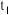 ℃,所得溶液的溶质质量分数:
℃,所得溶液的溶质质量分数: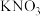
______ (填“<”。“>”或“=”)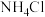 。
。
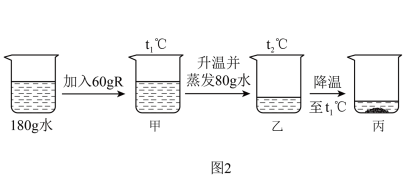
②根据以上信息,推测图2中的R是______ (填“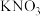 ”或“
”或“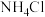 ”)。
”)。
③关于图2中烧杯内的物质,下列说法不正确的是______ (填字母)。
A.只有丙中上层清液是饱和溶液
B.要使丙中的固体溶解,可采用加水或升温的方法
C.甲、乙中,溶液的溶质质量相等
D.甲中溶液的溶质质量分数比丙中上层清液的溶质质量分数大
Ⅰ、配制溶质质量分数为24%的樟脑的酒精溶液。
Ⅱ、配制硝酸钾、氯化铵和水的混合溶液。
Ⅲ、将上述两种溶液混合装瓶,并密封。

(2)将樟脑的酒精饱和溶液滴入水中,出现了明显的浑浊,说明樟脑在水中的溶解能力
(3)图1为
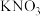 和
和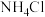 的溶解度曲线。
的溶解度曲线。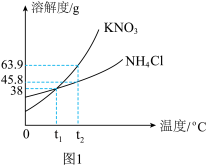
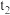 ℃时,分别将等质量的
℃时,分别将等质量的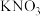 和
和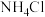 饱和溶液降温到
饱和溶液降温到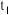 ℃,所得溶液的溶质质量分数:
℃,所得溶液的溶质质量分数: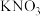
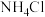 。
。②根据以上信息,推测图2中的R是
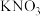 ”或“
”或“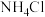 ”)。
”)。③关于图2中烧杯内的物质,下列说法不正确的是
A.只有丙中上层清液是饱和溶液
B.要使丙中的固体溶解,可采用加水或升温的方法
C.甲、乙中,溶液的溶质质量相等
D.甲中溶液的溶质质量分数比丙中上层清液的溶质质量分数大
您最近一年使用:0次
5 . 已知过氧化钠(Na2O2)与水的反应为2Na2O2+2H2O=4NaOH+O2↑,反应时放出大量的热。向一定量饱和的氢氧化钠溶液中加入少量的过氧化钠固体,已知氢氧化钠的溶解度随温度升高而增大。不考虑水的挥发、下列图像正确的个数有
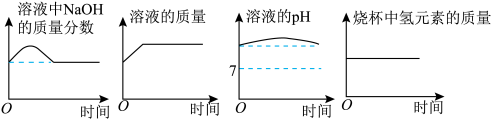
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
解题方法
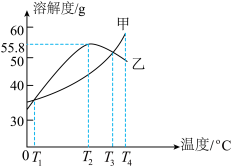
6 . 下列是MgSO4和KCl的溶解度表及溶解度曲线。下列说法不正确的是
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | |
| S/g | MgSO4 | 33.7 | 38.9 | 44.5 | 50.6 | 54.6 | 55.8 | 52.9 | 52.2 |
| KC1 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | 51.1 | 54.0 | |
| A.甲表示KCl的溶解度曲线 |
| B.将两物质的饱和溶液由T3℃降温至T2℃,有KCl晶体析出 |
| C.T2℃时,MgSO4饱和溶液溶质质量分数为55.8% |
| D.T4℃时,分别将等质量KCl和MgSO4固体溶于水配成饱和溶液,所得溶液质量前者小于后者 |
您最近一年使用:0次
2024-04-20更新
|
75次组卷
|
3卷引用:江苏省镇江市丹徒区上会中学2023-2024学年九年级下学期3月月考化学试题
解题方法
7 . 逻辑推理是一种重要的化学思维方法,以下推理正确的是
| A.活泼金属与酸反应能产生气体,能与酸反应产生气体的固体一定是活泼金属 |
| B.溶液有晶体析出时,溶液中溶质质量减小,则溶液的溶质质量分数一定减小 |
| C.碱性溶液中加入酚酞试液后显红色,加入酚酞试液后显红色的一定是碱性溶液 |
| D.同种元素的原子具有相同的质子数,所以质子数相同的粒子属于同种元素 |
您最近一年使用:0次
8 . 水是生命之源,可由多种途经获得水。
I、空气制水机能充分利用大气中的水分制出饮用水,其工作原理如下:______ (填“大于”或“小于”)滤孔直径的物质。
(2)②中需吸附色素和异味,常用的物质是______ 。
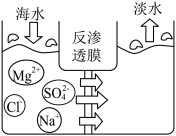
II、蒸馏法和膜分离法(下图)是两种常用的海水淡化方法。图中,加压后钠离子、镁离子等不能通过反渗透膜。______ (填“增大”、“减小”或“不变”)。
I、空气制水机能充分利用大气中的水分制出饮用水,其工作原理如下:

(2)②中需吸附色素和异味,常用的物质是
II、蒸馏法和膜分离法(下图)是两种常用的海水淡化方法。图中,加压后钠离子、镁离子等不能通过反渗透膜。
您最近一年使用:0次
解题方法
9 . 阅读科普短文,结合化学知识,回答下列问题。
②我国广西、贵州、云南、四川、重庆等地的大多数喀斯特地区,因高温多雨,地表难以达到碳酸钙的析出条件,钙华沉积通常发生在温度较低的地下,例如溶洞和地下暗河中,形成钟乳石、地下瀑布等景观。
③在较为寒冷的喀斯特地区,例如温带或者高山地区,钙华沉积则主要发生在地表。地表水在循环过程中因溶解岩石中的碳酸钙而含有较多的碳酸氢钙。雨季时节,水流变大、变快,水中的碳酸氢钙分解产生二氧化碳和碳酸钙(化学方程式为:Ca(HCO3)2=CaCO3↓+H2O+CO2↑)。其中的大部分二氧化碳被释放到空气中,部分被植物利用,参与光合作用;过饱和的碳酸钙则沉积下来,形成白色结晶。
(节选自《科学世界》第373期,有删改)
(1)根据第①段划线句子可知,钙华沉积时,地表水中_______ (填“能”或“不能”)继续溶解碳酸钙。
(2)请用简要文字解释第②段中“因高温多雨,地表难以达到碳酸钙的析出条件”的原因:_______ 。
(3)如表为不同温度时碳酸钙在水中的溶解度,则a_______ b(填“>”“<”或“=”)。
(4)综上,在25℃的温度下,地表水发生钙华沉积时,碳酸钙的质量分数为_______ (用含a的式子表示)。
(5)CO2能被植物利用,参与光合作用,还可用于_______ (写出一个合理答案即可)。
地表钙华沉积是瀑布形成的重要因素
①钙华沉积也称碳酸钙沉积。钙华是由于地表水中碳酸钙(CaCO3)过饱和而沉积形成的大空隙碳酸钙晶体。喀斯特地区因水中含有大量的碳酸钙而易发生钙华沉积。但是,由于受气候影响,不同喀斯特地区的钙华沉积可能发生在地下,也可能发生在地表。②我国广西、贵州、云南、四川、重庆等地的大多数喀斯特地区,因高温多雨,地表难以达到碳酸钙的析出条件,钙华沉积通常发生在温度较低的地下,例如溶洞和地下暗河中,形成钟乳石、地下瀑布等景观。
③在较为寒冷的喀斯特地区,例如温带或者高山地区,钙华沉积则主要发生在地表。地表水在循环过程中因溶解岩石中的碳酸钙而含有较多的碳酸氢钙。雨季时节,水流变大、变快,水中的碳酸氢钙分解产生二氧化碳和碳酸钙(化学方程式为:Ca(HCO3)2=CaCO3↓+H2O+CO2↑)。其中的大部分二氧化碳被释放到空气中,部分被植物利用,参与光合作用;过饱和的碳酸钙则沉积下来,形成白色结晶。
(节选自《科学世界》第373期,有删改)
(1)根据第①段划线句子可知,钙华沉积时,地表水中
(2)请用简要文字解释第②段中“因高温多雨,地表难以达到碳酸钙的析出条件”的原因:
(3)如表为不同温度时碳酸钙在水中的溶解度,则a
| 温度/℃ | 25 | 100 |
| 溶解度/g | a | b |
(5)CO2能被植物利用,参与光合作用,还可用于
您最近一年使用:0次
解题方法
10 . 如图为Na2CO3和NH4HCO3的溶解度曲线。下列说法正确的是
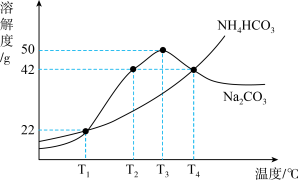
| A.T1℃时,将30gNH4HCO3加到50g水中,NH4HCO3完全溶解 |
| B.T2℃的Na2CO3饱和溶液升温到T3℃,溶质质量分数不变 |
| C.将100gNa2CO3溶液从T4℃降温到T1℃,一定析出Na2CO3晶体 |
| D.将T1℃的两物质饱和溶液升温到T4℃,为使溶液恰好饱和,加入两固体质量一定相等 |
您最近一年使用:0次



