解题方法
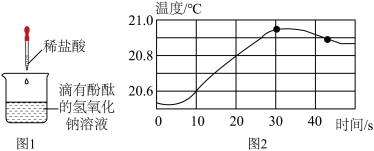
1 . 如图所示是化学兴趣小组的同学进行酸碱中和反应的实验研究。______ 。发生反应的化学方程式为______ 。
(2)在滴加实验结束后,为探究图1反应后烧杯中稀盐酸是否过量,可选用的试剂有______(填字母序号)。
(3)随着稀盐酸不断滴入,烧杯中溶液温度变化如坐标图2所示,根据图像可以判断该中和反应是______ (填“放热”或“吸热”)反应。
(2)在滴加实验结束后,为探究图1反应后烧杯中稀盐酸是否过量,可选用的试剂有______(填字母序号)。
| A.氢氧化钙溶液 | B.铜粉 | C.碳酸钙粉末 | D.硝酸银溶液 |
(3)随着稀盐酸不断滴入,烧杯中溶液温度变化如坐标图2所示,根据图像可以判断该中和反应是
您最近一年使用:0次
2 . 中和反应在日常生活和工农业生产中有广泛的应用。某实验小组在实验室探究氢氧化钠和盐酸的反应。
(1)向盛有5mL氢氧化钠溶液的烧杯中滴加几滴酚酞溶液,可观察到溶液变红。再向其中慢慢滴入稀盐酸,溶液变无色。
小组成员对于所加盐酸是否过量提出了疑问,于是对反应后溶液中溶质的成分作出猜想。
猜想一:NaCl
猜想二:___________ (填化学式)。
(2)为了验证其猜想,同学们进行如下探究。
(3)向氢氧化钠溶液中滴加稀盐酸时,有同学触摸到试管外壁,感觉有温度变化。小组利用温度传感器得出反应时间与溶液温度变化的关系(如图所示)。___________ 。
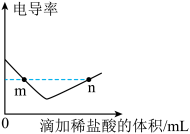
(4)查阅资料得知,在中和反应中溶液的导电性也发生变化。已知电导率是衡量溶液导电能力大小的物理量。在相同条件下,电导率与离子浓度(单位体积内的离子数)成正比。小组通过电导率传感器得出向氢氧化钠溶液中滴加稀盐酸过程中的电导率变化图像(如图所示)。___________ n点溶液中单位体积内离子数(填“>”“<”或“=”)。
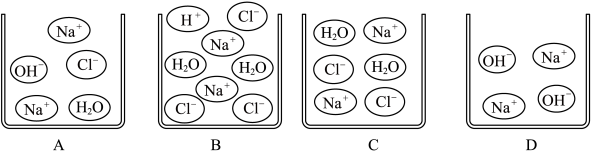
②如图表示该反应过程中不同时间点的微观粒子示意图,按时间先后排列的顺序为___________ (填序号)。
①从微观视角分析,酸碱中和反应的实质是:在溶液中,酸解离出的H+和碱解离出的___________ (填离子符号)结合生成水。
②要验证氢氧化钠溶液与稀盐酸混合后所得溶液中盐酸是否过量,除以上方法外,使用下列哪些物质也能达到目的?___________ (填序号)
A.硝酸银溶液 B.镁条 C.铜丝 D.pH试纸
(1)向盛有5mL氢氧化钠溶液的烧杯中滴加几滴酚酞溶液,可观察到溶液变红。再向其中慢慢滴入稀盐酸,溶液变无色。
小组成员对于所加盐酸是否过量提出了疑问,于是对反应后溶液中溶质的成分作出猜想。
猜想一:NaCl
猜想二:
(2)为了验证其猜想,同学们进行如下探究。
| 实验操作 | 实验现象 | 实验结论 |
| 取少量反应后的溶液,加入锌粒 | 猜想二正确,证明盐酸过量 |
(3)向氢氧化钠溶液中滴加稀盐酸时,有同学触摸到试管外壁,感觉有温度变化。小组利用温度传感器得出反应时间与溶液温度变化的关系(如图所示)。

(4)查阅资料得知,在中和反应中溶液的导电性也发生变化。已知电导率是衡量溶液导电能力大小的物理量。在相同条件下,电导率与离子浓度(单位体积内的离子数)成正比。小组通过电导率传感器得出向氢氧化钠溶液中滴加稀盐酸过程中的电导率变化图像(如图所示)。
②如图表示该反应过程中不同时间点的微观粒子示意图,按时间先后排列的顺序为
①从微观视角分析,酸碱中和反应的实质是:在溶液中,酸解离出的H+和碱解离出的
②要验证氢氧化钠溶液与稀盐酸混合后所得溶液中盐酸是否过量,除以上方法外,使用下列哪些物质也能达到目的?
A.硝酸银溶液 B.镁条 C.铜丝 D.pH试纸
您最近一年使用:0次
名校
解题方法
3 . 某兴趣小组对酸碱中和反应开展了项目式学习。
任务一:从能量变化角度探究酸和碱的反应。
某小组同学根据盐酸与氢氧化钠溶液反应过程中溶液温度升高得出两者能反应的结论。某同学认为此结论不够严谨。该同学在室温下借助传感器设计了以下实验:
①10mL、20%的盐酸与 蒸馏水混合,测量溶液温度的变化;
蒸馏水混合,测量溶液温度的变化;
② 、20%的氢氧化钠溶液与
、20%的氢氧化钠溶液与 蒸馏水混合,测量溶液温度的变化;
蒸馏水混合,测量溶液温度的变化;
③10mL、20%的盐酸与10mL、20%的氢氧化钠溶液混合,测量溶液温度的变化。
三个实验中溶液温度随时间变化的关系如图1所示。
(1)该同学设计实验①②的原因是________ 也可能有温度升高的现象;
(2)基于实验①②③,说明氢氧化钠和盐酸发生了反应的证据是________ ;
(3)写出氢氧化钠和盐酸反应的化学方程式________ ;
[查阅资料]相同状况下,单位体积的溶液中离子数目相同,电导率相同,离子越多,电导率越大。向一定体积的氢氧化钠溶液中滴加电导率相同的盐酸,测得电导率变化情况如图2所示。
(4)结合资料解释mn段曲线下降的原因________(填字母);
(5)判断n点溶液呈________ 性(填“酸”、“碱”或“中”);
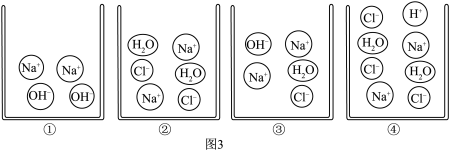
(6)用图3表示上述反应过程中,溶液中微观粒子的变化储况(氢氧化钠溶液和稀盐酸中的水分子在图中未体现),按时间先后排列的顺序为________ (填数字序号);
(7)电导率相同的盐酸和氢氧化钠溶液的溶质质量分数之比是否为36.5:40?请你给出判断并说明理由________ ;
任务三:探究中和反应中溶液 的变化。
的变化。
取三份相同体积相同浓度的氢氧化钠溶液,分别滴入两滴无色酚酞溶液,再以相同的速度同时滴加不同浓度的盐酸,得到溶液的 随时间变化的曲线如图4。
随时间变化的曲线如图4。________ ,溶液红色最先褪去的是________ 。
任务一:从能量变化角度探究酸和碱的反应。
某小组同学根据盐酸与氢氧化钠溶液反应过程中溶液温度升高得出两者能反应的结论。某同学认为此结论不够严谨。该同学在室温下借助传感器设计了以下实验:
①10mL、20%的盐酸与
 蒸馏水混合,测量溶液温度的变化;
蒸馏水混合,测量溶液温度的变化;②
 、20%的氢氧化钠溶液与
、20%的氢氧化钠溶液与 蒸馏水混合,测量溶液温度的变化;
蒸馏水混合,测量溶液温度的变化;③10mL、20%的盐酸与10mL、20%的氢氧化钠溶液混合,测量溶液温度的变化。
三个实验中溶液温度随时间变化的关系如图1所示。
(1)该同学设计实验①②的原因是
(2)基于实验①②③,说明氢氧化钠和盐酸发生了反应的证据是
(3)写出氢氧化钠和盐酸反应的化学方程式


[查阅资料]相同状况下,单位体积的溶液中离子数目相同,电导率相同,离子越多,电导率越大。向一定体积的氢氧化钠溶液中滴加电导率相同的盐酸,测得电导率变化情况如图2所示。
(4)结合资料解释mn段曲线下降的原因________(填字母);
| A.反应过程中离子数目减少 | B.反应过程中离子数目不变 |
| C.反应过程中溶液体积增大 | D.反应过程中溶液体积不变 |
(5)判断n点溶液呈
(6)用图3表示上述反应过程中,溶液中微观粒子的变化储况(氢氧化钠溶液和稀盐酸中的水分子在图中未体现),按时间先后排列的顺序为
(7)电导率相同的盐酸和氢氧化钠溶液的溶质质量分数之比是否为36.5:40?请你给出判断并说明理由
任务三:探究中和反应中溶液
 的变化。
的变化。取三份相同体积相同浓度的氢氧化钠溶液,分别滴入两滴无色酚酞溶液,再以相同的速度同时滴加不同浓度的盐酸,得到溶液的
 随时间变化的曲线如图4。
随时间变化的曲线如图4。
您最近一年使用:0次
解题方法
4 . 进行如下实验,研究氢氧化钙的性质,下列说法不正确的是
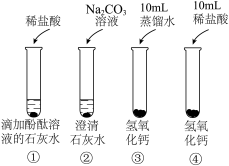
| A.①中溶液颜色变为无色,说明稀盐酸已过量 |
| B.②中生成白色沉淀,实验室可以采用该反应制取NaOH |
| C.③中试管底部有白色固体残留,说明氢氧化钙在水中的溶解度比较小 |
| D.④中反应后溶液温度升高,说明氢氧化钙与稀盐酸反应发热 |
您最近一年使用:0次
真题
解题方法
5 . 用 溶液与稀硫酸进行中和反应实验,开始时滴入几滴酚酞溶液,测得溶液的pH变化如下图所示。下列说法不正确的是
溶液与稀硫酸进行中和反应实验,开始时滴入几滴酚酞溶液,测得溶液的pH变化如下图所示。下列说法不正确的是
 溶液与稀硫酸进行中和反应实验,开始时滴入几滴酚酞溶液,测得溶液的pH变化如下图所示。下列说法不正确的是
溶液与稀硫酸进行中和反应实验,开始时滴入几滴酚酞溶液,测得溶液的pH变化如下图所示。下列说法不正确的是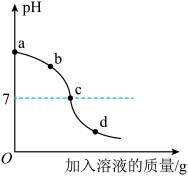
A.图像表明是向 溶液中加入稀硫酸 溶液中加入稀硫酸 |
| B.ac段溶液颜色逐渐变浅,d点溶液为无色 |
| C.d点溶液钠元素质量分数大于b点溶液钠元素质量分数 |
| D.ac段溶液升温明显高于cd段,说明该反应放出热量 |
您最近一年使用:0次
解题方法
6 . 聂同学利用pH传感器和温度传感器研究氢氧化钠和稀盐酸反应过程,装置如图1,得到图2的数据关系。下列说法不正确的是

| A.该实验是将稀盐酸滴入氢氧化钠溶液 |
| B.图2中d点只有一种溶质 |
| C.图2中c→d所示溶液NaCl质量不再增加 |
| D.温度传感器可在反应过程中检测到温度上升 |
您最近一年使用:0次
2024·山西·模拟预测
7 . 实验是培养创新意识和实践能力的有效途径。若用下图所示装置进行实验,下列说法中正确的是

| A.该装置可证明硝酸铵溶于水吸热 |
| B.该装置可证明CO2与NaOH反应 |
| C.用该装置进行中和反应,气球会变大 |
| D.用该装置进行铁粉和稀盐酸的反应,气球会变大 |
您最近一年使用:0次
2024·山东济南·模拟预测
解题方法
8 . 根据下列实验事实得出的结论错误的是
| 选项 | 实验事实 | 结论 |
| A | 将NaOH固体与稀盐酸混合,测得溶液温度升高 | 中和反应放出热量 |
| B | 将铁丝和铜丝分别伸入等浓度的稀盐酸中,铁丝表面有气泡产生,铜丝表面无变化 | 铁的金属活动性比铜强 |
| C | 50mL水和50mL酒精混合后的总体积小于100mL | 分子间存在间隔 |
| D | 潮湿的环境中铁容易生锈,干燥的环境中铁不生锈 | 水是铁锈蚀需要的条件之一 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . “学化学,爱化学,用好化学”兴趣小组的同学围绕“酸碱中和反应”开展实验探究活动,请你参与下列活动。
【实验探究】将氢氧化钾溶液与稀硫酸混合,观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。
甲同学在实验过程中测得pH变化如图1所示,则该同学是将______ (填字母序号)。
a.氢氧化钾溶液滴入稀硫酸中 b.稀硫酸滴入氢氧化钾溶液中
(2)测混合过程中的温度变化。乙同学在实验过程中测得反应混合溶液的温度变化如图2所示,其中B点溶液中的溶质有___________ 。
(3)借助于酸碱指示剂
丙同学通过图3所示实验,他观察到溶液由红色变成无色,也证明氢氧化钾溶液与稀硫酸发生了化学反应,反应的化学方程式为_____________ 。
【提出问题】针对反应后溶液中溶质的成分,大家纷纷提出了猜想。
【猜想与假设】
猜想一:只有K2SO4;猜想二:有K2SO4和H2SO4;猜想三:有K2SO4和KOH
【进行实验】
(4)为了验证猜想,学习小组选用Fe2O3粉末、BaCl2溶液,进行如下探究:
【实验结论】通过探究,同学们一致确定猜想二是正确的。
【评价与反思】
(5)丁同学针对上述方案提出疑问,认为方案二是不合理的,理由是_________ 。
(6)同学们经过反思与讨论,最后认为方案一中的Fe2O3粉末可以用某些物质代替,也能得到同样的实验结论,请你选出下列的不可用来代替Fe2O3药品的字母序号________。
【实验探究】将氢氧化钾溶液与稀硫酸混合,观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。

甲同学在实验过程中测得pH变化如图1所示,则该同学是将
a.氢氧化钾溶液滴入稀硫酸中 b.稀硫酸滴入氢氧化钾溶液中
(2)测混合过程中的温度变化。乙同学在实验过程中测得反应混合溶液的温度变化如图2所示,其中B点溶液中的溶质有
(3)借助于酸碱指示剂
丙同学通过图3所示实验,他观察到溶液由红色变成无色,也证明氢氧化钾溶液与稀硫酸发生了化学反应,反应的化学方程式为
【提出问题】针对反应后溶液中溶质的成分,大家纷纷提出了猜想。
【猜想与假设】
猜想一:只有K2SO4;猜想二:有K2SO4和H2SO4;猜想三:有K2SO4和KOH
【进行实验】
(4)为了验证猜想,学习小组选用Fe2O3粉末、BaCl2溶液,进行如下探究:
| 实验方案 | 实验操作 | 实验现象 | 实验结论 |
| 方案一 | 取少量反应后的溶液于试管中,加入Fe2O3粉末 | 溶液中有H2SO4,猜想二正确 | |
| 方案二 | 取少量反应后的溶液于试管中,滴加BaCl2溶液 | 产生白色沉淀 | 溶液中有H2SO4,猜想二正确 |
【实验结论】通过探究,同学们一致确定猜想二是正确的。
【评价与反思】
(5)丁同学针对上述方案提出疑问,认为方案二是不合理的,理由是
(6)同学们经过反思与讨论,最后认为方案一中的Fe2O3粉末可以用某些物质代替,也能得到同样的实验结论,请你选出下列的不可用来代替Fe2O3药品的字母序号________。
| A.Mg | B.CuO | C.KCl | D.Na2CO3 |
您最近一年使用:0次
解题方法
10 . 下列实验基本操作,错误的是
A.连接仪器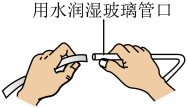 |
B.用托盘天平称取NaOH固体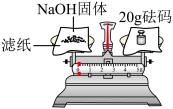 |
C.探究中和反应的能量变化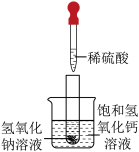 |
D.检查装置的气密性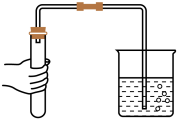 |
您最近一年使用:0次



