名校
1 . 某学生设计了下图所示的四套装置来制取CO2,其中在制取时不能使反应随时发生或停止的装置为( )
A.  | B.  |
C.  | D. 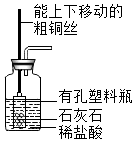 |
您最近一年使用:0次
名校
2 . 有下列装置,其中A是气体发生装置,B、C、D是气体收集装置,E、F还可作气体的净化装置。
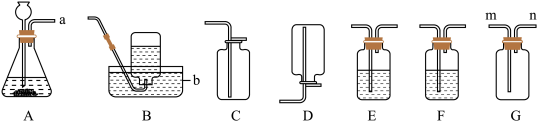
(1)仪器b的名称为___________ 。
(2)当用大理石和稀盐酸制取CO2时,反应的化学方程式为___________ ,选取的收集装置是 ___________ (填“B”“C”或“D”)。为了得到纯净、干燥的CO2,需将气体依次通过E→F装置,应在E装置中注入 ___________ 溶液,F装置中试剂的作用是 ___________ 。
(3)当用过氧化氢溶液和二氧化锰来制取氧气时,A中发生反应的化学方程式为___________ ,若a与n相连来收集氧气,还需将装置G ___________ 。

(1)仪器b的名称为
(2)当用大理石和稀盐酸制取CO2时,反应的化学方程式为
(3)当用过氧化氢溶液和二氧化锰来制取氧气时,A中发生反应的化学方程式为
您最近一年使用:0次
21-22九年级上·浙江·期末
3 . 食用级碳酸钙广泛应用于现代保健食品行业,是奶制品、肉制品和面制品等行业的优质营养强化添加剂。已知食用级碳酸钙中往往会含有少量杂质,且杂质不与酸反应。小明为测定某品牌食用级碳酸钙中碳酸钙的的含量,利用气密性良好的图甲装置进行实验:①称取样品6克,加入锥形瓶中,塞紧瓶塞,从左侧持续缓慢鼓入空气;②一段时间后打开分液漏斗活塞,缓慢注入足量的稀盐酸,并开始计时;③待装置D总质量不再增加时停止鼓入空气。实验过程中测得装置D增加的质量随时间变化图像如图乙所示。(碳酸钙与盐酸反应的化学方程式为: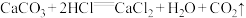 )
)

(1)实验前,要先鼓入空气的目的是______ 。
(2)根据图乙,计算该石灰石样品中碳酸钙的质量分数。(计算结果精确到0.1%)______
(3)下列情况中,会导致测得的碳酸钙质量分数偏大的是______ (可多选)
①去掉装置A,将空气直接鼓入装置B②去掉装置C,将B与D装置直接相连
③当气泡停止产生时立即停止鼓入空气④将稀盐酸快速注入锥形瓶中与样品反应
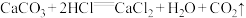 )
)
(1)实验前,要先鼓入空气的目的是
(2)根据图乙,计算该石灰石样品中碳酸钙的质量分数。(计算结果精确到0.1%)
(3)下列情况中,会导致测得的碳酸钙质量分数偏大的是
①去掉装置A,将空气直接鼓入装置B②去掉装置C,将B与D装置直接相连
③当气泡停止产生时立即停止鼓入空气④将稀盐酸快速注入锥形瓶中与样品反应
您最近一年使用:0次
4 . 学了物质及其变化后,同学们利用装修后剩下的大理石碎片进行相关实验。

(1)一位同学设计了装置A制取CO2,该装置能通过上下移动穿过橡胶塞的粗铜丝来控制反应的发生或停止。大理石碎片应放在______ 中。根据气体制备的一般原则,A中的粗铜丝能否用铁丝代替______ (填“能”或“不能”),原因是______ 。
(2)浓H2 SO4 具有强烈的吸水性,可作为干燥剂除去某些气体中的水分。如用装置B干燥CO2,则CO2应从______ (填字母)端口通入。
(3)如用装置C收集CO2,则CO2应从______ (填字母)端口通入。
(4)装置D用于通入CO2将水压入量筒中以测量CO2的体积,植物油的作用是______ 。D中液体未装满,对测量CO2气体的体积有无影响______ (填“有”或“无”)

(1)一位同学设计了装置A制取CO2,该装置能通过上下移动穿过橡胶塞的粗铜丝来控制反应的发生或停止。大理石碎片应放在
(2)浓H2 SO4 具有强烈的吸水性,可作为干燥剂除去某些气体中的水分。如用装置B干燥CO2,则CO2应从
(3)如用装置C收集CO2,则CO2应从
(4)装置D用于通入CO2将水压入量筒中以测量CO2的体积,植物油的作用是
您最近一年使用:0次
名校
5 . 某化学兴趣小组为测定大理石中碳酸钙的含量,进行如图1所示实验:将过量的稀盐酸加入20 g大理石中(其他成分不与盐酸反应),把产生的CO2气体用足量的烧碱溶液吸收,同时测量C瓶烧碱溶液增加的质量,结果如下表所示:
(1)计算大理石样品中碳酸钙的质量分数。(要写计算过程)
(2)请在如图的坐标纸上,以时间为横坐标,以产生CO2气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线。
(3)B中所装药品为碳酸氢钠溶液,作用是吸收挥发出的HCl气体,该装置使测量结果___________(填“偏大”、“偏小”或“没有影响”)。
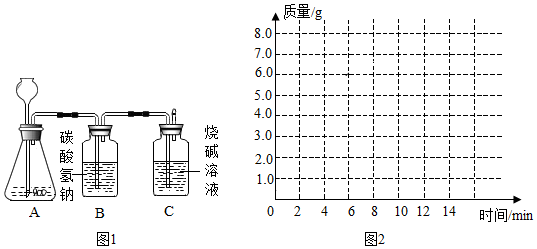
| 时间/分 | 0 | 2 | 4 | 6 | 8 | 10 |
| C瓶溶液增加的质量/g | 0 | 3.0 | 5.0 | 6.0 | 6.6 | 6.6 |
(1)计算大理石样品中碳酸钙的质量分数。(要写计算过程)
(2)请在如图的坐标纸上,以时间为横坐标,以产生CO2气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线。
(3)B中所装药品为碳酸氢钠溶液,作用是吸收挥发出的HCl气体,该装置使测量结果___________(填“偏大”、“偏小”或“没有影响”)。

您最近一年使用:0次
6 . 为测定某钙片中碳酸钙的质量分数(钙片中其他成分不参与反应),小乐取10g钙片研磨后,进行了如图所示的实验(忽略水分蒸发)。回答下列问题:

(1)研磨钙片的目的是________ 。该实验中,装置的气密性对测定结果________ (选填“有”或“无”)影响。
(2)计算该钙片中碳酸钙的质量分数________ 。(写出计算过程)。

(1)研磨钙片的目的是
(2)计算该钙片中碳酸钙的质量分数
您最近一年使用:0次
7 . 小乐利用如图所示装置和药品进行相关气体的制取实验(部分固定装置已省略),据图回答问题:
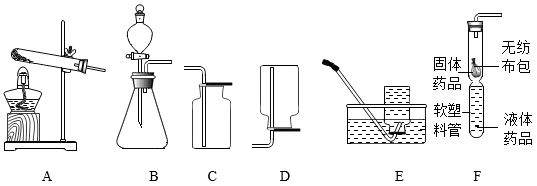
(1)若小乐选择装置A制取氧气,则装置A试管中发生反应的化学方程式为________ ,若小乐选择装置E收集了一瓶氧气,测得氧气的纯度偏低,原因可能是________ (选填序号)。
①收集气体前,集气瓶中没有注满水
②导管口刚有气泡冒出,就立刻收集
③收集气体后,集气瓶中仍有少量水
④收集气体后,集气瓶正放在桌面上
(2)实验室制取并收集二氧化碳的装置为________ (从装置A~E中选填),小乐尝试用装置F制取二氧化碳,简要描述操作过程:________ 。

(1)若小乐选择装置A制取氧气,则装置A试管中发生反应的化学方程式为
①收集气体前,集气瓶中没有注满水
②导管口刚有气泡冒出,就立刻收集
③收集气体后,集气瓶中仍有少量水
④收集气体后,集气瓶正放在桌面上
(2)实验室制取并收集二氧化碳的装置为
您最近一年使用:0次
8 . 小科同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如表所示:
试求:
(1)m的值为___________。
(2)12g石灰石样品中碳酸钙的质量等于___________g
(3)反应完全后最终溶液中氯化钙的质量分数?(写出计算过程)
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 生成气体的总质量/g | 1.1 | 2.2 | m | 4.4 | 4.4 |
试求:
(1)m的值为___________。
(2)12g石灰石样品中碳酸钙的质量等于___________g
(3)反应完全后最终溶液中氯化钙的质量分数?(写出计算过程)
您最近一年使用:0次
名校
9 . 小明同学要测定某大理石样品中碳酸钙的质量分数,决定取一定量的大理石粉末与稀盐酸反应测量生成二氧化碳的质量来完成实验,并设计了两个实验方案(假设二氧化碳全部从溶液中逸出,不考虑盐酸挥发和水的蒸发,杂质不参与化学反应)。
【方案一】用下图装置实验可计算出生成二氧化碳的质量。
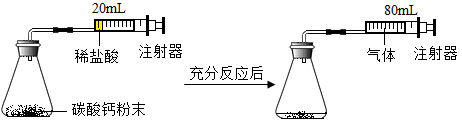
(1)在检查图装置气密性时,小明用双手捧住锥形瓶容器一段时间后再放开,若出现___________ 的现象,则证明气密性良好。
(2)针对以上方案一,下列分析正确的有___________ (填字母编号)。
A.通过测定CO2的体积可计算CO2的质量
B.共生成了80 mL CO2气体
C.注射器中收集到的是纯净的CO2气体
D.反应前后整个装置的质量不变
(3)若实验中外界大气压变大,将导致实验得到的碳酸钙的质量分数比实际值偏___________
(4)若该人理石样品中碳酸钙的质量分数为80%,则图三中天平示数m的值为多少g___________ 。(写出计算过程,CaCO3+2HCl=CaCl2+CO2↑+H2O)

【方案一】用下图装置实验可计算出生成二氧化碳的质量。

(1)在检查图装置气密性时,小明用双手捧住锥形瓶容器一段时间后再放开,若出现
(2)针对以上方案一,下列分析正确的有
A.通过测定CO2的体积可计算CO2的质量

B.共生成了80 mL CO2气体
C.注射器中收集到的是纯净的CO2气体
D.反应前后整个装置的质量不变
(3)若实验中外界大气压变大,将导致实验得到的碳酸钙的质量分数比实际值偏
(4)若该人理石样品中碳酸钙的质量分数为80%,则图三中天平示数m的值为多少g

您最近一年使用:0次
2021-11-07更新
|
333次组卷
|
2卷引用:浙江省温州市平阳新纪元学校2021-2022学年九年级10月月考科学试题
10 . 听说墨鱼骨能治疗胃酸过多,好学的小科和小妍想探个究竟。查阅资料,墨鱼骨含碳酸钙70%~85%以上,还含有多种氨基酸(有机物在高温条件下易分解)。为了测定墨鱼骨中碳酸钙的含量,他们先将墨鱼骨洗净晒干,并按各自设计实验方法进行研究。
(1)小科称取10克洗净晒干的墨鱼骨,高温灼烧至质量不变,冷却后称得剩余固体质量为5.4克,处理如下:
CO2 质量=10克-5.4克=4.6克
设碳酸钙质量为M


所以M = 10.5克
CaCO3% =10.5克÷10克×100%=105%
小科的计算结果与事实不符,产生错误的原因是:___________。
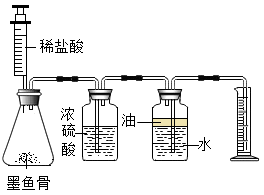
(2)小研用如图所示的实验装置进行实验,其中浓硫酸的作用是___________。
(3)小妍将30mL稀盐酸分3次加入5克样品中,每次加入盐酸后充分反应,待量筒内的水的体积不再变化时,读出水的体积,结果见下表。已知本实验条件下CO2的密度为2.0克/升,求:该墨鱼骨粉样品中CaCO3的质量分数。

(1)小科称取10克洗净晒干的墨鱼骨,高温灼烧至质量不变,冷却后称得剩余固体质量为5.4克,处理如下:
CO2 质量=10克-5.4克=4.6克
设碳酸钙质量为M


所以M = 10.5克
CaCO3% =10.5克÷10克×100%=105%
小科的计算结果与事实不符,产生错误的原因是:___________。
(2)小研用如图所示的实验装置进行实验,其中浓硫酸的作用是___________。
(3)小妍将30mL稀盐酸分3次加入5克样品中,每次加入盐酸后充分反应,待量筒内的水的体积不再变化时,读出水的体积,结果见下表。已知本实验条件下CO2的密度为2.0克/升,求:该墨鱼骨粉样品中CaCO3的质量分数。
| 第一次 | 第二次 | 第三次 | |
| 加入稀盐酸的体积(毫升) | 10 | 10 | 10 |
| 进入量筒内水的体积(毫升) | 330 | 660 | 880 |
您最近一年使用:0次



