1 . 元素周期表揭示了元素间的内在联系,使元素构成了一个较为系统的体系;元素周期表的建立成为化学发展史上的重要里程碑。下图是元素周期表的一部分,表中所列字母a、b、c、d、e、f、g分别代表某种化学元素。请依据这7种元素回答下列问题:
(1)上述7种元素中金属性最强的是___________ (用元素符号表示)。
(2)g在周期表中的位置是___________ ,其最高价氧化物对应的水化物的化学式为___________ 。
(3)a、c两元素形成的含有非极性共价键的化合物的电子式为___________ 。
(4)c、d、e、f简单离子半径由小到大的顺序是___________ (用离子符号表示)。
(5)b、c两元素形成的简单氢化物中稳定性最强的是________ (填化学式)。
(6)富硒酵母是一种新型添加剂,硒 元素与c同主族,则还原性:
元素与c同主族,则还原性:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(7)b、c、d三元素形成的正盐溶液呈___________ (填“碱性”“中性”或“酸性”),向其溶液中通入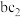 所发生反应的离子方程式为
所发生反应的离子方程式为___________ 。
| a | |||||||||||||||||
| b | c | ||||||||||||||||
| d | e | f | g | ||||||||||||||
(2)g在周期表中的位置是
(3)a、c两元素形成的含有非极性共价键的化合物的电子式为
(4)c、d、e、f简单离子半径由小到大的顺序是
(5)b、c两元素形成的简单氢化物中稳定性最强的是
(6)富硒酵母是一种新型添加剂,硒
 元素与c同主族,则还原性:
元素与c同主族,则还原性:
 (填“>”或“<”)。
(填“>”或“<”)。(7)b、c、d三元素形成的正盐溶液呈
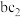 所发生反应的离子方程式为
所发生反应的离子方程式为
您最近一年使用:0次
名校
2 . 探究是培养创新精神和实践能力的手段。用如下装置探究氯气的性质,图中三支试管口均放置浸有NaOH溶液的棉花。下列对实验现象的分析错误的是
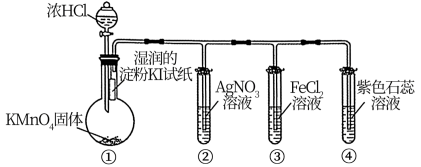

| A.①中淀粉KI试纸变蓝,说明氯气的氧化性强于碘 |
| B.②中产生白色沉淀,说明氯气与水反应生成Cl— |
| C.③中的溶液变为棕黄色,说明氯气有氧化性 |
| D.④溶液先变红后褪色,说明氯水有酸性和漂白性 |
您最近一年使用:0次
2021-03-18更新
|
5172次组卷
|
27卷引用:重庆市西南大学附中2020-2021学年高三下学期第四次月考化学试题
重庆市西南大学附中2020-2021学年高三下学期第四次月考化学试题重庆市育才中学校2022-2023学年高一上学期期中考试化学试题广东省广州市2021届高三3月第一次模拟考试化学试题广东省广州市2021届高三下学期毕业班综合测试(一)化学试题(已下线)第四章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测(已下线)第9周 周测卷-备战2022年高考化学周测与晚练(新高考专用)(已下线)专题07 非金属及其化合物-2022年高考化学二轮复习重点专题常考点突破练广东省广州市三校2021-202学年高一上学期期末联考化学试题福建省厦门市同安第一中学2021-2022学年高一下学期第一次月考(3月)化学试题(已下线)第12讲 富集在海水中的元素——卤素(练)-2023年高考化学一轮复习讲练测(全国通用)第二节 氯及其化合物 第2课时 氯气的实验室制法及氯离子的检验江西省赣州市赣县第三中学2023届高三上学期月考强化训练(B8)化学试题辽宁省北镇市满族高级中学2022-2023学年高三上学期第一次质量检测化学试题广东省广州市海珠外国语实验中学2022-2023学年高一上学期第二次月考化学试题河南省安阳市第一中学2022-2023学年高一上学期12月月考化学试题山东省临沂第一中学文峰校区2022-2023学年高一上学期期末考试化学试题四川省成都市树德中学2022-2023学年高一上学期期末复习化学试题福建省尤溪县第七中学2022-2023学年高一下学期第一次阶段检测化学试题湖南省永州市第一中学2022-2023学年高一上学期期末考试化学试题 河南大学附属中学2022-2023学年高一下学期第一次月考化学试题湖南师范大学附属中学2023-2024学年高一上学期期中考试化学试题天津市双菱中学2023-2024学年高一上学期期中考试化学试卷陕西省西安市长安区第一中学2023-2024学年高一上学期期中考试化学试题河北省邯郸市涉县第一中学2023-2024学年高一上学期12月月考 化学试卷四川省成都市成华区某校2023-2024学年高一上学期12月月考化学试题湖南省长沙市雅礼中学2023-2024学年高三上学期一模化学试题黑龙江省哈尔滨市宾县第二中学2023-2024学年高一上学期第三次月考化学试题
名校
3 . 某同学设计完成了以下两个实验:
①向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色(生成了HIO3)。
②向盛有KBr溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成红棕色。继续向试管中滴加氯水,振荡,CCl4层的颜色没有变化。
下列说法不正确的是
①向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色(生成了HIO3)。
②向盛有KBr溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成红棕色。继续向试管中滴加氯水,振荡,CCl4层的颜色没有变化。
下列说法不正确的是
| A.实验①生成HIO3时发生的反应为:I2+5Cl2+6H2O=2HIO3+10HCl |
| B.实验②中当CCl4层变成红棕色时可通过分液的方法获得Br2的CCl4溶液 |
| C.由上述实验得出Cl2、Br2、I2的氧化性由强到弱的顺序是:Cl2>Br2>I2 |
| D.由上述实验得出Cl2、HIO3、HBrO3氧化性由强到弱的顺序是:HBrO3>Cl2>HIO3 |
您最近一年使用:0次
2017-02-17更新
|
872次组卷
|
8卷引用:重庆市第八中学校2021-2022学年高三上学期期中考试化学试题
重庆市第八中学校2021-2022学年高三上学期期中考试化学试题2017届北京市丰台区高三上学期期末化学试卷北京市第十中学2019届高三第一学期10月月考化学试题【全国百强校】河南省信阳高级中学2018-2019学年高一上学期期末考试化学试题【全国百强校】河北省武邑中学2018-2019学年高一下学期开学考试化学试题(已下线)第6单元 常见的非金属元素(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷河南省洛阳市第一高级中学2021届高三9月月考化学试题(已下线)BBWYhjhx1004.pdf
名校
解题方法
4 . Al与NaOH的水溶液能反应,而镁不反应。然而一位同学将镁条放入饱和碳酸氢钠溶液时,却观察到反应迅速发生,且有大量气体放出。查阅资料显示:①镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物;②Mg与沸水能明显发生反应。为探究反应原理,同学们设计了如下实验方案并验证产物。
【实验I】:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红。
(1)提出假设
该同学对反应中产生的白色不溶物作出如下猜测:
猜测1:可能是_______ 。
猜测2:可能是 。
。
猜测3:可能是碱式碳酸镁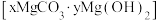 。
。
(2)设计定性实验确定产物并验证猜测:
(3)设计定量实验确定实验I的产物:称取实验I中所得干燥、纯净的白色不溶物31.0g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验前后装置A增重1.8g,装置B增重13.2g,试确定白色不溶物的化学式_______ 。
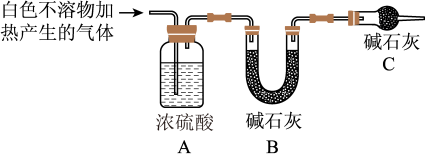
(4)根据资料显示以及实验现象,有同学认为,上述反应可能就是镁分别与水、与碳酸氢钠两个直接反应的共同结果。请你分别写出这两个可能发生的化学反应的化学方程式:_______ ,_______ 。
【实验I】:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红。
(1)提出假设
该同学对反应中产生的白色不溶物作出如下猜测:
猜测1:可能是
猜测2:可能是
 。
。猜测3:可能是碱式碳酸镁
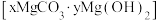 。
。(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 预期现象和结论 |
| 【实验II】 | 将实验I中收集的气体点燃 | 现象及结论 |
| 【实验III】 | 取实验I中的白色不溶物,洗涤,加入足量 |  |
| 【实验IV】 | 取实验I中的滤液,向其中加入BaCl2稀溶液 | 产生白色沉淀;溶液中存在 |

(4)根据资料显示以及实验现象,有同学认为,上述反应可能就是镁分别与水、与碳酸氢钠两个直接反应的共同结果。请你分别写出这两个可能发生的化学反应的化学方程式:
您最近一年使用:0次
2023-01-12更新
|
367次组卷
|
2卷引用:重庆市南开中学2022-2023学年高一上期期末考试化学试题
解题方法
5 . 铜、铁及其化合物在工业、农业、科技和日常生活中有广泛应用。
(1)工业上利用辉铜矿(主要成分是Cu2S)冶炼铜。为了测定辉铜矿样品的纯度,用酸性高锰酸钾溶液反应(已知1 molCu2S失去10mol的电子),写出该反应的离子方程式____________________________ 。
(2)工业上利用废铜屑、废酸(含硝酸、硫酸)为主要原料制备硫酸铜晶体。某含有c(HNO3)="2" mol·L—1,c(H2SO4)="4" mol·L—1的废酸混合液100 mL(不含其它酸或氧化剂),最多能制备硫酸铜晶体(CuSO4·5H2O)的质量为______________ 。
(3)现有一块含有铜绿的铜片(假设不含其它杂质)在空气中灼烧至完全反应,经测定,反应前后固体的质量相同。(已知:金属生锈率= )
)
①上述铜片中铜的生锈率为________________ (结果保留2位有效数字)
②固态铜与适量氧气反应,能量变化如下图所示,写出固态铜与氧气反应生成1 mol固态氧化亚铜的热化学方程式____________________________ 。

(4)高铁酸盐在能源环保等领域有广泛用途,如高铁酸钾(K2FeO4) 因有强氧化性,能杀菌消毒,产生Fe(OH)3有吸附性,是一种新型净水剂,用如下图所示的装置可以制取少量的高铁酸钾。
(已知爱迪生蓄电池的反应式为: )
)

①爱迪生蓄电池的负极材料是______________________
②写出制取高铁酸钾阳极的电极反应式______________________
③当生成19.8g的K2FeO4时,隔膜两侧电解液的质量变化差(△m右一△m左)为______________ g。
(1)工业上利用辉铜矿(主要成分是Cu2S)冶炼铜。为了测定辉铜矿样品的纯度,用酸性高锰酸钾溶液反应(已知1 molCu2S失去10mol的电子),写出该反应的离子方程式
(2)工业上利用废铜屑、废酸(含硝酸、硫酸)为主要原料制备硫酸铜晶体。某含有c(HNO3)="2" mol·L—1,c(H2SO4)="4" mol·L—1的废酸混合液100 mL(不含其它酸或氧化剂),最多能制备硫酸铜晶体(CuSO4·5H2O)的质量为
(3)现有一块含有铜绿的铜片(假设不含其它杂质)在空气中灼烧至完全反应,经测定,反应前后固体的质量相同。(已知:金属生锈率=
 )
)①上述铜片中铜的生锈率为
②固态铜与适量氧气反应,能量变化如下图所示,写出固态铜与氧气反应生成1 mol固态氧化亚铜的热化学方程式

(4)高铁酸盐在能源环保等领域有广泛用途,如高铁酸钾(K2FeO4) 因有强氧化性,能杀菌消毒,产生Fe(OH)3有吸附性,是一种新型净水剂,用如下图所示的装置可以制取少量的高铁酸钾。
(已知爱迪生蓄电池的反应式为:
 )
)
①爱迪生蓄电池的负极材料是
②写出制取高铁酸钾阳极的电极反应式
③当生成19.8g的K2FeO4时,隔膜两侧电解液的质量变化差(△m右一△m左)为
您最近一年使用:0次
解题方法
6 . I.由硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、Al2O3和SiO2)得到绿矾(FeSO4·7H2O),然后制取透明氧化铁颜料的流程如下:
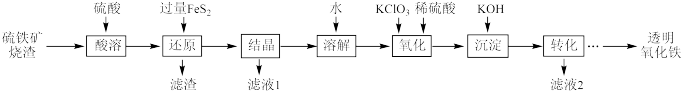
已知:①透明氧化铁又称纳米氧化铁,粒子直径微小(10~90nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
②Fe3+能将FeS2中的硫元素氧化为+6价。
回答下列问题:
(1)FeS2的电子式为___________ 。
(2)“滤渣”中的主要成分是___________ 。
(3)“还原”过程中涉及的离子方程式为___________ 。
(4)流程中“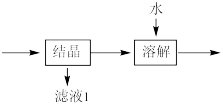 ”环节的目的是
”环节的目的是___________ 。
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到色泽纯正的氢氧化铁,而且还可以___________ 。
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示:
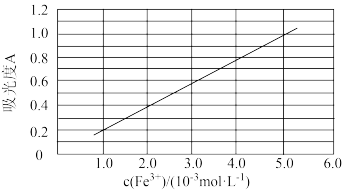
称取3.47g透明氧化铁,用稀硫酸溶解并定容至1L,准确移取该溶液10.00mL,加入足量KSCN溶液,再用蒸馏水定容至100mL。测得溶液吸光度A=0.8,则透明氧化铁中氧化铁红(Fe2O3)的质量分数为___________ %(保留小数点后一位)。
Ⅱ.氧化亚铜(Cu2O)用途广泛,干法生产Cu2O粉末的主要工艺流程如下:
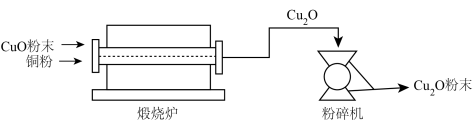
(7)粉碎机中,发生的变化属于___________ (填“物理变化”或“化学变化”)。
(8)800~900℃时,煅烧炉中发生化合反应,该反应的化学方程式为___________ 。

已知:①透明氧化铁又称纳米氧化铁,粒子直径微小(10~90nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
②Fe3+能将FeS2中的硫元素氧化为+6价。
回答下列问题:
(1)FeS2的电子式为
(2)“滤渣”中的主要成分是
(3)“还原”过程中涉及的离子方程式为
(4)流程中“
 ”环节的目的是
”环节的目的是(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到色泽纯正的氢氧化铁,而且还可以
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示:

称取3.47g透明氧化铁,用稀硫酸溶解并定容至1L,准确移取该溶液10.00mL,加入足量KSCN溶液,再用蒸馏水定容至100mL。测得溶液吸光度A=0.8,则透明氧化铁中氧化铁红(Fe2O3)的质量分数为
Ⅱ.氧化亚铜(Cu2O)用途广泛,干法生产Cu2O粉末的主要工艺流程如下:

(7)粉碎机中,发生的变化属于
(8)800~900℃时,煅烧炉中发生化合反应,该反应的化学方程式为
您最近一年使用:0次



