名校
1 . Ni2O3主要用作陶瓷、搪瓷和玻璃的着色颜料。也可用于镍粉的制造,其一种生产工艺如图。

有关氢氧化物开始沉淀和沉淀完全的pH如表:
(1)Ni2O3中Ni的化合价为___ 。
(2)“酸浸”时温度不宜过高的原因是__ 。
(3)加入H2O2“氧化”的目的是__ 。加入Na2CO3溶液调节溶液pH的范围为__ 。
(4)从滤液A中可回收利用的主要物质是__ 。
(5)加入NaClO溶液和NaOH溶液,“氧化”生成Ni2O3的离子方程式为__ 。
(6)为测定样品中Ni2O3的质量分数。进行实验;称取5.000g样品。加入足量硫酸后再加入100mL1.0mol·L-1的Fe2+标准溶液。充分反应。加水定容至200mL.取出20.00mL。用0.040mol·L-1KMnO4标准溶液滴定。用去KMnO4标准溶液20.00mL。试通过计算确定Ni2O3的质量分数__ 。测定过程中涉及的反应如下:Ni2O3+2Fe2++6H+=2Ni2++2Fe3++3H2O;5Fe2++MnO +8H+=5Fe3++Mn2++4H2O。
+8H+=5Fe3++Mn2++4H2O。

有关氢氧化物开始沉淀和沉淀完全的pH如表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀时pH | 1.5 | 6.5 | 7.1 |
| 完全沉淀时pH | 3.7 | 9.7 | 9.1 |
(2)“酸浸”时温度不宜过高的原因是
(3)加入H2O2“氧化”的目的是
(4)从滤液A中可回收利用的主要物质是
(5)加入NaClO溶液和NaOH溶液,“氧化”生成Ni2O3的离子方程式为
(6)为测定样品中Ni2O3的质量分数。进行实验;称取5.000g样品。加入足量硫酸后再加入100mL1.0mol·L-1的Fe2+标准溶液。充分反应。加水定容至200mL.取出20.00mL。用0.040mol·L-1KMnO4标准溶液滴定。用去KMnO4标准溶液20.00mL。试通过计算确定Ni2O3的质量分数
 +8H+=5Fe3++Mn2++4H2O。
+8H+=5Fe3++Mn2++4H2O。
您最近一年使用:0次
2020-10-04更新
|
243次组卷
|
2卷引用:贵州省贵阳市2021届高三8月摸底考试化学试题
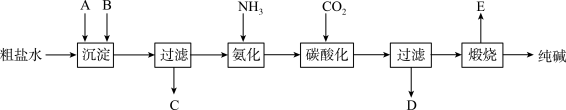
2 . 工业生产纯碱的工艺流程示意图如下:
完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。
A__________________________________ B__________________________________
(2)实验室提纯粗盐的实验操作依次为:
取样、______ 、沉淀、______ 、______ 、冷却结晶、______ 、烘干。
(3)工业生产纯碱工艺流程中,碳酸化时产生的现象是____________________________ 。
碳酸化时没有析出碳酸钠晶体,其原因是_______________________________________ 。
(4)碳酸化后过滤,滤液D最主要的成分是_____________________________ (填写化学式),检验这一成分的阴离子的具体方法是:________________________________________ 。
(5)氨碱法流程中氨是循环使用的,为此,滤液D加入石灰水产生氨。加石灰水后所发生的反应的离子方程式为:_________________________________________________________
滤液D加石灰水前先要加热,原因是_____________________________________________ 。
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:
_____________________________________________________________________________
(注明你的表达式中所用的有关符号的含义)

完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。
A
(2)实验室提纯粗盐的实验操作依次为:
取样、
(3)工业生产纯碱工艺流程中,碳酸化时产生的现象是
碳酸化时没有析出碳酸钠晶体,其原因是
(4)碳酸化后过滤,滤液D最主要的成分是
(5)氨碱法流程中氨是循环使用的,为此,滤液D加入石灰水产生氨。加石灰水后所发生的反应的离子方程式为:
滤液D加石灰水前先要加热,原因是
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:
(注明你的表达式中所用的有关符号的含义)
您最近一年使用:0次
2019-01-30更新
|
2010次组卷
|
6卷引用:2014届贵州省遵义市高三五校联考理综化学试卷
(已下线)2014届贵州省遵义市高三五校联考理综化学试卷贵州省余庆中学2019-2020学年上学期开学考试高三化学试题2010年全国普通高等学校招生统一考试上海卷化学试题(已下线)2011届湖北省天门市高三模拟考试(一)(理综)化学部分2020届高三化学大二轮增分强化练——化学工艺流程题2010年高考化学试题分项专题十五 化学实验
名校
3 . 金属的使用是人类拓展自身能力的标志之一。人类利用几种常用金属的先后顺序依次为金、铜、铁、铝,之所以有先后,主要取决于
| A.金属在地壳中的含量多少 | B.金属的熔沸点高低 |
| C.金属的活泼性强弱 | D.金属的导电性强弱 |
您最近一年使用:0次
2016-12-09更新
|
934次组卷
|
7卷引用:贵州省黔南布依族苗族自治州瓮安第二中学2019-2020学年高三上学期期末考试化学试题



