名校
解题方法
1 . “化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。
(1)小苏打常用于糕点制作,还可治疗胃酸过多等,有多种用途。请写出小苏打溶液与氢氧化钠溶液反应的离子方程式:_________ 。
(2)过氧化钠常用作呼吸面具或潜水艇中的供氧剂,请你写出过氧化钠与二氧化碳反应的化学方程式:_________ 。
(3)有小组同学称取10 g所制备Na2O2的样品(设样品中杂质不参与下列反应),利用下列装置测定Na2O2样品的纯度(夹持仪器省略),已知Na2O2的摩尔质量为78 g/mol。

有同学提出该实验装置存在缺陷,应该在A、B装置之间增加一个盛有饱和 溶液的洗气瓶,该同学想法是否有必要?理由是
溶液的洗气瓶,该同学想法是否有必要?理由是_________ 。倒出量筒内水的体积后,折算成标准状况下O2的体积为1120 mL,计算样品中Na2O2的质量分数约为_________ 。
(4)向30 mL NaOH溶液中逐渐通入一定量的CO2,再向该溶液中逐滴加入2 mol/L盐酸,所加入盐酸的体积(单位为mL)与产生二氧化碳的体积(标准状况下)关系如图所示。
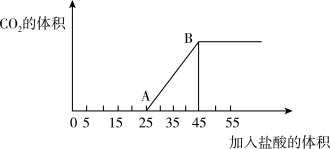
A点溶液中溶质为:_________ ,计算原NaOH溶液的物质的量浓度是_________ mol/L。
(1)小苏打常用于糕点制作,还可治疗胃酸过多等,有多种用途。请写出小苏打溶液与氢氧化钠溶液反应的离子方程式:
(2)过氧化钠常用作呼吸面具或潜水艇中的供氧剂,请你写出过氧化钠与二氧化碳反应的化学方程式:
(3)有小组同学称取10 g所制备Na2O2的样品(设样品中杂质不参与下列反应),利用下列装置测定Na2O2样品的纯度(夹持仪器省略),已知Na2O2的摩尔质量为78 g/mol。

有同学提出该实验装置存在缺陷,应该在A、B装置之间增加一个盛有饱和
 溶液的洗气瓶,该同学想法是否有必要?理由是
溶液的洗气瓶,该同学想法是否有必要?理由是(4)向30 mL NaOH溶液中逐渐通入一定量的CO2,再向该溶液中逐滴加入2 mol/L盐酸,所加入盐酸的体积(单位为mL)与产生二氧化碳的体积(标准状况下)关系如图所示。

A点溶液中溶质为:
您最近一年使用:0次
2 . 金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制的工业方法,其反应原理: 2NaCl(熔融) 2Na+Cl2↑。
2Na+Cl2↑。
回答下列有关单质钠的问题:
(1)下列各项中属于保存金属钠的正确方法是_______ 。
A.放在棕色瓶中 B.放在细沙中 C.放在水中 D.放在煤油中
(2)将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,请写出发生反应的化学方程式:_______ ,生成物的颜色为_______ 。
(3)过氧化钠常用于呼吸面具和潜水艇氧气的来源,其原理为:_______ ,_______ 。(用化学反应方程式表示)
(4)将一定质量的镁、铝合金投入一定浓度的100 mL盐酸中,使合金全部溶解,向所得溶液中滴加5.0 mol·L-1 的NaOH溶液至过量,生成沉淀的质量与加入NaOH溶液体积的关系如图所示。

则原合金中铝的质量分数为_______ 。盐酸中HCl的物质的量浓度为_______ 。
 2Na+Cl2↑。
2Na+Cl2↑。回答下列有关单质钠的问题:
(1)下列各项中属于保存金属钠的正确方法是
A.放在棕色瓶中 B.放在细沙中 C.放在水中 D.放在煤油中
(2)将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,请写出发生反应的化学方程式:
(3)过氧化钠常用于呼吸面具和潜水艇氧气的来源,其原理为:
(4)将一定质量的镁、铝合金投入一定浓度的100 mL盐酸中,使合金全部溶解,向所得溶液中滴加5.0 mol·L-1 的NaOH溶液至过量,生成沉淀的质量与加入NaOH溶液体积的关系如图所示。

则原合金中铝的质量分数为
您最近一年使用:0次
3 . (1)已知某盐酸溶液的密度为1.19g/cm3 ,质量分数为36.5%,则该溶液的物质的量浓度为___________
(2)含0.3 mol SO42-的Al2(SO4)3中所含的Al3+的数目为________________ 。
(3)相同质量的SO2、SO3硫原子的个数之比为_______________ 。
(4)33.3g某二价金属氯化物(ACl2)中含有0.6mol Cl−,则ACl2的化学式是_________ 。
(5)标准状况下,1.204×1023个H2的体积约为_______________ L
(2)含0.3 mol SO42-的Al2(SO4)3中所含的Al3+的数目为
(3)相同质量的SO2、SO3硫原子的个数之比为
(4)33.3g某二价金属氯化物(ACl2)中含有0.6mol Cl−,则ACl2的化学式是
(5)标准状况下,1.204×1023个H2的体积约为
您最近一年使用:0次
名校
4 . 有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)A原子的核外电子排布式:____________________________________________________ 。
(2)B元素在周期表中的位置:______________________________________________________ ;
离子半径:B________ (填“大于”或“小于”)A。
(3)C原子的电子排布图是_________ ,其原子核外有____ 个未成对电子,能量最高的电子为____ 轨道上的电子,其轨道呈______ 形。
(4)D-的结构示意图是________ 。
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为___________ 。与D的氢化物的水化物反应的化学方程式为__________________ 。
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生成过程中常用的消毒杀菌剂 |
请根据表中信息填写:
(1)A原子的核外电子排布式:
(2)B元素在周期表中的位置:
离子半径:B
(3)C原子的电子排布图是
(4)D-的结构示意图是
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为
您最近一年使用:0次
2016-12-09更新
|
129次组卷
|
5卷引用:贵州省毕节市黔西县第一中学2018-2019学年高二上学期12月份考试化学试题



