“化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。
(1)小苏打常用于糕点制作,还可治疗胃酸过多等,有多种用途。请写出小苏打溶液与氢氧化钠溶液反应的离子方程式:_________ 。
(2)过氧化钠常用作呼吸面具或潜水艇中的供氧剂,请你写出过氧化钠与二氧化碳反应的化学方程式:_________ 。
(3)有小组同学称取10 g所制备Na2O2的样品(设样品中杂质不参与下列反应),利用下列装置测定Na2O2样品的纯度(夹持仪器省略),已知Na2O2的摩尔质量为78 g/mol。

有同学提出该实验装置存在缺陷,应该在A、B装置之间增加一个盛有饱和 溶液的洗气瓶,该同学想法是否有必要?理由是
溶液的洗气瓶,该同学想法是否有必要?理由是_________ 。倒出量筒内水的体积后,折算成标准状况下O2的体积为1120 mL,计算样品中Na2O2的质量分数约为_________ 。
(4)向30 mL NaOH溶液中逐渐通入一定量的CO2,再向该溶液中逐滴加入2 mol/L盐酸,所加入盐酸的体积(单位为mL)与产生二氧化碳的体积(标准状况下)关系如图所示。
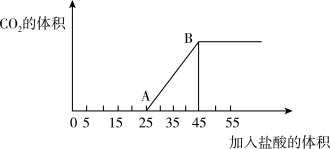
A点溶液中溶质为:_________ ,计算原NaOH溶液的物质的量浓度是_________ mol/L。
(1)小苏打常用于糕点制作,还可治疗胃酸过多等,有多种用途。请写出小苏打溶液与氢氧化钠溶液反应的离子方程式:
(2)过氧化钠常用作呼吸面具或潜水艇中的供氧剂,请你写出过氧化钠与二氧化碳反应的化学方程式:
(3)有小组同学称取10 g所制备Na2O2的样品(设样品中杂质不参与下列反应),利用下列装置测定Na2O2样品的纯度(夹持仪器省略),已知Na2O2的摩尔质量为78 g/mol。

有同学提出该实验装置存在缺陷,应该在A、B装置之间增加一个盛有饱和
 溶液的洗气瓶,该同学想法是否有必要?理由是
溶液的洗气瓶,该同学想法是否有必要?理由是(4)向30 mL NaOH溶液中逐渐通入一定量的CO2,再向该溶液中逐滴加入2 mol/L盐酸,所加入盐酸的体积(单位为mL)与产生二氧化碳的体积(标准状况下)关系如图所示。

A点溶液中溶质为:
更新时间:2022-12-04 10:19:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)Na2O2__________ (填“是”或“否”)属于碱性氧化物,Na2O2是______ 色固体粉末。向包有Na2O2固体的棉花上滴几滴水,棉花很快燃烧起来,原因是该反应有氧气生成且该反应为__________ (填”吸热”或者“放热”)反应;
(2)Na2O2作为在潜水艇和消防员呼吸面具中的供氧剂,写出其中一个反应的化学方程式_________ ,某潜水艇中有50人,若每人每小时消耗O2在标准状况下的体积为44.8L,假设所需要的O2全由Na2O2所提供,则每小时所需Na2O2的质量为________ kg。
(3)3.1gNa2O溶于水配成1L溶液,溶液中Na+离子物质的量浓度为________
(4)制备Fe(OH)3胶体:用洁净的烧杯取一定量蒸馏水,用酒精灯加热至沸腾,向烧杯中加入几滴饱和FeCl3溶液继续加热至液体呈透明的红褐色。
①写出制备Fe(OH)3胶体反应的离子方程式______________________________
②验证制得的分散系是胶体的方法为_________________________________
(2)Na2O2作为在潜水艇和消防员呼吸面具中的供氧剂,写出其中一个反应的化学方程式
(3)3.1gNa2O溶于水配成1L溶液,溶液中Na+离子物质的量浓度为
(4)制备Fe(OH)3胶体:用洁净的烧杯取一定量蒸馏水,用酒精灯加热至沸腾,向烧杯中加入几滴饱和FeCl3溶液继续加热至液体呈透明的红褐色。
①写出制备Fe(OH)3胶体反应的离子方程式
②验证制得的分散系是胶体的方法为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.如图1所示,某化学小组拟用该装置制取纯净的 。
。

(1)若C是一种淡黄色固体,则烧瓶中发生反应的化学方程式是_______ 。
(2)若C是一种黑色粉末,则B是_______ ,C的作用是_______ 。
(3)广口瓶中盛装的试剂D是_______ ,其作用是_______ 。
Ⅱ.日常生活中常用到苏打和小苏打,鉴别它们的方法有多种。例如:

(4)方法①:如图2装置所示,这是根据它们具有不同的_______ 性质加以鉴别的。实验过程中,当试管B盛放的澄清溶液出现白色浑浊时,试管A中发生反应的化学方程式是_______ 。
(5)方法②:取等质量的苏打和小苏打分别放入试管中,再分别加入足量盐酸充分反应,比较相同条件下收集到的气体的体积。请写出相关反应的离子方程式:_______ ;_______ 。
 。
。
(1)若C是一种淡黄色固体,则烧瓶中发生反应的化学方程式是
(2)若C是一种黑色粉末,则B是
(3)广口瓶中盛装的试剂D是
Ⅱ.日常生活中常用到苏打和小苏打,鉴别它们的方法有多种。例如:

(4)方法①:如图2装置所示,这是根据它们具有不同的
(5)方法②:取等质量的苏打和小苏打分别放入试管中,再分别加入足量盐酸充分反应,比较相同条件下收集到的气体的体积。请写出相关反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】过氧化钠是重要的化工原料,具有多种用途。
(1)过氧化钠是_______ 色固体。
(2)过氧化钠可用作呼吸面具、潜水艇的供氧剂,写出 和
和 反应的化学方程式:
反应的化学方程式:_______ 。
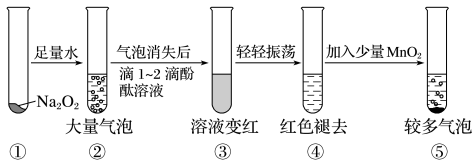
(3)某实验小组通过如图所示实验,探究 与水的反应,下列说法正确的是_______。
与水的反应,下列说法正确的是_______。
(4) 具有强氧化性,与
具有强氧化性,与 反应能生成硫酸钠,写出反应的化学方程式:
反应能生成硫酸钠,写出反应的化学方程式:_______ 。
(1)过氧化钠是
(2)过氧化钠可用作呼吸面具、潜水艇的供氧剂,写出
 和
和 反应的化学方程式:
反应的化学方程式:(3)某实验小组通过如图所示实验,探究
 与水的反应,下列说法正确的是_______。
与水的反应,下列说法正确的是_______。
| A.②中的大量气泡主要成分是氢气 |
| B.③中溶液变红,说明有酸性物质生成 |
| C.④中现象可能是由于溶液中含有强氧化性物质造成的 |
D.⑤中 的主要作用是降低了水中氧气的溶解度 的主要作用是降低了水中氧气的溶解度 |
 具有强氧化性,与
具有强氧化性,与 反应能生成硫酸钠,写出反应的化学方程式:
反应能生成硫酸钠,写出反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。
并检验其纯度的实验流程如图所示。

回答下列问题:
(1)生成 的化学方程式为
的化学方程式为_______ 。钠在空气中燃烧现象为_______ 。
(2)样液中加入 后产生一种无色无味的气体单质,该气体的名称为
后产生一种无色无味的气体单质,该气体的名称为_______ 。
(3)写出 与
与 反应的方程式
反应的方程式_______ 。已知白色沉淀为 ,说明
,说明 样品中含有杂质,为防止杂质的生成需对空气进行预处理,预处理的措施是
样品中含有杂质,为防止杂质的生成需对空气进行预处理,预处理的措施是_______ 。
 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。
并检验其纯度的实验流程如图所示。
回答下列问题:
(1)生成
 的化学方程式为
的化学方程式为(2)样液中加入
 后产生一种无色无味的气体单质,该气体的名称为
后产生一种无色无味的气体单质,该气体的名称为(3)写出
 与
与 反应的方程式
反应的方程式 ,说明
,说明 样品中含有杂质,为防止杂质的生成需对空气进行预处理,预处理的措施是
样品中含有杂质,为防止杂质的生成需对空气进行预处理,预处理的措施是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:____________ 。
(2)除去Na2CO3粉末中混入的NaHCO3杂质最佳方法是_________ ,化学方程式为_________ 。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:
(2)除去Na2CO3粉末中混入的NaHCO3杂质最佳方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价-类”二维图,请回答下列问题:

(1)物质①与水反应的离子方程式为_______ 。
(2)淡黄色固体②用于呼吸面具,写出②和CO2的反应方程式为_______ ,若有2mol的过氧化钠参与反应,转移的电子的物质的量为_______ mol。
(3)从核心元素价态的视角看,NaH中H元素的化合价为_______ ,从H元素的价态分析,NaH常用作_______ (填“氧化剂”或“还原剂”)。
(4)纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。

图Ⅲ、Ⅳ中_______ 能更好说明二者的稳定性(填装置序号)。Ⅳ中受热处发生反应的化学方程式:_______ 。
(5)若要除去碳酸氢钠溶液中的碳酸钠,发生反应的化学方程式为_______ 。

(1)物质①与水反应的离子方程式为
(2)淡黄色固体②用于呼吸面具,写出②和CO2的反应方程式为
(3)从核心元素价态的视角看,NaH中H元素的化合价为
(4)纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。

图Ⅲ、Ⅳ中
(5)若要除去碳酸氢钠溶液中的碳酸钠,发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】工业上产生的硫化氢要经过处理变成硫单质后方能排放,以防止大气污染。富玛克斯法治理硫化氢的方法和步骤如下:
①用2%~3%的Na2CO3溶液作吸收剂生成2种酸式盐;
②再加入一种RNO(液)(R表示芳香烃基)与生成的一种酸式盐的水溶液反应生成硫、碱和RNHOH;
③第②步生成的碱在溶液中与另一种酸式盐反应生成正盐;
④RNHOH与空气中的氧发生反应又得到RNO。
(1)写出上述四步反应的化学方程式_______ 。
(2)请对富玛克斯法的优点做一简要评价_______ 。
①用2%~3%的Na2CO3溶液作吸收剂生成2种酸式盐;
②再加入一种RNO(液)(R表示芳香烃基)与生成的一种酸式盐的水溶液反应生成硫、碱和RNHOH;
③第②步生成的碱在溶液中与另一种酸式盐反应生成正盐;
④RNHOH与空气中的氧发生反应又得到RNO。
(1)写出上述四步反应的化学方程式
(2)请对富玛克斯法的优点做一简要评价
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】写出下列反应的离子方程式:
(1)将铜片插入硝酸银溶液中:________________ ;
(2)铝和硫酸铜溶液反应:_________________ ;
(3)将氧化镁与稀盐酸混合:___________________ ;
(4)石灰乳与Na2CO3溶液混合:_________________ ;
(5)碳酸钡溶于稀盐酸中:_____________________ ;
(6)硫酸和氢氧化钡溶液反应:_________________ ;
(7)向氢氧化钠溶液中通入过量CO2:____________ ;
(8)将NaHCO3溶液滴入NaOH溶液中:_________________ 。
(1)将铜片插入硝酸银溶液中:
(2)铝和硫酸铜溶液反应:
(3)将氧化镁与稀盐酸混合:
(4)石灰乳与Na2CO3溶液混合:
(5)碳酸钡溶于稀盐酸中:
(6)硫酸和氢氧化钡溶液反应:
(7)向氢氧化钠溶液中通入过量CO2:
(8)将NaHCO3溶液滴入NaOH溶液中:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】煤是我国重要的化石燃料,煤化工行业中产生的H2S也是一种重要的工业资源.
(1)煤液化是_____ (填“物理”或“化学”)变化过程。
(2)煤液化过程中产生的H2S可生产硫酸,部分过程如图所示:
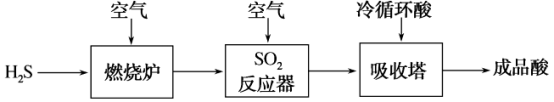
①SO2反应器中的化学方程式是_____ 。
②生产过程中的尾气需要测定SO2的含量符合标准才能排放.已知有V L(已换算成标准状况)尾气,通入足量H2O2吸收再加足量BaCl2溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥、称量得到b g沉淀。尾气中SO2的含量(体积分数)的计算式是_____ 。
(3)H2S还可用于回收单质硫.含有H2S和空气的尾气按一定流速通入酸性FeCl3溶液,可实现空气脱硫,得到单质硫.FeCl3溶液吸收H2S过程中,溶液中的n(Fe3+)、被吸收的n(H2S) 随时间t的变化如图。
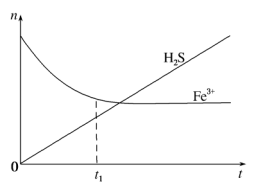
①由图中信息可知,0~t1时,一定发生的反应是_____ (用离子方程式表示)。
②t1以后,溶液中n(Fe3+)保持基本不变,原因是_____ 。
(1)煤液化是
(2)煤液化过程中产生的H2S可生产硫酸,部分过程如图所示:

①SO2反应器中的化学方程式是
②生产过程中的尾气需要测定SO2的含量符合标准才能排放.已知有V L(已换算成标准状况)尾气,通入足量H2O2吸收再加足量BaCl2溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥、称量得到b g沉淀。尾气中SO2的含量(体积分数)的计算式是
(3)H2S还可用于回收单质硫.含有H2S和空气的尾气按一定流速通入酸性FeCl3溶液,可实现空气脱硫,得到单质硫.FeCl3溶液吸收H2S过程中,溶液中的n(Fe3+)、被吸收的n(H2S) 随时间t的变化如图。

①由图中信息可知,0~t1时,一定发生的反应是
②t1以后,溶液中n(Fe3+)保持基本不变,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】连二亚硫酸钠的分析检测。铁氰化钾法:铁氰化钾K3[Fe(CN)6]是一种比较弱的氧化剂,其具有强氧化剂所没有的选择性氧化性,能将S2O 氧化为SO
氧化为SO ,[Fe(CN)6]3-还原为[Fe(CN)6]
,[Fe(CN)6]3-还原为[Fe(CN)6] 。取50.00mLNa2S2O4样品溶液,用0.02mol•L-1的K3[Fe(CN)6]标准液滴定至终点,消耗10.00mL。该样品中Na2S2O4的含量为
。取50.00mLNa2S2O4样品溶液,用0.02mol•L-1的K3[Fe(CN)6]标准液滴定至终点,消耗10.00mL。该样品中Na2S2O4的含量为___________ g•L-1.(以SO2计)
 氧化为SO
氧化为SO ,[Fe(CN)6]3-还原为[Fe(CN)6]
,[Fe(CN)6]3-还原为[Fe(CN)6] 。取50.00mLNa2S2O4样品溶液,用0.02mol•L-1的K3[Fe(CN)6]标准液滴定至终点,消耗10.00mL。该样品中Na2S2O4的含量为
。取50.00mLNa2S2O4样品溶液,用0.02mol•L-1的K3[Fe(CN)6]标准液滴定至终点,消耗10.00mL。该样品中Na2S2O4的含量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在铋系高温超导材料的探索中,得到样品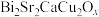 ,其中Cu可能存在的价态为+2和+3,Bi的可能价态为+3和+5.设计如下实验测定两种元素的平均氧化态。
,其中Cu可能存在的价态为+2和+3,Bi的可能价态为+3和+5.设计如下实验测定两种元素的平均氧化态。
实验A:将102.3mg样品(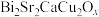 ,式量为760.4+16.00x)溶于100.0mL含有
,式量为760.4+16.00x)溶于100.0mL含有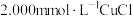 的
的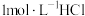 溶液中,以库仑滴定法测定过量的
溶液中,以库仑滴定法测定过量的 ,结果为0.1085mmol。
,结果为0.1085mmol。
实验B:将94.6mg样品溶解于 的酸性溶液中。以库仑滴定法测定过量的
的酸性溶液中。以库仑滴定法测定过量的 ,结果为0.0577mmol。
,结果为0.0577mmol。
(1)写出实验A中样品溶解时涉及氧化还原反应的所有方程式___________ 。
(2)写出实验B中样品溶解时涉及氧化还原反应的所有方程式___________ 。
(3)求算样品中Bi和Cu的氧化数,确定化学式中x的值___________ 。
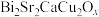 ,其中Cu可能存在的价态为+2和+3,Bi的可能价态为+3和+5.设计如下实验测定两种元素的平均氧化态。
,其中Cu可能存在的价态为+2和+3,Bi的可能价态为+3和+5.设计如下实验测定两种元素的平均氧化态。实验A:将102.3mg样品(
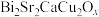 ,式量为760.4+16.00x)溶于100.0mL含有
,式量为760.4+16.00x)溶于100.0mL含有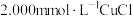 的
的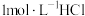 溶液中,以库仑滴定法测定过量的
溶液中,以库仑滴定法测定过量的 ,结果为0.1085mmol。
,结果为0.1085mmol。实验B:将94.6mg样品溶解于
 的酸性溶液中。以库仑滴定法测定过量的
的酸性溶液中。以库仑滴定法测定过量的 ,结果为0.0577mmol。
,结果为0.0577mmol。(1)写出实验A中样品溶解时涉及氧化还原反应的所有方程式
(2)写出实验B中样品溶解时涉及氧化还原反应的所有方程式
(3)求算样品中Bi和Cu的氧化数,确定化学式中x的值
您最近一年使用:0次

 固体;④
固体;④ 晶体
晶体

