名校
1 . 甘肃马家窑遗址(今临洮县)出土的青铜刀,是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,其化学式为Cu2(OH)2CO3。
(1)从物质分类标准看,“铜绿”属于哪类物质___________。(填选项)
(2)铜器表面有时会生成“铜绿”,这层“铜绿”可用化学方法除去,写出盐酸去除“铜绿”的化学方程式:___________ 。
(3)现代工业以黄铜矿为原料,在炼铜的过程中发生了多个反应,其中有如下两个反应:反应Ⅰ:2Cu2S+3O2 2Cu2O+2SO2,反应Ⅱ:Cu2S+2Cu2O
2Cu2O+2SO2,反应Ⅱ:Cu2S+2Cu2O 6Cu+SO2↑,请回答下列问题:
6Cu+SO2↑,请回答下列问题:
①反应Ⅰ中,氧化产物是___________ ,用单线桥标出反应Ⅰ中电子转移的方向和数目________ 。
②反应Ⅱ中,Cu2O的作用是___________ (填“氧化剂”“还原剂”或“氧化剂和还原剂”)。
(1)从物质分类标准看,“铜绿”属于哪类物质___________。(填选项)
| A.酸 | B.碱 | C.盐 | D.氧化物 |
(3)现代工业以黄铜矿为原料,在炼铜的过程中发生了多个反应,其中有如下两个反应:反应Ⅰ:2Cu2S+3O2
 2Cu2O+2SO2,反应Ⅱ:Cu2S+2Cu2O
2Cu2O+2SO2,反应Ⅱ:Cu2S+2Cu2O 6Cu+SO2↑,请回答下列问题:
6Cu+SO2↑,请回答下列问题:①反应Ⅰ中,氧化产物是
②反应Ⅱ中,Cu2O的作用是
您最近一年使用:0次
名校
2 . 回答下列问题
(1)火药是中国的“四大发明”之一,黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑,其中被氧化的元素是___________ (填元素名称)。
(2)人体内的铁元素是以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转换成Fe2+,有利于人体吸收,说明维生素C具有___________ (填“氧化性”或“还原性”)。
(3)工业废水中含有的重铬酸根离子(Cr2O )有毒,必须处理达标后才能排放。工业上常用明矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放。工业上常用明矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O,在该反应中,氧化剂是
+14H+=6Fe3++2Cr3++7H2O,在该反应中,氧化剂是___________ (填离子符号,下同),被氧化的是___________ 。
(4)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式___________ 。
(1)火药是中国的“四大发明”之一,黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑,其中被氧化的元素是
(2)人体内的铁元素是以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转换成Fe2+,有利于人体吸收,说明维生素C具有
(3)工业废水中含有的重铬酸根离子(Cr2O
 )有毒,必须处理达标后才能排放。工业上常用明矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放。工业上常用明矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O,在该反应中,氧化剂是
+14H+=6Fe3++2Cr3++7H2O,在该反应中,氧化剂是(4)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式
您最近一年使用:0次
名校
3 . 央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是___________ 价。Fe(CrO2)2属于___________ (填“酸”、“碱”、“盐”或“氧化物”)。
(2)明胶的水溶液和K2SO4溶液共同具备的性质是___________(填序号)。
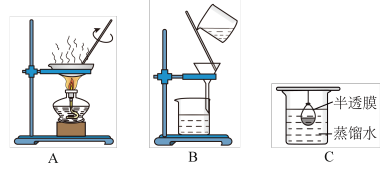
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的___________ (填序号)。
A.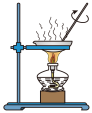 B.
B.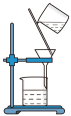 C.
C.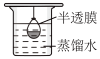
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
(2)明胶的水溶液和K2SO4溶液共同具备的性质是___________(填序号)。
| A.都不稳定,密封放置会产生沉淀 | B.分散质粒子可通过滤纸 |
| C.分散质粒子可通过半透膜 | D.二者均有丁达尔效应 |
A.
 B.
B. C.
C.
您最近一年使用:0次
名校
4 . 对于成千上万、形形色色的化学物质,用分类的思想对其进行学习和研究极其重要。有以下物质,请按要求作答。
现有下列10种物质:①铝;②纯醋酸;③CO2;④H2SO4;⑤NaOH;⑥硫酸铜溶液;⑦熔融的NaCl;⑧NaHSO4;⑨硝酸钾晶体;⑩乙醇。
(1)上述物质中属于电解质的有___________ (填序号,下同);属于非电解质的有___________ ;①②⑥⑦⑨⑩六种物质中能导电的有___________ 。
(2)向⑥中加入⑤的离子方程式是___________ 。
(3)②在水中的电离方程式为___________ 。
(4)向Ba(OH)2的水溶液中逐滴滴加⑧的水溶液,当溶液恰好呈中性时NaHSO4与Ba(OH)2反应的化学计量数之比为___________ ,其离子反应方程式为___________ 。
现有下列10种物质:①铝;②纯醋酸;③CO2;④H2SO4;⑤NaOH;⑥硫酸铜溶液;⑦熔融的NaCl;⑧NaHSO4;⑨硝酸钾晶体;⑩乙醇。
(1)上述物质中属于电解质的有
(2)向⑥中加入⑤的离子方程式是
(3)②在水中的电离方程式为
(4)向Ba(OH)2的水溶液中逐滴滴加⑧的水溶液,当溶液恰好呈中性时NaHSO4与Ba(OH)2反应的化学计量数之比为
您最近一年使用:0次
名校
5 . 现有以下物质:①H2SO4;②氯水;③KOH固体;④熔融KHSO4;⑤漂白粉;⑥生铁;⑦SO2;⑧Al2O3;⑨蔗糖。请回答下列问题:
(1)以上物质中能导电的是_______ (填序号),以上物质中属于电解质的是_______ (填序号)。以上物质中属于非电解质的是_______ (填序号)。
(2)某物质A加热时按化学方程式 分解,产物均为全体,测得相同条件下由生成物组成的混合气体对
分解,产物均为全体,测得相同条件下由生成物组成的混合气体对 的相对密度为50,则反应物A的摩尔质量为
的相对密度为50,则反应物A的摩尔质量为_______ 。
(3)标准状况下,将V L的氨气溶于1 L的水中,所得溶液的密度为 ,此氨水的物质的量浓度是
,此氨水的物质的量浓度是_______ mol/L:已知8 mol/L的氨水的密度为 ,2 mol/L的氨水的密度为
,2 mol/L的氨水的密度为 ,
, ,若将上述两种溶液等质量混合(忽略混合时体积变化),所得氨水的浓度
,若将上述两种溶液等质量混合(忽略混合时体积变化),所得氨水的浓度_______ 5 mol/L(填>、<或=)。
(1)以上物质中能导电的是
(2)某物质A加热时按化学方程式
 分解,产物均为全体,测得相同条件下由生成物组成的混合气体对
分解,产物均为全体,测得相同条件下由生成物组成的混合气体对 的相对密度为50,则反应物A的摩尔质量为
的相对密度为50,则反应物A的摩尔质量为(3)标准状况下,将V L的氨气溶于1 L的水中,所得溶液的密度为
 ,此氨水的物质的量浓度是
,此氨水的物质的量浓度是 ,2 mol/L的氨水的密度为
,2 mol/L的氨水的密度为 ,
, ,若将上述两种溶液等质量混合(忽略混合时体积变化),所得氨水的浓度
,若将上述两种溶液等质量混合(忽略混合时体积变化),所得氨水的浓度
您最近一年使用:0次
6 . 利用下图可从不同角度研究含氯物质的性质及其转化关系。回答下列问题:
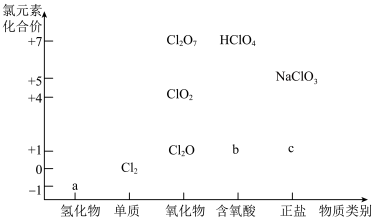
(1)图中a物质是否为电解质___________ (填“是”或“否”),b物质的化学式为___________ 。
(2)实验室用二氧化锰与浓盐酸在加热条件下制取氯气,写出该反应的离子方程式:___________ 。
(3)“84消毒液”是常用含氯消毒剂,其有效成分是图中c物质,“84消毒液”不可与洁厕灵(主要成分稀盐酸)混合使用的原因是___________ 。(用离子方程式说明)
(4)工业漂白粉中的有效成分 能与空气中的水蒸气和二氧化碳发生如下反应:
能与空气中的水蒸气和二氧化碳发生如下反应: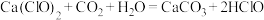 ,久置于空气中的漂白粉易失效,请用化学方程式解释漂白粉失效的原因:
,久置于空气中的漂白粉易失效,请用化学方程式解释漂白粉失效的原因:___________ 。
(5)高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理,工业上制备 有多种方法,其中一种制备的化学原理是在碱性条件下用
有多种方法,其中一种制备的化学原理是在碱性条件下用 氧化氯化铁,请完成离子方程式的配平:
氧化氯化铁,请完成离子方程式的配平:
__ ____
____ ____
____ —___
—___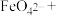 ___
___ ___
___ ,
,______________ 。反应中消耗 数与转移的电子数之比是
数与转移的电子数之比是___________ 。

(1)图中a物质是否为电解质
(2)实验室用二氧化锰与浓盐酸在加热条件下制取氯气,写出该反应的离子方程式:
(3)“84消毒液”是常用含氯消毒剂,其有效成分是图中c物质,“84消毒液”不可与洁厕灵(主要成分稀盐酸)混合使用的原因是
(4)工业漂白粉中的有效成分
 能与空气中的水蒸气和二氧化碳发生如下反应:
能与空气中的水蒸气和二氧化碳发生如下反应: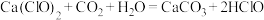 ,久置于空气中的漂白粉易失效,请用化学方程式解释漂白粉失效的原因:
,久置于空气中的漂白粉易失效,请用化学方程式解释漂白粉失效的原因:(5)高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理,工业上制备
 有多种方法,其中一种制备的化学原理是在碱性条件下用
有多种方法,其中一种制备的化学原理是在碱性条件下用 氧化氯化铁,请完成离子方程式的配平:
氧化氯化铁,请完成离子方程式的配平:__
 ____
____ ____
____ —___
—___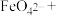 ___
___ ___
___ ,
, 数与转移的电子数之比是
数与转移的电子数之比是
您最近一年使用:0次
2023-07-28更新
|
283次组卷
|
2卷引用:江西省赣州市2022-2023学年高一上学期11月期中考试化学试题
7 . 根据所学知识完成下列问题。
(1)有下列四个反应:
① ②
②
③ ④
④
上述反应中不属于氧化还原反应的是_________ (填序号,下同); 只作还原剂的是
只作还原剂的是_______ ;属于氧化还原反应,但其中的 既不被氧化,又不被还原的是
既不被氧化,又不被还原的是_________ 。
(2)为治理汽车尾气中的 和
和 对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应
对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应 。
。
①用双线桥标出电子转移的方向和数目___________ (注明得失)
②若消耗 的
的 得到氧化产物的质量为
得到氧化产物的质量为___________ g。
(3)唐代是我国古代炼丹术的鼎盛时期,皇帝、王公贵族、士大夫均热衷于此,其中用的铅丹与硝酸反应方程式是:X(铅丹) ,则铅丹的化学式为
,则铅丹的化学式为_______ ,铅丹可以由一氧化铅( )在空气中加热至500℃制备,制备铅丹的化学方程式为
)在空气中加热至500℃制备,制备铅丹的化学方程式为_______ 。
(1)有下列四个反应:
①
 ②
②
③
 ④
④
上述反应中不属于氧化还原反应的是
 只作还原剂的是
只作还原剂的是 既不被氧化,又不被还原的是
既不被氧化,又不被还原的是(2)为治理汽车尾气中的
 和
和 对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应
对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应 。
。①用双线桥标出电子转移的方向和数目
②若消耗
 的
的 得到氧化产物的质量为
得到氧化产物的质量为(3)唐代是我国古代炼丹术的鼎盛时期,皇帝、王公贵族、士大夫均热衷于此,其中用的铅丹与硝酸反应方程式是:X(铅丹)
 ,则铅丹的化学式为
,则铅丹的化学式为 )在空气中加热至500℃制备,制备铅丹的化学方程式为
)在空气中加热至500℃制备,制备铅丹的化学方程式为
您最近一年使用:0次
2023-07-28更新
|
254次组卷
|
5卷引用:江西省赣州市2022-2023学年高一上学期11月期中考试化学试题
名校
解题方法
8 . 央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是__________ 价。 是一种酸根离子,则
是一种酸根离子,则 属于
属于__________ (填“酸”、“碱”、“盐”或“氧化物”)。
(2)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的__________ (填序号)。
(3)现有10mL明胶的水溶液与5mLK2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜:
能够透过半透膜:_____________________ ;该检验过程中发生的离子方程式为____________________ 。
(1)已知
 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是 是一种酸根离子,则
是一种酸根离子,则 属于
属于(2)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的

(3)现有10mL明胶的水溶液与5mLK2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
 能够透过半透膜:
能够透过半透膜:
您最近一年使用:0次
9 . 回答下列问题:
(1)写出以下反应的化学方程式,并用双线桥表示反应中电子转移的方向和数目:H2S气体和SO2气体反应生成S和水:_______ 。
(2)写出以下反应的离子方程式,并用单线桥表示反应中电子转移的数目:实验室用MnO2和浓盐酸制Cl2:_______ 。
(3)写出下列物质的结构式:CH4_______ ;CO2 _______ 。
(4)写出下列物质的电子式:NH4Cl_______ ;Na2O2 _______ 。
(1)写出以下反应的化学方程式,并用双线桥表示反应中电子转移的方向和数目:H2S气体和SO2气体反应生成S和水:
(2)写出以下反应的离子方程式,并用单线桥表示反应中电子转移的数目:实验室用MnO2和浓盐酸制Cl2:
(3)写出下列物质的结构式:CH4
(4)写出下列物质的电子式:NH4Cl
您最近一年使用:0次
名校
解题方法
10 . 回答下列问题:
(1)氧化还原反应与四种基本类型反应的关系如图,则下列化学反应属于区域3的反应是 (填序号)。

(2)高锰酸钾和氢溴酸溶液可以发生如下反应;2KMnO4+16HBr=5Br2+2MnBr2+2KBr+8H2O。
①其中____________ 元素被氧化(填化学式,下同),_________ 作氧化剂。
②在参加反应的HBr中,起还原剂(被氧化)作用的HBr与起酸性作用的HBr的质量之比为____________ 。
(3)某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
①若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是____________ 。
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
②写出制备 Fe(OH)3胶体的化学反应方程式:____________ 。
③Fe(OH)3胶体区别于FeCl3溶液最本质的特征是____________ 。
A.Fe(OH)3胶体粒子的直径在1~100 nm之间 B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系 D.Fe(OH)3胶体的分散质粒子能透过滤纸
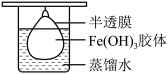
④将制得的胶体放入半透膜制成的袋内,如图所示,放置2 min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察____________ (填“有”或“无”)丁达尔现象。
(1)氧化还原反应与四种基本类型反应的关系如图,则下列化学反应属于区域3的反应是 (填序号)。

A. |
B.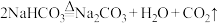 |
C. |
| D.Zn+H2SO4=ZnSO4+H2↑ |
①其中
②在参加反应的HBr中,起还原剂(被氧化)作用的HBr与起酸性作用的HBr的质量之比为
(3)某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
①若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
②写出制备 Fe(OH)3胶体的化学反应方程式:
③Fe(OH)3胶体区别于FeCl3溶液最本质的特征是
A.Fe(OH)3胶体粒子的直径在1~100 nm之间 B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系 D.Fe(OH)3胶体的分散质粒子能透过滤纸
④将制得的胶体放入半透膜制成的袋内,如图所示,放置2 min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察

您最近一年使用:0次



