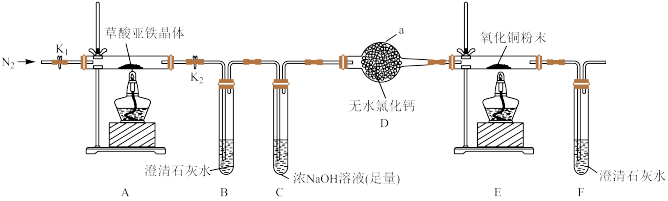
1 . 草酸亚铁晶体( FeC2O4·2H2O)是一种淡黄色粉末,可用作照相显影剂。某课外小组利用如下实验装置对草酸亚铁晶体分解产物进行探究,并设计实验测定草酸亚铁晶体样品纯度。
回答下列问题:
(1)仪器a的名称为_____ ;装置B中澄清石灰水变浑浊,说明气体分解产物中含有_____ ;
(2)实验前先通一段时间N2目的是________ ;装置C中浓NaOH溶液的作用是______ ;
(3)证明草酸亚铁晶体分解产物中含有CO的实验现象是______ ;
(4)充分反应后,将装置A硬质玻璃管中的残留固体溶于足量的稀硫酸中,无气泡产生,滴加几滴KSCN溶液,溶液不变红,说明固体分解产物是______ (填化学式);根据上述实验现象写出草酸亚铁晶体分解的化学方程式_______ ;
(5)所给实验装置存在明显的设计缺陷,该缺陷是______ ;
(6)草酸亚铁晶体样品纯度的测定:准确称取12. 000 g某草酸亚铁晶体样品,在一定条件下溶于稍过量的硫酸中,配成250 mL溶液。取25.00 mL上述溶液,用0.100 mol/L KMnO4标准溶液滴定,达到滴定终点时, 消耗35.00 mL KMnO4标准溶液,滴定反应为:FeC2O4·2H2O + KMnO4+ H2SO4→Fe2(SO4)3+CO2↑+ MnSO4 + K2SO4 + H2O(未配平)。则该草酸亚铁晶体样品的纯度为________ (已知该草酸亚铁晶体样品中不含其他与高锰酸钾反应的还原性杂质)。

回答下列问题:
(1)仪器a的名称为
(2)实验前先通一段时间N2目的是
(3)证明草酸亚铁晶体分解产物中含有CO的实验现象是
(4)充分反应后,将装置A硬质玻璃管中的残留固体溶于足量的稀硫酸中,无气泡产生,滴加几滴KSCN溶液,溶液不变红,说明固体分解产物是
(5)所给实验装置存在明显的设计缺陷,该缺陷是
(6)草酸亚铁晶体样品纯度的测定:准确称取12. 000 g某草酸亚铁晶体样品,在一定条件下溶于稍过量的硫酸中,配成250 mL溶液。取25.00 mL上述溶液,用0.100 mol/L KMnO4标准溶液滴定,达到滴定终点时, 消耗35.00 mL KMnO4标准溶液,滴定反应为:FeC2O4·2H2O + KMnO4+ H2SO4→Fe2(SO4)3+CO2↑+ MnSO4 + K2SO4 + H2O(未配平)。则该草酸亚铁晶体样品的纯度为
您最近一年使用:0次
解题方法
2 . 已知A、B、C是中学化学常见物质,它们在一定条件下有如下转化关系:

(1)若A能使湿润的红色石蕊试纸变蓝;C为红棕色气体。则A转化为B反应的化学方程式为_____________ .
(2)若D是由地壳中含量最多的元素组成的非金属单质,A为短周期元素中金属性最强的金属单质,则C的电子式为_____________ .
(3)若D为氯碱工业的主要产品,B是一种两性氢氧化物,则B转化为C反应的离子方程式为____________________ .
(4)若D是一中常见金属,A为黄绿色气体,则C溶液在贮存时应加入少量D,其理由是(用必要的文字和离子方程式说明)___________ .
(5)若D 是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴阳离子均含10个电子,则B转化为C的离子方程式为_____________ .
(6)若A、B、C均为氧化物,D是一种黑色固态非金属单质,则B分子的结构式为_________ .

(1)若A能使湿润的红色石蕊试纸变蓝;C为红棕色气体。则A转化为B反应的化学方程式为
(2)若D是由地壳中含量最多的元素组成的非金属单质,A为短周期元素中金属性最强的金属单质,则C的电子式为
(3)若D为氯碱工业的主要产品,B是一种两性氢氧化物,则B转化为C反应的离子方程式为
(4)若D是一中常见金属,A为黄绿色气体,则C溶液在贮存时应加入少量D,其理由是(用必要的文字和离子方程式说明)
(5)若D 是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴阳离子均含10个电子,则B转化为C的离子方程式为
(6)若A、B、C均为氧化物,D是一种黑色固态非金属单质,则B分子的结构式为
您最近一年使用:0次



