1 . Cl2既是实验室中的一种重要试剂,又是工业生产中的一种重要原料。
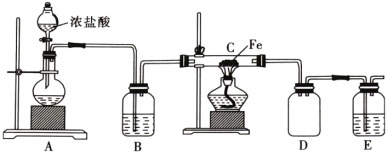
(1)实验室中利用铁屑与氯气反应制备 ,实验装置如图所示。
,实验装置如图所示。
①实验开始前,首先应________________________ 。
②盛浓盐酸的仪器的名称为________ 。
③装置A中观察到溶液紫色变浅,则发生反应的离子方程式为________________ ,还原剂为________ (填化学式,下同),氧化产物为________ 。
④每生成 时,消耗的
时,消耗的 为
为________ L (标准状况下),转移的电子数为________  。
。
(2)E中所盛装的试剂为________ (填“氢氧化钙”或“氢氧化钠”)溶液,原因是________________________ 。

(1)实验室中利用铁屑与氯气反应制备
 ,实验装置如图所示。
,实验装置如图所示。①实验开始前,首先应
②盛浓盐酸的仪器的名称为
③装置A中观察到溶液紫色变浅,则发生反应的离子方程式为
④每生成
 时,消耗的
时,消耗的 为
为 。
。(2)E中所盛装的试剂为
您最近一年使用:0次
2 . W、X、Y、Z均为短周期主族元素。W-与氦原子的电子层结构相同,X的单质是空气中体积分数最大的气体,Y是地壳中含量最多的元素,Y与Z同主族。下列说法正确的是
A.原子半径: |
| B.W、X、Y三种元素只能组成共价化合物 |
| C.Z的氧化物对应水化物的酸性一定比X的强 |
| D.某种化合物中可能同时存在W、X、Y、Z四种元素 |
您最近一年使用:0次
3 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A. 与 与 在一定条件下反应,每生成 在一定条件下反应,每生成 时,转移的电子数为 时,转移的电子数为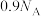 |
B.标准状况下, 的分子数目为 的分子数目为 |
C. 的 的 溶液中,所含 溶液中,所含 的数目为 的数目为 |
D. 熔融状态下的 熔融状态下的 晶体中,所含离子数目为 晶体中,所含离子数目为 |
您最近一年使用:0次
4 . 向Na2S和Na2SO3的混合溶液中加入足量的稀硫酸,可发生以下反应: 。下列说法不正确的是
。下列说法不正确的是
 。下列说法不正确的是
。下列说法不正确的是| A.单质S既是氧化产物又是还原产物 |
| B.该反应中稀硫酸只体现酸性 |
| C.氧化剂与还原剂的物质的量之比为2:1 |
D. |
您最近一年使用:0次
2021-07-15更新
|
145次组卷
|
2卷引用:贵州省黔西南州2020-2021学年高二下学期期末检测理科化学试题
5 . 室温下,下列各组离子在指定溶液中能大量共存的是
A.pH=2的溶液中: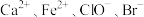 |
B.澄清透明的溶液中: |
C. 的HI溶液中: 的HI溶液中: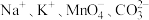 |
D.含有大量 的溶液中: 的溶液中: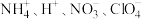 |
您最近一年使用:0次
2021-07-15更新
|
238次组卷
|
2卷引用:贵州省黔西南州2020-2021学年高二下学期期末检测理科化学试题
解题方法
6 . “氯水是浅黄绿色的液体”,且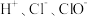 的水溶液均为无色,下列说法中正确的是
的水溶液均为无色,下列说法中正确的是
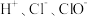 的水溶液均为无色,下列说法中正确的是
的水溶液均为无色,下列说法中正确的是A.氯水中的反应可表示为: |
| B.将氯水滴入KI溶液中,溶液变为棕黄色 |
C.氯水的漂白性是 的氧化性所致 的氧化性所致 |
| D.氯水在实验室中可以长期保存 |
您最近一年使用:0次
7 . 短周期主族元素W、X、Y、Z的原子序数依次增大,W的一种核素无中子,X的最高正价与最低负价代数和为2,Y与W同主族,Z原子的电子层数与最外层电子数相等。下列推断正确的是
A.原子半径: |
| B.Z的氧化物是两性氧化物 |
C.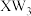 的水溶液呈酸性 的水溶液呈酸性 |
D.最高价氧化物对应的水化物的碱性: |
您最近一年使用:0次
8 . 下列化学反应离子方程式正确的是
| A.向滴有酚酞的NaOH溶液中加入醋酸:H++OH−=H2O |
| B.向硫酸铜溶液中滴加氢氧化钡溶液:Cu2++2OH−=Cu(OH)2↓ |
| C.向淀粉KI溶液中通入适量Cl2:Cl2+2I−=2Cl−+I2 |
| D.向FeCl3溶液中加入铁粉:Fe3++Fe=2Fe2+ |
您最近一年使用:0次
9 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.常温常压下,16g  中含有C-H键数目为4 中含有C-H键数目为4 |
B.标准状况下,22.4L  中含有原子数目为5 中含有原子数目为5 |
C.1mol  与足量铁反应转移电子数为3 与足量铁反应转移电子数为3 |
D.1L 0.1  溶液中含有 溶液中含有 数目为0.1 数目为0.1 |
您最近一年使用:0次
18-19高二上·江西九江·阶段练习
名校
10 . 由下列实验及现象推出的相应结论正确的是
| 实验 | 现象 | 结论 |
| A.某溶液中滴加K3[Fe(CN)6]溶液 | 产生蓝色沉淀 | 原溶液中有Fe2+,无Fe3+ |
| B.向Na2SiO3溶液中通入CO2 | 溶液变浑浊 | 酸性:H2CO3> H2SiO3 |
| C.向含有ZnS和Na2S的悬浊液中滴加CuSO4溶液 | 生成黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
| D.①某溶液中加入Ba(NO3)2溶液 ②再加足量盐酸 | ①产生白色沉淀 ②仍有白色沉淀 | 原溶液中有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



