名校
解题方法
1 . 已知短周期元素M、N、X、Y、Z分布在三个周期,N、X最外层电子数相同,物质A由原子序数依次增大的元素X、Y、Z组成,其中Z的简单离子半径在同周期中最小,X、Y、Z简单离子的核外电子排布相同,物质A的结构式如下图所示:
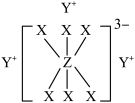
回答下列问题:
(1)请写出YM的电子式:_______ 。
(2)N、X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示):_______ 。
(3)在YZO2与YX的混合液中,通入足量CO2,是工业制取A的一种方法,写出该反应的化学方程式:_______ 。
(4)镓(31Ga)与Z为同主族元素,氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列有关说法正确的是_______ 。
a. Ga位于元素周期表第四周期IVA族
b. GaN为新型无机非金属材料
c. Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
d. 酸性:H3AsO4>H3PO4>HNO3
(5)YZM4是有机合成的重要还原剂,其合成路线如图所示

利用YZM4遇水反应生成的氢气的体积测定YZM4样品纯度。
①其反应的化学方程式为_______ 。
②现设计如图四种装置测定YZM4样品的纯度(假设杂质不参与反应)。
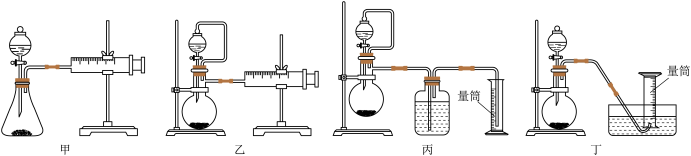
从简约性、准确性考虑,最适宜的方案是_______ (填编号)。
③取样品ag,若实验测得氢气的体积为V L(标准状态),则YZM4样品纯度为_______ (用代数式表示)。

回答下列问题:
(1)请写出YM的电子式:
(2)N、X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示):
(3)在YZO2与YX的混合液中,通入足量CO2,是工业制取A的一种方法,写出该反应的化学方程式:
(4)镓(31Ga)与Z为同主族元素,氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列有关说法正确的是
a. Ga位于元素周期表第四周期IVA族
b. GaN为新型无机非金属材料
c. Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
d. 酸性:H3AsO4>H3PO4>HNO3
(5)YZM4是有机合成的重要还原剂,其合成路线如图所示

利用YZM4遇水反应生成的氢气的体积测定YZM4样品纯度。
①其反应的化学方程式为
②现设计如图四种装置测定YZM4样品的纯度(假设杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是
③取样品ag,若实验测得氢气的体积为V L(标准状态),则YZM4样品纯度为
您最近一年使用:0次
名校
解题方法
2 . 丙烯酸酯类物质广泛用于建筑、包装材料等,丙烯酸是合成丙烯酸酯的原料之一。丙烯醇可用于生产甘油、塑料等。以丙烯醛为原料生产丙烯醇、丙烯酸的流程如图所示:

已知:
①2CH2=CH-CHO+NaOH CH2=CHCH2OH+CH2=CHCOONa
CH2=CHCH2OH+CH2=CHCOONa
②2CH2=CHCOONa+H2SO4→2CH2=CHCOOH+Na2SO4
③有关物质的相关性质如表:
(1)操作①需要连续加热30min,所用装置如图所示。仪器L名称是________ 。

(2)操作②使用的主要仪器是分液漏斗,在使用之前需进行的操作是___ 。
(3)操作④包括____ 、过滤、冰水洗涤、低温吸干。
(4)操作⑤中,加热蒸馏“下层液体”,分离出四氯化碳;再分离出丙烯醇(如图),要得到丙烯醇应收集____ (填温度)的馏分。图中有一处明显错误,应改为____ 。

(5)测定丙烯醇的摩尔质量:准确量取amL丙烯醇于分液漏斗中,烧瓶内盛装足量钠粒。实验前量气管B中读数为b mL,当丙烯醇完全反应后,冷却至室温、调平B、C液面,量气管B的读数为c mL。已知室温下气体摩尔体积为VL·mol-1。

调平B、C液面的操作是____ ;实验测得丙烯醇的摩尔质量为____ g·mol-1(用代数式表示)。如果读数时C管液面高于B管,测得结果将____ (填“偏大”“偏小”或“不变”)。

已知:
①2CH2=CH-CHO+NaOH
 CH2=CHCH2OH+CH2=CHCOONa
CH2=CHCH2OH+CH2=CHCOONa②2CH2=CHCOONa+H2SO4→2CH2=CHCOOH+Na2SO4
③有关物质的相关性质如表:
| 物质 | 丙烯醛 | 丙烯醇 | 丙烯酸 | 四氯化碳 |
| 沸点/℃ | 53 | 97 | 141 | 77 |
| 熔点/℃ | - 87 | - 129 | 13 | -22.8 |
| 密度/g·mL-3 | 0.84 | 0.85 | 1.02 | 1.58 |
| 溶解性(常温) | 易溶于水和有机溶剂 | 溶于水和有机溶剂 | 溶于水和有机溶剂 | 难溶于水 |

(2)操作②使用的主要仪器是分液漏斗,在使用之前需进行的操作是
(3)操作④包括
(4)操作⑤中,加热蒸馏“下层液体”,分离出四氯化碳;再分离出丙烯醇(如图),要得到丙烯醇应收集

(5)测定丙烯醇的摩尔质量:准确量取amL丙烯醇于分液漏斗中,烧瓶内盛装足量钠粒。实验前量气管B中读数为b mL,当丙烯醇完全反应后,冷却至室温、调平B、C液面,量气管B的读数为c mL。已知室温下气体摩尔体积为VL·mol-1。

调平B、C液面的操作是
您最近一年使用:0次
2020-04-13更新
|
545次组卷
|
8卷引用:江西省吉安市安福二中、井大附中、吉安县三中、遂川二中2021-2022学年高二下学期四校联考第三次月考化学试题
江西省吉安市安福二中、井大附中、吉安县三中、遂川二中2021-2022学年高二下学期四校联考第三次月考化学试题江西省景德镇一中2020-2021学年高二下学期期末考试化学(2班)试题湖北省武汉市第十一中学2021-2022学年高二下学期6月月考化学试题(已下线)第29讲 化学综合实验(讲)-2023年高考化学一轮复习讲练测(全国通用)三湘名校教育联盟●2020届高三第二次大联考(全国I卷)理综化学试题(已下线)第29讲 化学综合实验(精讲)-2022年一轮复习讲练测云南省罗平县第二中学2021-2022学年高二上学期9月月考化学试题(已下线)专题讲座(十)化学实验设计与探究(练) — 2022年高考化学一轮复习讲练测(新教材新高考)



