名校
解题方法
1 . 利用下图,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:

(1)丙的化学式为_______ ;丁属于_______ (“酸性”或“碱性”)氧化物。
(2)根据氯元素的化合价判断,乙物质的性质_______ (填标号)。
a.只有氧化性
b.既有氧化性又有还原性
c.只有还原性
(3)物质己的化学式为HClO4,电解甲溶液制备己的化学反应为: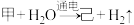 (未配平),配平后参与反应的甲与H2O的微粒个数之比是
(未配平),配平后参与反应的甲与H2O的微粒个数之比是_______ 。
(4)庚是家庭中常用消毒液的有效成分NaClO,用乙制取庚的化学方程式为_______ 。庚与洁厕灵(主要成分盐酸)同时使用会产生有毒的氯气,写出反应的离子方程式:_______ 。
(5)辛在MnO2催化下受热分解可用于制备氧气,每生成1.204×1024个氧气分子,转移e-的物质的量为_______ 。
(6)工业上可以用草酸(H2C2O4,二元弱酸)还原辛的方法生产丙,草酸被氧化为CO2,请写出该反应的离子方程式_______ 。

(1)丙的化学式为
(2)根据氯元素的化合价判断,乙物质的性质
a.只有氧化性
b.既有氧化性又有还原性
c.只有还原性
(3)物质己的化学式为HClO4,电解甲溶液制备己的化学反应为:
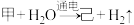 (未配平),配平后参与反应的甲与H2O的微粒个数之比是
(未配平),配平后参与反应的甲与H2O的微粒个数之比是(4)庚是家庭中常用消毒液的有效成分NaClO,用乙制取庚的化学方程式为
(5)辛在MnO2催化下受热分解可用于制备氧气,每生成1.204×1024个氧气分子,转移e-的物质的量为
(6)工业上可以用草酸(H2C2O4,二元弱酸)还原辛的方法生产丙,草酸被氧化为CO2,请写出该反应的离子方程式
您最近一年使用:0次
名校
解题方法
2 . 储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,此反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、Cr2(SO4)3、K2SO4、H2O七种物质。
(1)若将碳纳米颗粒分散到一定溶剂中,形成稳定的分散系,其所具有的性质是_______ 。
①丁达尔效应 ②加入饱和(NH4)2SO4溶液产生聚沉 ③可通过半透膜
(2)化学方程式为:3C+ 2K2Cr2O7 + 8H2SO4= 2K2SO4+ 3CO2 ↑ + 2Cr2(SO4)3+ 8H2O。
①H2SO4在上述反应中表现出来的性质是_______ (填选项编号)。
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
②上述反应中电子由_______ 转移给_______ (都填化学式)
(1)若将碳纳米颗粒分散到一定溶剂中,形成稳定的分散系,其所具有的性质是
①丁达尔效应 ②加入饱和(NH4)2SO4溶液产生聚沉 ③可通过半透膜
(2)化学方程式为:3C+ 2K2Cr2O7 + 8H2SO4= 2K2SO4+ 3CO2 ↑ + 2Cr2(SO4)3+ 8H2O。
①H2SO4在上述反应中表现出来的性质是
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
②上述反应中电子由
您最近一年使用:0次
名校
3 . 下列排列顺序不正确的是:①沸点: ②氧化性:
②氧化性: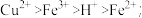 ③
③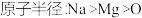 ④还原性:
④还原性: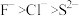 ⑤结合
⑤结合 的能力:
的能力: ⑥酸性:
⑥酸性: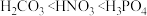
 ②氧化性:
②氧化性: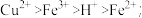 ③
③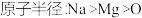 ④还原性:
④还原性: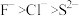 ⑤结合
⑤结合 的能力:
的能力: ⑥酸性:
⑥酸性: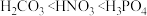
| A.②④⑥ | B.①②③ | C.③⑤ | D.②④⑤ |
您最近一年使用:0次
2022-12-02更新
|
244次组卷
|
7卷引用:江西省景德镇市第一中学2021-2022学年高一上学期期末化学试题
名校
4 . 氯气是一种重要的化工原料,在生产生活中具有广泛的应用。
(1)实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
①写出实验室制取氯气的化学方程式_______ 。若产生标准状况下4.48 LCl2,则反应过程中被氧化的HCl的物质的量是_______ mol。
②为了防止氯气污染环境,需将剩余氯气通入_______ ,发生的化学反应方程式_______ 。
③实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下: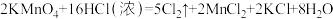 。在此反应中浓盐酸中显示出来的性质是
。在此反应中浓盐酸中显示出来的性质是_______ (填写字母)
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)电解饱和食盐水生产氢气、氯气、氢氧化钠,氯气与石灰乳反应可制取漂白粉。干燥的漂白粉不能发挥漂白效果,请写出漂白粉能发挥漂白效果的化学反应方程式_______ 。
(1)实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
①写出实验室制取氯气的化学方程式
②为了防止氯气污染环境,需将剩余氯气通入
③实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
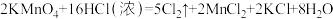 。在此反应中浓盐酸中显示出来的性质是
。在此反应中浓盐酸中显示出来的性质是A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)电解饱和食盐水生产氢气、氯气、氢氧化钠,氯气与石灰乳反应可制取漂白粉。干燥的漂白粉不能发挥漂白效果,请写出漂白粉能发挥漂白效果的化学反应方程式
您最近一年使用:0次
名校
5 . 下表是元素周期表的一部分,针对表中的 元素,用元素符号或化学式填空回答以下问题:
元素,用元素符号或化学式填空回答以下问题:
(1)元素①、②的简单氢化物中的稳定性最强的是_______  用化学式表示
用化学式表示 ;
;
(2)元素的最高价氧化物对应的水化物中酸性最强的是_______ ,碱性最强的是_______ ,元素③的最高价氧化物对应水化物中含有的化学键类型为_______ ;
(3)在③④⑤⑦四种元素中,简单离子半径最小的是_______ ;
(4) 的电子式为
的电子式为_______ ; 的电子式为
的电子式为_______ ;
(5)在⑦与⑩的单质中,氧化性较强的是_______ ,用化学反应方程式证明:_______ 。
 元素,用元素符号或化学式填空回答以下问题:
元素,用元素符号或化学式填空回答以下问题: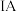 | 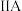 | 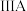 | 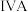 | 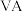 | 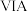 |  |  | |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 用化学式表示
用化学式表示 ;
;(2)元素的最高价氧化物对应的水化物中酸性最强的是
(3)在③④⑤⑦四种元素中,简单离子半径最小的是
(4)
 的电子式为
的电子式为 的电子式为
的电子式为(5)在⑦与⑩的单质中,氧化性较强的是
您最近一年使用:0次
6 . 化学上常用标准电极电势数据φθ(氧化型/还原型)比较物质氧化能力。φθ值越高,氧化型物质氧化能力越强,φθ值与体系pH有关。利用表格所给数据分析,以下说法错误的是
| 氧化型/还原型 | φθ(Co3+/Co2+) | φθ(HClO/Cl— |
| 酸性介质 | 1.84V | 1.49V |
| 氧化型/还原型 | φθ[Co(OH)3/Co(OH)2] | φθ(ClO—/Cl—) |
| 碱性介质 | 0.17V | x |
| A.推测:x<1.49V |
| B.Co3O4与浓盐酸发生反应:Co3O4+8H+=Co2++2Co3++4H2O |
| C.若x=0.81V,碱性条件下可发生反应:2Co(OH)2+NaClO+H2O=2Co(OH)3+NaCl |
| D.从图中数据可知氧化型物质的氧化性随着溶液酸性增强而增强 |
您最近一年使用:0次
2022-02-22更新
|
2301次组卷
|
14卷引用:江西省新余市第一中学2022-2023学年高三上学期新生入学考试化学试题
江西省新余市第一中学2022-2023学年高三上学期新生入学考试化学试题河南省信阳市2022届高三第二次质量检测化学试题(已下线)专题04氧化还原反应-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题04氧化还原反应-2022年高考真题+模拟题汇编(全国卷)(已下线)专题04氧化还原反应-三年(2020~2022)高考真题汇编(全国卷)湖南省长沙市雅礼中学2021-2022学年高三下学期5月模拟考试(二)化学试题(已下线)专题03 氧化还原反应-备战2023年高考化学母题题源解密(全国通用)广东省广州市真光中学2022-2023学年高一上学期期中考化学试题湖南省株洲市九方中学2022-2023学年高一上学期期中考试化学试题河北省衡水中学2023届高三上学期三调考试化学试题辽宁省沈阳市回民中学2022-2023学年高一上学期期末线上考试化学试题河北省石家庄二中教育集团2022-2023学年度高一年级上学期期末考试化学试题辽宁省大连市第二十四中学2023-2024学年高一上学期第二次统测化学试卷 浙江省杭州第十四中学2023-2024学年高一上学期期中阶段性测试化学试题
7 . 铁是人体必需的微量元素,严重缺铁时需要服用补铁剂。实验小组为研究某补铁剂中铁元素的价态,设计并进行了如下实验:
【资料】Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为-2价,通常被氧化为+6价

将补铁剂碾碎的目的是增大接触面积,使其充分溶解。
(1)试剂1是_______ (填名称),试剂2是_______ (填名称)。
(2)加入试剂2后溶液变为浅红色,说明溶液①中含有_______ (填离子符号)。
(3)能证明溶液①中含有Fe2+的实验现象是_______ 。
(4)写出在上述条件下Fe2+与NaClO发生反应的离子方程式:_______ 。
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的 与NaClO发生了化学反应。
与NaClO发生了化学反应。
a.甲同学猜测的依据是_______ 。
b.乙同学通过实验证实了甲同学的猜测,其实验方案及现象是_______ 。
【资料】Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为-2价,通常被氧化为+6价

将补铁剂碾碎的目的是增大接触面积,使其充分溶解。
(1)试剂1是
(2)加入试剂2后溶液变为浅红色,说明溶液①中含有
(3)能证明溶液①中含有Fe2+的实验现象是
(4)写出在上述条件下Fe2+与NaClO发生反应的离子方程式:
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的
 与NaClO发生了化学反应。
与NaClO发生了化学反应。a.甲同学猜测的依据是
b.乙同学通过实验证实了甲同学的猜测,其实验方案及现象是
您最近一年使用:0次
名校
8 . 回答下列问题
(1)火药是中国的“四大发明”之一,黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑,其中被氧化的元素是___________ (填元素名称)。
(2)人体内的铁元素是以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转换成Fe2+,有利于人体吸收,说明维生素C具有___________ (填“氧化性”或“还原性”)。
(3)工业废水中含有的重铬酸根离子(Cr2O )有毒,必须处理达标后才能排放。工业上常用明矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放。工业上常用明矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O,在该反应中,氧化剂是
+14H+=6Fe3++2Cr3++7H2O,在该反应中,氧化剂是___________ (填离子符号,下同),被氧化的是___________ 。
(4)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式___________ 。
(1)火药是中国的“四大发明”之一,黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑,其中被氧化的元素是
(2)人体内的铁元素是以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转换成Fe2+,有利于人体吸收,说明维生素C具有
(3)工业废水中含有的重铬酸根离子(Cr2O
 )有毒,必须处理达标后才能排放。工业上常用明矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放。工业上常用明矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O,在该反应中,氧化剂是
+14H+=6Fe3++2Cr3++7H2O,在该反应中,氧化剂是(4)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式
您最近一年使用:0次
9 . 已知:①2KMnO4+16HCl=2KC1+2MnCl2+5Cl2↑+8H2O;② Cl2+2FeCl2=2FeCl3;③ 2KI+2FeCl3=2KCl+I2+2FeCl2则下列判断正确的是
A.氧化性: >Fe3+>I2 >Fe3+>I2 | B.还原性:I->Cl->Fe2+ |
| C.Fe3+只有氧化性,Fe2+只有还原性 | D.由信息推测:2Cl-+I2=Cl2+2I-反应可以进行 |
您最近一年使用:0次
2022-12-08更新
|
104次组卷
|
2卷引用:江西省南昌市进贤县第二中学2022-2023学年高一上学期第一次月考化学试题
10 . 回答下列问题:
(1)氮元素在元素周期表中的位置为_____ 。
(2)氮元素简单气态氢化物的电子式为_____ 。
与氮元素同主族的磷元素化合物有如下反应,其中反应物有:PH3、H2SO4、KClO3;生成物有:K2SO4、H3PO4、H2O和一种未知物质X。
(3)已知KClO3在反应中得到电子,则该反应的还原剂是_____ 。
(4)已知0.2molKClO3在反应中得到1mol电子生成X,则X的化学式为_____ 。
(5)完成并配平上述反应的化学方程式_____ 。
(6)根据上述氧化还原反应原理可推知_____ 。(填序号)
(7)在该反应中转移电子2mol时,生成H3PO4_____ mol。
(1)氮元素在元素周期表中的位置为
(2)氮元素简单气态氢化物的电子式为
与氮元素同主族的磷元素化合物有如下反应,其中反应物有:PH3、H2SO4、KClO3;生成物有:K2SO4、H3PO4、H2O和一种未知物质X。
(3)已知KClO3在反应中得到电子,则该反应的还原剂是
(4)已知0.2molKClO3在反应中得到1mol电子生成X,则X的化学式为
(5)完成并配平上述反应的化学方程式
(6)根据上述氧化还原反应原理可推知
| A.氧化性:KClO3>H3PO4 | B.氧化性:KClO3>H2O |
| C.还原性:PH3>X | D.还原性:PH3>K2SO4 |
您最近一年使用:0次



