名校
1 . 某课外活动小组设计实验验证二氧化碳跟过氧化钠反应时需要与水接触。下列说法中正确的是
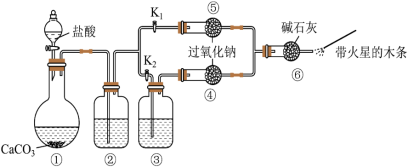

| A.装置①中盐酸不能换成硫酸 |
B.装置②中的试剂是饱和 溶液 溶液 |
C.打开弹簧夹 ,关闭 ,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条复燃 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条复燃 |
| D.上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应 |
您最近一年使用:0次
2022-12-07更新
|
193次组卷
|
2卷引用:江西省九江市同文中学2022-2023学年高一上学期期中考试化学试题
解题方法
2 . 下列关于钠及其化合物的说法中错误的是
| A.碳酸氢钠药片是抗酸药,服用时喝些醋能提高药效 |
B. 与 与 反应放出氧气,可用于制作呼吸面具 反应放出氧气,可用于制作呼吸面具 |
| C.分别将少量钠投入到盛有水和乙醇的烧杯中,可比较水与乙醇中氢的活泼性 |
D.用铂丝蘸取某溶液灼烧,火焰呈黄色,证明其中含有 |
您最近一年使用:0次
名校
3 . 食盐中所加的碘以碘酸钾(KIO3)形式存在。根据反应:IO +I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO
+I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO 。下列说法不正确的是
。下列说法不正确的是
 +I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO
+I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO 。下列说法不正确的是
。下列说法不正确的是| A.上述反应中氧化剂和还原剂的物质的量之比为1∶5 |
| B.实验时可观察到试纸变蓝 |
| C.实验可证明该条件下I-的还原性强于Cl- |
| D.食醋中含有的乙酸是强酸,它能提供反应所需的H+ |
您最近一年使用:0次
2020-07-04更新
|
324次组卷
|
5卷引用:江西省南昌市豫章中学20212-2022学年高一下学期第一次月考化学试题
江西省南昌市豫章中学20212-2022学年高一下学期第一次月考化学试题北京市东城区北京景山学校2019~2020学年高一下学期期末考试化学试题贵州省铜仁市伟才学校2019-2020学年高一下学期期末考试化学(理)试题黑龙江省大庆市肇州县第二中学2019-2020学年高一下学期期末考试化学试题(已下线)1.3.4 氧化还原反应方程式的配平-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)
名校
解题方法
4 . 实验室以锈蚀程度很大的废铁屑为原料制备 晶体的流程如下:
晶体的流程如下: 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀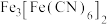 。回答下列问题:
。回答下列问题:
(1)“酸溶”过程中发生的主要反应有:① ;
;
②___________ (用离子方程式表示)
③___________ (用离子方程式表示)
(2)“酸溶”需控制温度在 左右,最佳的加热方式为
左右,最佳的加热方式为___________ 。
(3)“过滤”需要的玻璃仪器除烧杯外还有___________ 。
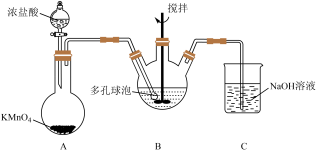
(4)“氧化”过程可在下图所示装置中进行。___________ 。
②装置 中发生的反应离子方程式为
中发生的反应离子方程式为___________ 。
③B中使用多孔球泡的作用是___________ 。
④证明装置 溶液中
溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是___________ 。
 晶体的流程如下:
晶体的流程如下:
 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀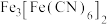 。回答下列问题:
。回答下列问题:(1)“酸溶”过程中发生的主要反应有:①
 ;
;②
③
(2)“酸溶”需控制温度在
 左右,最佳的加热方式为
左右,最佳的加热方式为(3)“过滤”需要的玻璃仪器除烧杯外还有
(4)“氧化”过程可在下图所示装置中进行。
②装置
 中发生的反应离子方程式为
中发生的反应离子方程式为③B中使用多孔球泡的作用是
④证明装置
 溶液中
溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是
您最近一年使用:0次
5 . A、B、C、D几种纯净物至少含一种共同的元素,它们之间有如下转化关系(部分条件和产物省略)。

回答下列问题:
(1)若A为金属单质,C为浅黄色粉末,Y为液态氧化物(常温常压),则B的化学式为___________ 。C→D的离子方程式为___________ 。
(2)若A是酸性氧化物,向空气中大量排放A,会加剧温室效应的形成,强碱X的焰色呈黄色,则B的化学式为___________ ,X的电离方程式为___________ 。
(3)若A是非金属单质,C是光合作用的原料,A和C在高温下生成B,该反应中氧化产物、还原产物的质量之比为___________ 。
(4)若A为黄绿色气体,X为金属单质,B为X在A中燃烧生成的棕褐色烟,为探究C中阳离子具有还原性,设计如下方案:
取适量的C固体溶于水,将溶液分成甲、乙、丙三份,进行如下实验:
①能证明C中阳离子具有还原性的实验是___________ (填代号)。
②丙实验中溶液由无色变红色的原因是___________ (用离子方程式表示)。

回答下列问题:
(1)若A为金属单质,C为浅黄色粉末,Y为液态氧化物(常温常压),则B的化学式为
(2)若A是酸性氧化物,向空气中大量排放A,会加剧温室效应的形成,强碱X的焰色呈黄色,则B的化学式为
(3)若A是非金属单质,C是光合作用的原料,A和C在高温下生成B,该反应中氧化产物、还原产物的质量之比为
(4)若A为黄绿色气体,X为金属单质,B为X在A中燃烧生成的棕褐色烟,为探究C中阳离子具有还原性,设计如下方案:
取适量的C固体溶于水,将溶液分成甲、乙、丙三份,进行如下实验:
| 实验 | 操作 | 现象 |
| 甲 | 加入镁粉 | 溶液颜色逐渐变为无色 |
| 乙 | 依次滴加KSCN溶液、新制氯水 | 开始不变色,后变红色 |
| 丙 | 先滴加KSCN溶液,后滴加酸化的双氧水 | 开始不变色,后变红色 |
②丙实验中溶液由无色变红色的原因是
您最近一年使用:0次
名校
解题方法
6 . 央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是__________ 价。 是一种酸根离子,则
是一种酸根离子,则 属于
属于__________ (填“酸”、“碱”、“盐”或“氧化物”)。
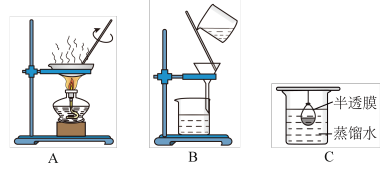
(2)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的__________ (填序号)。
(3)现有10mL明胶的水溶液与5mLK2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜:
能够透过半透膜:_____________________ ;该检验过程中发生的离子方程式为____________________ 。
(1)已知
 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是 是一种酸根离子,则
是一种酸根离子,则 属于
属于(2)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的

(3)现有10mL明胶的水溶液与5mLK2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
 能够透过半透膜:
能够透过半透膜:
您最近一年使用:0次
7 . 铁是人体必需的微量元素,严重缺铁时需要服用补铁剂。实验小组为研究某补铁剂中铁元素的价态,设计并进行了如下实验:
【资料】Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为-2价,通常被氧化为+6价

将补铁剂碾碎的目的是增大接触面积,使其充分溶解。
(1)试剂1是_______ (填名称),试剂2是_______ (填名称)。
(2)加入试剂2后溶液变为浅红色,说明溶液①中含有_______ (填离子符号)。
(3)能证明溶液①中含有Fe2+的实验现象是_______ 。
(4)写出在上述条件下Fe2+与NaClO发生反应的离子方程式:_______ 。
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的 与NaClO发生了化学反应。
与NaClO发生了化学反应。
a.甲同学猜测的依据是_______ 。
b.乙同学通过实验证实了甲同学的猜测,其实验方案及现象是_______ 。
【资料】Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为-2价,通常被氧化为+6价

将补铁剂碾碎的目的是增大接触面积,使其充分溶解。
(1)试剂1是
(2)加入试剂2后溶液变为浅红色,说明溶液①中含有
(3)能证明溶液①中含有Fe2+的实验现象是
(4)写出在上述条件下Fe2+与NaClO发生反应的离子方程式:
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的
 与NaClO发生了化学反应。
与NaClO发生了化学反应。a.甲同学猜测的依据是
b.乙同学通过实验证实了甲同学的猜测,其实验方案及现象是
您最近一年使用:0次
解题方法
8 . 向胶体中加入电解质能使胶体聚沉,使一定量的胶体溶液在一定时间内开始聚沉所需电解质的浓度(mol/L)称作“聚沉值”,电解质“聚沉值”越小,则表示其聚沉能力越大,实验证明:聚沉能力主要取决于与胶体所带相反电荷的离子所带电荷数,电荷数越大,聚沉能力越大。向 胶体中加入下列电解质时,其“聚沉值”最大的是
胶体中加入下列电解质时,其“聚沉值”最大的是
 胶体中加入下列电解质时,其“聚沉值”最大的是
胶体中加入下列电解质时,其“聚沉值”最大的是A. | B. | C.CsCl | D. |
您最近一年使用:0次
解题方法
9 . Liepatoff规则:胶核总选择性吸附与其本身组成相似的离子形成胶粒。例如, 溶于水形成胶体粒子,
溶于水形成胶体粒子, 胶核选择性吸附
胶核选择性吸附 形成胶粒并带正电荷。下列叙述正确的是
形成胶粒并带正电荷。下列叙述正确的是

 溶于水形成胶体粒子,
溶于水形成胶体粒子, 胶核选择性吸附
胶核选择性吸附 形成胶粒并带正电荷。下列叙述正确的是
形成胶粒并带正电荷。下列叙述正确的是
| A.氢氧化铁胶体可用于饮用水消毒和净化 |
| B.丁达尔现象能证明氢氧化铁胶粒带电荷 |
C. 溶胶中吸附的阳离子总数大于阴离子总数 溶胶中吸附的阳离子总数大于阴离子总数 |
D.利用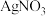 和 和 制 制 胶体,若 胶体,若 过量,则胶粒带负电荷 过量,则胶粒带负电荷 |
您最近一年使用:0次
10 . 铁是人类较早使用的金属之一,运用所学知识,回答下列问题。电子工业常用 30%的 FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中存在Fe3+的试剂是_______ (填化学式)溶液,证明 Fe3+存在的现象是_______ 。
(2)写出 FeCl3溶液与金属铜发生反应的离子方程式_______ 。
(3)某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:
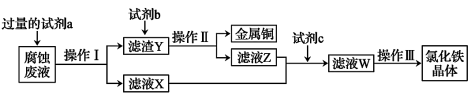
回答下列问题:
①试剂a是_______ ,操作I用到的玻璃仪器有烧杯、玻璃棒和_______ 。
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为_______ 。
③上述流程中操作III包括_______ 、过滤、洗涤。
(1)检验溶液中存在Fe3+的试剂是
(2)写出 FeCl3溶液与金属铜发生反应的离子方程式
(3)某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
①试剂a是
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为
③上述流程中操作III包括
您最近一年使用:0次



