名校
1 . 某课外活动小组设计实验验证二氧化碳跟过氧化钠反应时需要与水接触。下列说法中正确的是
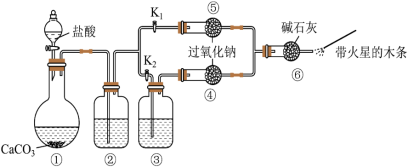

| A.装置①中盐酸不能换成硫酸 |
B.装置②中的试剂是饱和 溶液 溶液 |
C.打开弹簧夹 ,关闭 ,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条复燃 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条复燃 |
| D.上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应 |
您最近一年使用:0次
2022-12-07更新
|
191次组卷
|
2卷引用:江西省九江市同文中学2022-2023学年高一上学期期中考试化学试题
2 . 下列关于离子检验的说法正确的是
A.向某无色溶液中加入BaCl2溶液,有白色沉淀生成,再加入稀盐酸,沉淀不消失,证明溶液中一定含有 |
B.向某无色溶液中加入少量稀氢氧化钠溶液后,用湿润的红色石蕊试纸靠近试管口,若试纸不变蓝,则说明该溶液中无 |
C.向某溶液中滴入足量盐酸,观察到产生的气体能使澄清石灰水变浑浊,证明溶液中一定有 或 或 |
| D.透过蓝色钴玻璃能观察到紫色火焰,则一定有钾元素,可能含有钠元素 |
| E.将灼热的木炭与浓硝酸反应产生的气体缓缓通入澄清石灰水中,溶液中没有沉淀产生 |
您最近一年使用:0次
解题方法
3 . 下列关于钠及其化合物的说法中错误的是
| A.碳酸氢钠药片是抗酸药,服用时喝些醋能提高药效 |
B. 与 与 反应放出氧气,可用于制作呼吸面具 反应放出氧气,可用于制作呼吸面具 |
| C.分别将少量钠投入到盛有水和乙醇的烧杯中,可比较水与乙醇中氢的活泼性 |
D.用铂丝蘸取某溶液灼烧,火焰呈黄色,证明其中含有 |
您最近一年使用:0次
4 . 关于常见金属及其化合物,下列说法不正确的是
| A.人类利用金属的历史顺序(铜→铁→铝)主要受地壳中金属元素含量的影响 |
| B.等质量的钠分别在常温和加热条件下与氧气充分反应,失去的电子一样多 |
| C.常温常压下,等质量铝片分别与足量盐酸和烧碱溶液反应,放出气体体积相同 |
| D.常温下,Na可以与水反应,证明Na比Fe更活泼 |
您最近一年使用:0次
2022-01-23更新
|
170次组卷
|
2卷引用:江西省抚州市2021-2022学年高一上学期期末学业质量检测化学试题
名校
解题方法
5 . 下列说法正确的有
①在周期表中,同周期第ⅡA族和第ⅢA族元素质子数相差可能是1、11或25
②同主族元素从上至下,单质的氧化性逐渐减弱,熔点逐渐降低
③碱性:LiOH>NaOH>KOH>RbOH
④酸性:H2SO4>HClO4>HBrO4>HIO4
⑤卤族元素由上至下,阴离子的还原性增强,单质的颜色加深
⑥碱金属单质物理通性是硬度小,密度小,熔点低
⑦碱金属元素的原子半径和离子半径都随核电荷数的增大而增大
⑧可以利用非金属单质与H2反应的难易程度来证明其元素非金属性的强弱
①在周期表中,同周期第ⅡA族和第ⅢA族元素质子数相差可能是1、11或25
②同主族元素从上至下,单质的氧化性逐渐减弱,熔点逐渐降低
③碱性:LiOH>NaOH>KOH>RbOH
④酸性:H2SO4>HClO4>HBrO4>HIO4
⑤卤族元素由上至下,阴离子的还原性增强,单质的颜色加深
⑥碱金属单质物理通性是硬度小,密度小,熔点低
⑦碱金属元素的原子半径和离子半径都随核电荷数的增大而增大
⑧可以利用非金属单质与H2反应的难易程度来证明其元素非金属性的强弱
| A.4个 | B.5个 | C.6个 | D.7个 |
您最近一年使用:0次
2021-12-03更新
|
348次组卷
|
2卷引用:江西省丰城中学2022-2023学年高一上学期期中考试化学试题(创新班)
名校
6 . 食盐中所加的碘以碘酸钾(KIO3)形式存在。根据反应:IO +I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO
+I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO 。下列说法不正确的是
。下列说法不正确的是
 +I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO
+I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO 。下列说法不正确的是
。下列说法不正确的是| A.上述反应中氧化剂和还原剂的物质的量之比为1∶5 |
| B.实验时可观察到试纸变蓝 |
| C.实验可证明该条件下I-的还原性强于Cl- |
| D.食醋中含有的乙酸是强酸,它能提供反应所需的H+ |
您最近一年使用:0次
2020-07-04更新
|
322次组卷
|
5卷引用:江西省南昌市豫章中学20212-2022学年高一下学期第一次月考化学试题
江西省南昌市豫章中学20212-2022学年高一下学期第一次月考化学试题北京市东城区北京景山学校2019~2020学年高一下学期期末考试化学试题贵州省铜仁市伟才学校2019-2020学年高一下学期期末考试化学(理)试题黑龙江省大庆市肇州县第二中学2019-2020学年高一下学期期末考试化学试题(已下线)1.3.4 氧化还原反应方程式的配平-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)
名校
解题方法
7 . 实验室以锈蚀程度很大的废铁屑为原料制备 晶体的流程如下:
晶体的流程如下: 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀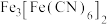 。回答下列问题:
。回答下列问题:
(1)“酸溶”过程中发生的主要反应有:① ;
;
②___________ (用离子方程式表示)
③___________ (用离子方程式表示)
(2)“酸溶”需控制温度在 左右,最佳的加热方式为
左右,最佳的加热方式为___________ 。
(3)“过滤”需要的玻璃仪器除烧杯外还有___________ 。
(4)“氧化”过程可在下图所示装置中进行。___________ 。
②装置 中发生的反应离子方程式为
中发生的反应离子方程式为___________ 。
③B中使用多孔球泡的作用是___________ 。
④证明装置 溶液中
溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是___________ 。
 晶体的流程如下:
晶体的流程如下:
 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀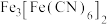 。回答下列问题:
。回答下列问题:(1)“酸溶”过程中发生的主要反应有:①
 ;
;②
③
(2)“酸溶”需控制温度在
 左右,最佳的加热方式为
左右,最佳的加热方式为(3)“过滤”需要的玻璃仪器除烧杯外还有
(4)“氧化”过程可在下图所示装置中进行。
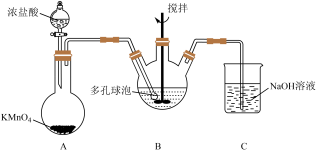
②装置
 中发生的反应离子方程式为
中发生的反应离子方程式为③B中使用多孔球泡的作用是
④证明装置
 溶液中
溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是
您最近一年使用:0次
名校
解题方法
8 . 下列实验操作能达到相应实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 用pH试纸测新制氯水的pH | 用干燥洁净的玻璃棒蘸取溶液,滴在pH试纸上,与标准比色卡对照 |
| B | 制备Fe(OH)3胶体 | 向饱和FeCl3溶液中滴加氨水并不断搅拌 |
| C | 证明还原性:I->Fe2+ | 向FeI2和KSCN混合溶液中滴入少量氯水,再加入CCl4,振荡 |
| D | 除去甲烷中的乙烯 | 将混合气体缓慢通过酸性高锰酸钾溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)明胶的水溶液和淀粉溶液共同具备的性质是________ (填字母)。
(2)现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
甲同学:向1mol/L的FeCl3溶液中加少量NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向25mL沸水中逐滴加入5~6滴FeCl3饱和浓液,继续煮沸至溶液呈红褐色,停止加热。
试回答下列问题:
①其中操作正确的同学是________ ,化学反应方程式:_________ 。
②证明有Fe(OH) 3胶体生成的实验操作是_________ ;FeCl3饱和溶液和Fe(OH)3胶体根本区别是________ 。
③在胶体中加入电解质溶液或带有相反电荷的胶体粒子能使胶体粒子沉淀出来。丁同学利用所制得的Fe(OH)3胶体进行实验:
a.将其装入U形管内,用石墨作电极,通电一段时间后发现阴极区附近的颜色逐渐变深,这表明________ 。
b.向其中加入饱和K2SO4溶液,产生的现象是________ 。
(1)明胶的水溶液和淀粉溶液共同具备的性质是
| A.都不稳定,密封放置沉淀 | B.都能产生丁达尔效应 |
| C.分散质粒子可通过滤纸 | D.分散质粒子可通过半透膜 |
甲同学:向1mol/L的FeCl3溶液中加少量NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向25mL沸水中逐滴加入5~6滴FeCl3饱和浓液,继续煮沸至溶液呈红褐色,停止加热。
试回答下列问题:
①其中操作正确的同学是
②证明有Fe(OH) 3胶体生成的实验操作是
③在胶体中加入电解质溶液或带有相反电荷的胶体粒子能使胶体粒子沉淀出来。丁同学利用所制得的Fe(OH)3胶体进行实验:
a.将其装入U形管内,用石墨作电极,通电一段时间后发现阴极区附近的颜色逐渐变深,这表明
b.向其中加入饱和K2SO4溶液,产生的现象是
您最近一年使用:0次
10 . 铁是人体必需的微量元素,严重缺铁时需要服用补铁剂。实验小组为研究某补铁剂中铁元素的价态,设计并进行了如下实验:
【资料】Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为-2价,通常被氧化为+6价

将补铁剂碾碎的目的是增大接触面积,使其充分溶解。
(1)试剂1是_______ (填名称),试剂2是_______ (填名称)。
(2)加入试剂2后溶液变为浅红色,说明溶液①中含有_______ (填离子符号)。
(3)能证明溶液①中含有Fe2+的实验现象是_______ 。
(4)写出在上述条件下Fe2+与NaClO发生反应的离子方程式:_______ 。
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的 与NaClO发生了化学反应。
与NaClO发生了化学反应。
a.甲同学猜测的依据是_______ 。
b.乙同学通过实验证实了甲同学的猜测,其实验方案及现象是_______ 。
【资料】Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为-2价,通常被氧化为+6价

将补铁剂碾碎的目的是增大接触面积,使其充分溶解。
(1)试剂1是
(2)加入试剂2后溶液变为浅红色,说明溶液①中含有
(3)能证明溶液①中含有Fe2+的实验现象是
(4)写出在上述条件下Fe2+与NaClO发生反应的离子方程式:
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的
 与NaClO发生了化学反应。
与NaClO发生了化学反应。a.甲同学猜测的依据是
b.乙同学通过实验证实了甲同学的猜测,其实验方案及现象是
您最近一年使用:0次



