名校
解题方法
1 . 下列说法正确的有
①在周期表中,同周期第ⅡA族和第ⅢA族元素质子数相差可能是1、11或25
②同主族元素从上至下,单质的氧化性逐渐减弱,熔点逐渐降低
③碱性:LiOH>NaOH>KOH>RbOH
④酸性:H2SO4>HClO4>HBrO4>HIO4
⑤卤族元素由上至下,阴离子的还原性增强,单质的颜色加深
⑥碱金属单质物理通性是硬度小,密度小,熔点低
⑦碱金属元素的原子半径和离子半径都随核电荷数的增大而增大
⑧可以利用非金属单质与H2反应的难易程度来证明其元素非金属性的强弱
①在周期表中,同周期第ⅡA族和第ⅢA族元素质子数相差可能是1、11或25
②同主族元素从上至下,单质的氧化性逐渐减弱,熔点逐渐降低
③碱性:LiOH>NaOH>KOH>RbOH
④酸性:H2SO4>HClO4>HBrO4>HIO4
⑤卤族元素由上至下,阴离子的还原性增强,单质的颜色加深
⑥碱金属单质物理通性是硬度小,密度小,熔点低
⑦碱金属元素的原子半径和离子半径都随核电荷数的增大而增大
⑧可以利用非金属单质与H2反应的难易程度来证明其元素非金属性的强弱
| A.4个 | B.5个 | C.6个 | D.7个 |
您最近一年使用:0次
2021-12-03更新
|
348次组卷
|
2卷引用:江西省丰城中学2022-2023学年高一上学期期中考试化学试题(创新班)
名校
解题方法
2 . 央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是__________ 价。 是一种酸根离子,则
是一种酸根离子,则 属于
属于__________ (填“酸”、“碱”、“盐”或“氧化物”)。
(2)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的__________ (填序号)。
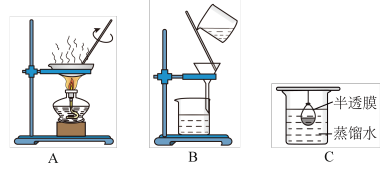
(3)现有10mL明胶的水溶液与5mLK2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜:
能够透过半透膜:_____________________ ;该检验过程中发生的离子方程式为____________________ 。
(1)已知
 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是 是一种酸根离子,则
是一种酸根离子,则 属于
属于(2)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的

(3)现有10mL明胶的水溶液与5mLK2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
 能够透过半透膜:
能够透过半透膜:
您最近一年使用:0次
3 . 铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)所含铁元素既有氧化性又有还原性的物质是____ (填字母代号)。
(2)向沸水中逐滴滴加lmol/LFeCl3溶液,至____ ,该分散系中粒子直径的范围是____ nm。
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:____ 。某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:首先取少量待测溶液﹐滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是____ ,在此基础上,又进行了定量组成的测定:取50.0mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,____ (填实验操作,下同)、洗涤、干燥,称量沉淀质量为43.05g。则待测溶液中,FeCl3的物质的量浓度为____ 。
(4)若要验证该溶液中含有Fe2+,正确的实验方法是____ (填字母代号)。
A.向试管中加入试液,滴入KSCN溶液,若显红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
(5)欲从废水中回收铜,并重新获得FeCl3溶液,设计实验方案如图:

A.请写出上述实验中加入或生成的有关物质的化学式:①____ ;②____ ;③____ ;④____ 。
B.请写出通入⑥的化学方程式:_____ 。
(1)所含铁元素既有氧化性又有还原性的物质是
| A.Fe | B.FeCl2 | C.FeSO4 | D.Fe2O3 |
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
(4)若要验证该溶液中含有Fe2+,正确的实验方法是
A.向试管中加入试液,滴入KSCN溶液,若显红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
(5)欲从废水中回收铜,并重新获得FeCl3溶液,设计实验方案如图:

A.请写出上述实验中加入或生成的有关物质的化学式:①
B.请写出通入⑥的化学方程式:
您最近一年使用:0次
名校
4 . 下表是元素周期表的一部分,针对表中的①~⑩号元素,用元素符号或化学式回答以下问题:
(1)⑦⑧⑨⑩号元素原子分别形成简单离子的离子半径由大到小的顺序_______ (填离子符号)
(2)①和⑤号元素形成的原子可构成10电子分子,该分子电子式为_______ .
(3)⑤⑦元素原子可形成 和
和 类型化合物,写出其
类型化合物,写出其 型化合物与水反应的化学方程式
型化合物与水反应的化学方程式_______
(4)由⑧、⑩构成的化合物属于_______ (填电解质或非电解质)熔融状态下该化合物是否导电_______ (填是或否)
(5)元素⑦与元素⑧相比,金属性较强的是_______ (填元素符号),下列表述中能证明这一事实的是_______ (填字母).
a.⑦单质的熔点比⑧单质低 b.⑦单质与水反应比⑧单质剧烈
c.⑦最高价氧化物对应的水化物的碱性比⑧强 d.⑦的化合价比⑧低
(6)元素④的一种原子的质子数比中子数少1,则mg此元素构成的单质标准状况下的体积为_______ (结果保留两位小数)
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ⑥ | |||
| 三 | ⑦ | ⑧ | ⑨ | ⑩ |
(2)①和⑤号元素形成的原子可构成10电子分子,该分子电子式为
(3)⑤⑦元素原子可形成
 和
和 类型化合物,写出其
类型化合物,写出其 型化合物与水反应的化学方程式
型化合物与水反应的化学方程式(4)由⑧、⑩构成的化合物属于
(5)元素⑦与元素⑧相比,金属性较强的是
a.⑦单质的熔点比⑧单质低 b.⑦单质与水反应比⑧单质剧烈
c.⑦最高价氧化物对应的水化物的碱性比⑧强 d.⑦的化合价比⑧低
(6)元素④的一种原子的质子数比中子数少1,则mg此元素构成的单质标准状况下的体积为
您最近一年使用:0次
名校
解题方法
5 . 现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X_______
(2)上述实验流程中①②③步均要进行的实验操作是_______ (填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液后发生反应的离子方程式:_______ 、_______ 。
(4)(本小题两空均填化学式)按此实验方案得到的溶液3中肯定含有_______ 杂质。为了解决这个问题,可以向溶液3中加入适量的_______ 。
(5)在①步操作中如何证明加的BaCl2溶液已过量?_______ 。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X
(2)上述实验流程中①②③步均要进行的实验操作是
(3)上述实验流程中加入过量Na2CO3溶液后发生反应的离子方程式:
(4)(本小题两空均填化学式)按此实验方案得到的溶液3中肯定含有
(5)在①步操作中如何证明加的BaCl2溶液已过量?
您最近一年使用:0次
2021-06-21更新
|
421次组卷
|
4卷引用:江西省宜春市上高二中2022-2023学年高一上学期第一次月考化学试题
名校
解题方法
6 . 下列关于胶体的说法中正确的是
| A.溶液和胶体的本质区别是当一束光线通过胶体时可出现一条光亮的通路,溶液则没有此现象 |
B.制备 胶体的方法是将饱和氯化铁溶液加热煮沸 胶体的方法是将饱和氯化铁溶液加热煮沸 |
| C.静电除尘,利用了胶体电泳 |
| D.胶体不均一、不稳定,静置易产生沉淀:溶液均一、稳定,静置不产生沉淀 |
您最近一年使用:0次
名校
解题方法
7 . 溶液X中可能存在 、
、 、
、 、
、 、
、 、
、 中的若干种。为探究该溶液组成进行如下实验:
中的若干种。为探究该溶液组成进行如下实验:

下列关于溶液X的说法正确的是
 、
、 、
、 、
、 、
、 、
、 中的若干种。为探究该溶液组成进行如下实验:
中的若干种。为探究该溶液组成进行如下实验:
下列关于溶液X的说法正确的是
A.可能存在 | B.一定存在 、 、 、 、 |
C.  和 和 至少有一种 至少有一种 | D.一定不存在 、 、 |
您最近一年使用:0次
2023-01-13更新
|
178次组卷
|
11卷引用:江西省丰城市第九中学(日新班)2021-2022学年高一下学期期末检测化学试题
江西省丰城市第九中学(日新班)2021-2022学年高一下学期期末检测化学试题云南省昆明市第一中学2021-2022学年高一上学期期末考试化学试题湖北省问津联合体2021-2022学年高一下学期5月质量检测化学试题安徽省安庆市第一中学龙山校区2021-2022学年高一下学期3月阶段性考试化学试题浙江省宁波市2020-2021学年高一上学期期末考试化学试题吉林省辽源市第五中学2020-2021学年高一下学期第一次月考化学试题(已下线)【浙江新东方】在线化学54高一上内蒙古呼和浩特市第二中学致远级部2022-2023学年高一上学期期末考试化学试题 四川省宜宾市第四中学校2022-2023学年高一下学期开学考试化学试题安徽省安庆市怀宁县高河中学2023-2024学年高一上学期第二次月考化学试题牡丹江市第一高级中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
8 . 实现“碳达峰碳中和”战略目标既是我国建设现代化强国、实现中华民族永续发展的内在要求。 中科院成都研究所研究员李东提出了一种新的负排放技术——POWER TO GAS(可再生电转生物天然气)。这项技术,指的是先捕获工厂和沼气池产生的二氧化碳,利用可再生电水解制氢,再将氢气用于还原沼气中的二氧化碳,使二氧化碳变为甲烷,替代天然气使用。下列说法不正确的是
| A.碳中和,即排放的二氧化碳和吸收利用的二氧化碳达到平衡 |
| B.1molCO2 中含有 9.632×1024 个电子 |
| C.甲烷是非电解质 |
| D.44g CO2 全部被还原可生成 1molCH4 |
您最近一年使用:0次
名校
9 . 菜之魂在味,在“七味八滋”中,盐应是百味之首。粗盐常含有少量Ca2+、Mg2+、SO 以及泥沙等杂质,实验室中提纯NaCl的流程如图所示,下列说法中错误的是
以及泥沙等杂质,实验室中提纯NaCl的流程如图所示,下列说法中错误的是

 以及泥沙等杂质,实验室中提纯NaCl的流程如图所示,下列说法中错误的是
以及泥沙等杂质,实验室中提纯NaCl的流程如图所示,下列说法中错误的是 
| A.操作Ⅰ需要使用的玻璃仪器是玻璃棒、漏斗、烧杯 |
| B.操作Ⅱ为蒸发结晶,蒸发过程中当蒸发皿中全部晶体析出时停止加热 |
| C.溶液a为BaCl2溶液,加入溶液b的主要目的是除去Ca2+和Ba2+ |
| D.粗盐提纯的整个操作过程中共有两处需要使用玻璃棒 |
您最近一年使用:0次
2022-11-21更新
|
163次组卷
|
3卷引用:江西省宜春市宜丰中学2022-2023学年高一上学期12月月考化学试题
名校
解题方法
10 . 在物质研究过程中,同一物质中同一元素呈现不同的氧化数,比如:Fe3O4化学式可以写成Fe(II)Fe(III)2O4。A是一种名为GR-II(GreenRust,绿锈,简称GR)的物质,其制取过程如下:在N2保护和搅拌下,向100mL0.40mol•L-1的浅绿色FeSO4溶液中加入40mL0.80mol•L-1的NaOH溶液,得到Fe(OH)2沉淀,保持通N2升温至40℃,将气体切换为空气。随着空气通入,悬浊体系由浅绿色变深,形成蓝绿色沉淀A。其中涉及方程式为:10Fe(OH)2+2Fe2++2SO +O2+2H2O=2Fe(II)4Fe(III)2(OH)12(SO4)。
+O2+2H2O=2Fe(II)4Fe(III)2(OH)12(SO4)。
下列说法不正确的是
 +O2+2H2O=2Fe(II)4Fe(III)2(OH)12(SO4)。
+O2+2H2O=2Fe(II)4Fe(III)2(OH)12(SO4)。下列说法不正确的是
| A.Fe(II)4Fe(III)2(OH)12(SO4)的摩尔质量为636 |
| B.O2是氧化剂 |
| C.氧化剂与还原剂的物质的量之比为1:4 |
| D.每生成1molFe(II)4Fe(III)2(OH)12(SO4)转移2mol电子 |
您最近一年使用:0次
2022-11-19更新
|
142次组卷
|
3卷引用:江西省宜春市宜丰中学2022-2023学年高一上学期12月月考化学试题



