名校
1 . 某课外活动小组设计实验验证二氧化碳跟过氧化钠反应时需要与水接触。下列说法中正确的是
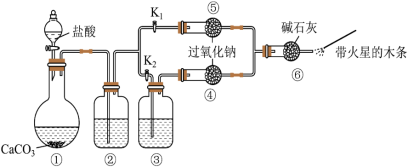

| A.装置①中盐酸不能换成硫酸 |
B.装置②中的试剂是饱和 溶液 溶液 |
C.打开弹簧夹 ,关闭 ,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条复燃 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条复燃 |
| D.上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应 |
您最近一年使用:0次
2022-12-07更新
|
193次组卷
|
2卷引用:江西省九江市同文中学2022-2023学年高一上学期期中考试化学试题
2 . 硝酸是中学常见的试剂,广泛应用于化学实验。
实验Ⅰ:探究元素性质递变规律。
某小组选择硝酸、碳酸钙和硅酸钠溶液,证明N、C、Si的非金属性依次减弱。

(1)B中试剂是_______ 。
(2)写出A中离子方程式:_______ 。
(3)C中可能的实验现象是_______ ,由此证明碳的非金属性比硅强。
(4)有同学采用替代试剂的方法,利用上述装置证明氯的非金属性比硫强,他选择的试剂是盐酸、亚硫酸钠粉末、品红溶液,他不能达到实验目的,原因是_______ 。
实验Ⅱ:探究铜与硝酸反应速率。
小组乙设计如下方案:
(5)实验测得b<a,可以得出实验结论是_______ 。
(6)设计实验②和④的目的是_______ 。上述实验方案,不能探究_______ (填字母)对铜和硝酸反应速率的影响。
A.温度 B.浓度 C.接触面 D.催化剂
实验Ⅰ:探究元素性质递变规律。
某小组选择硝酸、碳酸钙和硅酸钠溶液,证明N、C、Si的非金属性依次减弱。

(1)B中试剂是
(2)写出A中离子方程式:
(3)C中可能的实验现象是
(4)有同学采用替代试剂的方法,利用上述装置证明氯的非金属性比硫强,他选择的试剂是盐酸、亚硫酸钠粉末、品红溶液,他不能达到实验目的,原因是
实验Ⅱ:探究铜与硝酸反应速率。
小组乙设计如下方案:
| 实验 | 2g铜 | 10mL硝酸 | 温度/℃ | 铜完全溶解的时间/min |
| ① | 铜片 | 2mol/L | 20 | a |
| ② | 铜片 | 4mol/L | 20 | b |
| ③ | 铜粉 | 4mol/L | 20 | c |
| ④ | 铜片 | 4mol/L | 40 | d |
(6)设计实验②和④的目的是
A.温度 B.浓度 C.接触面 D.催化剂
您最近一年使用:0次
3 . 在反应 (未配平)中,下列有关说法正确的是
(未配平)中,下列有关说法正确的是
 (未配平)中,下列有关说法正确的是
(未配平)中,下列有关说法正确的是| A.KClO3在反应中得到电子,作还原剂 |
| B.每生成3个Cl2分子,转移5个电子 |
| C.HCl在反应中只体现了还原性 |
| D.反应中氧化剂和还原剂的个数比为1:6 |
您最近一年使用:0次
2022-12-07更新
|
177次组卷
|
4卷引用:江西省九江市同文中学2022-2023学年高一上学期期中考试化学试题
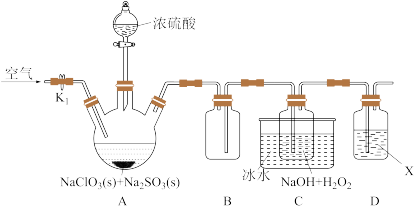
4 . 亚氯酸钠( )是一种高效的氧化剂和优质漂白剂,在水中溶解度较大,遇酸放出
)是一种高效的氧化剂和优质漂白剂,在水中溶解度较大,遇酸放出 。某探究小组设计实验制备
。某探究小组设计实验制备 固体的主要装置如图所示(夹持装置省略)。
固体的主要装置如图所示(夹持装置省略)。
已知:① 饱和溶液在低于38℃时会析出
饱和溶液在低于38℃时会析出 ,高于38℃低于60℃时析出
,高于38℃低于60℃时析出 ,高于60℃时
,高于60℃时 分解成
分解成 和NaCl。
和NaCl。
② 的沸点为11℃,纯度过高易爆炸,极易与水反应。
的沸点为11℃,纯度过高易爆炸,极易与水反应。
回答下列问题:
(1)A为 的发生装置。下列有关说法正确的是
的发生装置。下列有关说法正确的是_________ (填序号)。
a.反应结束后通入空气一段时间 b.反应过程中持续通入空气
c.可用浓硝酸代替浓硫酸 d.X试剂可以是氢氧化钠溶液
(2)装置B的作用是_________ 。
(3)写出A装置三颈烧瓶中生成 的化学方程式
的化学方程式_________ 。
(4)装置C中NaOH、 与
与 反应放出大量热量,生成
反应放出大量热量,生成 和一种助燃气体,该反应的还原剂为
和一种助燃气体,该反应的还原剂为_________ ;装置C用冰水浴冷却的主要目的是_________ 。
(5)充分反应后,为从产品溶液中获取 晶体,从下列选项中选出合理的操作并排序:
晶体,从下列选项中选出合理的操作并排序:_________ →干燥
a.趁热过滤 b.50℃水洗涤 c.加热蒸发结晶 d.冰水洗涤 e.55℃恒温减压蒸发结晶
(6)测定样品中 的纯度。准确称取所得
的纯度。准确称取所得 样品mg于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应,将所得混合液稀释成100mL待测溶液。移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用
样品mg于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应,将所得混合液稀释成100mL待测溶液。移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用 的
的 标准溶液滴定至终点,重复2次,测得消耗
标准溶液滴定至终点,重复2次,测得消耗 标准溶液的体积平均值为VmL。(已知:
标准溶液的体积平均值为VmL。(已知: ,
,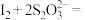
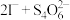 )。该样品中
)。该样品中 的质量分数为
的质量分数为_________ (用含m、c、V的代数式表示)。若在检测中加入稀硫酸的量过少,将导致测定值_________ (填“偏高”或“偏低”)。
 )是一种高效的氧化剂和优质漂白剂,在水中溶解度较大,遇酸放出
)是一种高效的氧化剂和优质漂白剂,在水中溶解度较大,遇酸放出 。某探究小组设计实验制备
。某探究小组设计实验制备 固体的主要装置如图所示(夹持装置省略)。
固体的主要装置如图所示(夹持装置省略)。
已知:①
 饱和溶液在低于38℃时会析出
饱和溶液在低于38℃时会析出 ,高于38℃低于60℃时析出
,高于38℃低于60℃时析出 ,高于60℃时
,高于60℃时 分解成
分解成 和NaCl。
和NaCl。②
 的沸点为11℃,纯度过高易爆炸,极易与水反应。
的沸点为11℃,纯度过高易爆炸,极易与水反应。回答下列问题:
(1)A为
 的发生装置。下列有关说法正确的是
的发生装置。下列有关说法正确的是a.反应结束后通入空气一段时间 b.反应过程中持续通入空气
c.可用浓硝酸代替浓硫酸 d.X试剂可以是氢氧化钠溶液
(2)装置B的作用是
(3)写出A装置三颈烧瓶中生成
 的化学方程式
的化学方程式(4)装置C中NaOH、
 与
与 反应放出大量热量,生成
反应放出大量热量,生成 和一种助燃气体,该反应的还原剂为
和一种助燃气体,该反应的还原剂为(5)充分反应后,为从产品溶液中获取
 晶体,从下列选项中选出合理的操作并排序:
晶体,从下列选项中选出合理的操作并排序:a.趁热过滤 b.50℃水洗涤 c.加热蒸发结晶 d.冰水洗涤 e.55℃恒温减压蒸发结晶
(6)测定样品中
 的纯度。准确称取所得
的纯度。准确称取所得 样品mg于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应,将所得混合液稀释成100mL待测溶液。移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用
样品mg于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应,将所得混合液稀释成100mL待测溶液。移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用 的
的 标准溶液滴定至终点,重复2次,测得消耗
标准溶液滴定至终点,重复2次,测得消耗 标准溶液的体积平均值为VmL。(已知:
标准溶液的体积平均值为VmL。(已知: ,
,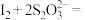
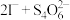 )。该样品中
)。该样品中 的质量分数为
的质量分数为
您最近一年使用:0次
5 . 科学家发现某些生物酶体系可以促进 和
和 的转移如(a、b和c),能将海洋中的
的转移如(a、b和c),能将海洋中的 转化为
转化为 进入大气层,反应过程如图所示。下列说法不正确的是
进入大气层,反应过程如图所示。下列说法不正确的是
 和
和 的转移如(a、b和c),能将海洋中的
的转移如(a、b和c),能将海洋中的 转化为
转化为 进入大气层,反应过程如图所示。下列说法不正确的是
进入大气层,反应过程如图所示。下列说法不正确的是
| A.过程I中NO是还原产物 |
B.a和b中转移的 数目相等 数目相等 |
C.过程Ⅱ中参与反应的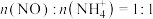 |
D.过程Ⅰ→Ⅲ的总反应为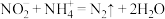 |
您最近一年使用:0次
2022-11-23更新
|
97次组卷
|
2卷引用:江西省九江市十校2022-2023学年高三上学期11月联考化学试题
名校
解题方法
6 . 下列说法正确的一组是
① 、MgO、
、MgO、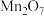 均属于碱性氧化物
均属于碱性氧化物
②已知氧化铝在熔融状态下能导电,则氧化铝在熔融状态下能电离
③海水、空气、胆矾、盐酸均为混合物
④苏打、碱石灰、醋酸、小苏打均为电解质
⑤电解质溶液导电的原因是溶液中有自由移动的阴、阳离子
⑥熔融的电解质都能导电
①
 、MgO、
、MgO、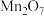 均属于碱性氧化物
均属于碱性氧化物②已知氧化铝在熔融状态下能导电,则氧化铝在熔融状态下能电离
③海水、空气、胆矾、盐酸均为混合物
④苏打、碱石灰、醋酸、小苏打均为电解质
⑤电解质溶液导电的原因是溶液中有自由移动的阴、阳离子
⑥熔融的电解质都能导电
| A.①⑤⑥ | B.②③⑤ | C.③④ | D.②⑤ |
您最近一年使用:0次
2022-12-07更新
|
121次组卷
|
2卷引用:江西省九江市同文中学2022-2023学年高一上学期期中考试化学试题
7 . 根据元素周期表和元素周期律,下列说法错误的是
| A.第118号元素在周期表中位于第七周期0族 |
| B.氢元素与其他元素可形成共价化合物或离子化合物 |
| C.碱金属元素从上到下随电子层数的增多金属性依次增强 |
| D.气态氢化物的稳定性:H2O>PH3>H2S |
您最近一年使用:0次
解题方法
8 . 胶体在自然界尤其是生物界普遍存在,应用也非常广泛。下列有关胶体的说法错误的是
| A.可用渗析法提纯、精制胶体 |
| B.丁达尔效应可被用来区分胶体和溶液 |
C.氢氧化铁胶粒带正电荷,1mol胶粒中含有1mol |
| D.气溶胶是胶体的一种,是混合物 |
您最近一年使用:0次
名校
解题方法
9 . 在一定温度下,将少量CaO固体置于Ca(OH)2悬浊液中,一段时间后恢复至原来温度。下列说法中正确的是
| A.溶液中的Ca2+总数不变 | B.溶液中c(OH—)保持不变 |
| C.溶质的质量分数增大 | D.溶液的质量不变 |
您最近一年使用:0次
2022-02-28更新
|
108次组卷
|
2卷引用:江西省九江第一中学2021-2022学年高二下学期5月月考化学试题
名校
解题方法
10 . 某兴趣小组同学向一定体积的 溶液中逐滴滴加稀
溶液中逐滴滴加稀 ,不断搅拌并测定溶液导电能力的变化(装置如图所示)。
,不断搅拌并测定溶液导电能力的变化(装置如图所示)。

I.实验测得混合溶液的导电能力随时间变化的曲线如图所示。

(1)写出 溶液与稀硫酸反应的离子方程式
溶液与稀硫酸反应的离子方程式_______ 。
(2)该小组的同学关于如图的说法中正确的是_______ (填“序号”)。
①AB段溶液的导电能力不断减弱,说明生成的 不是电解质
不是电解质
②B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子
③BC段溶液的导电能力不断增大,主要是由于过量的 ,电离出的离子导电
,电离出的离子导电
④a时刻 溶液与稀H2SO4恰好中和
溶液与稀H2SO4恰好中和
Ⅱ.配制250mL 1.0mol/L 溶液。
溶液。
(3)计算:需要用量筒量取18mol/L 溶液
溶液_______ mL。
(4)下列操作将导致所配制的 溶液浓度偏大有
溶液浓度偏大有_______ 。
a.移液过程有 溶液溅出瓶外
溶液溅出瓶外
b.将量取浓硫酸的量筒洗涤干净,洗涤液也转移到容量瓶中
c.定容时俯视容量瓶刻度线
d.加水超过刻度线,用胶头滴管吸出多余液体
(5)现有浓度为18mol/L的浓硫酸溶液200g,需要加入一定量的水将其稀释为9mol/L,则加入水的体积是_______ 。
A.大于200mL B.小于200mL C.等于200mL
 溶液中逐滴滴加稀
溶液中逐滴滴加稀 ,不断搅拌并测定溶液导电能力的变化(装置如图所示)。
,不断搅拌并测定溶液导电能力的变化(装置如图所示)。
I.实验测得混合溶液的导电能力随时间变化的曲线如图所示。

(1)写出
 溶液与稀硫酸反应的离子方程式
溶液与稀硫酸反应的离子方程式(2)该小组的同学关于如图的说法中正确的是
①AB段溶液的导电能力不断减弱,说明生成的
 不是电解质
不是电解质②B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子
③BC段溶液的导电能力不断增大,主要是由于过量的
 ,电离出的离子导电
,电离出的离子导电④a时刻
 溶液与稀H2SO4恰好中和
溶液与稀H2SO4恰好中和Ⅱ.配制250mL 1.0mol/L
 溶液。
溶液。(3)计算:需要用量筒量取18mol/L
 溶液
溶液(4)下列操作将导致所配制的
 溶液浓度偏大有
溶液浓度偏大有a.移液过程有
 溶液溅出瓶外
溶液溅出瓶外b.将量取浓硫酸的量筒洗涤干净,洗涤液也转移到容量瓶中
c.定容时俯视容量瓶刻度线
d.加水超过刻度线,用胶头滴管吸出多余液体
(5)现有浓度为18mol/L的浓硫酸溶液200g,需要加入一定量的水将其稀释为9mol/L,则加入水的体积是
A.大于200mL B.小于200mL C.等于200mL
您最近一年使用:0次



