名校
解题方法
1 . 被世卫组织列为Al级新型高效安全消毒剂的二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,易溶于水,沸点为11℃,遇热不稳定易分解发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁( )]还原氯酸钠(
)]还原氯酸钠( )制取二氧化氯。某研究小组利用如图装置制备
)制取二氧化氯。某研究小组利用如图装置制备 ,向三颈烧瓶中加入
,向三颈烧瓶中加入 溶液、浓
溶液、浓 通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。请回答下列问题:
通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。请回答下列问题:

(1) 中S元素的化合价为
中S元素的化合价为_______ 价;仪器a的名称是_______ 。
(2)三颈烧瓶中发生反应的离子方程式为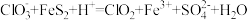 (未配平)。
(未配平)。
①该反应中被氧化的元素为_______ (填元素符号),还原产物为_______ (填化学式)。
②配平该离子方程式:_______ 。
(3)设计实验证明ClO2的氧化性比 的强:
的强:_______ 。
(4)将少量ClO2水溶液滴入盛有MnSO4溶液的试管中,振荡,有黑色沉淀生成,已知反应中氧化剂与还原剂的物质的量之比为2:5,则该反应的离子方程式为_______ 。
 )]还原氯酸钠(
)]还原氯酸钠( )制取二氧化氯。某研究小组利用如图装置制备
)制取二氧化氯。某研究小组利用如图装置制备 ,向三颈烧瓶中加入
,向三颈烧瓶中加入 溶液、浓
溶液、浓 通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。请回答下列问题:
通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。请回答下列问题:
(1)
 中S元素的化合价为
中S元素的化合价为(2)三颈烧瓶中发生反应的离子方程式为
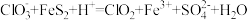 (未配平)。
(未配平)。①该反应中被氧化的元素为
②配平该离子方程式:
(3)设计实验证明ClO2的氧化性比
 的强:
的强:(4)将少量ClO2水溶液滴入盛有MnSO4溶液的试管中,振荡,有黑色沉淀生成,已知反应中氧化剂与还原剂的物质的量之比为2:5,则该反应的离子方程式为
您最近一年使用:0次
名校
2 . 某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题。
探究一:设计如图所示装置进行“铁与水反应”的实验
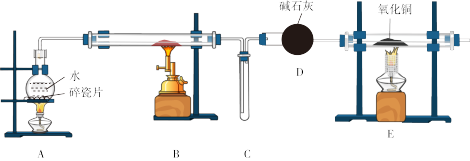
(1)硬质玻璃管中反应的化学方程式为_______
(2)装置 中的现象是
中的现象是_______ 。
探究二:设计如下实验方案确定反应后硬质玻璃管 中黑色固体的成分。
中黑色固体的成分。
实验操作:待硬质玻璃管 冷却后,取少许其中的固体物质溶于稀硫酸后,将所得溶液分成两份。滴加几滴
冷却后,取少许其中的固体物质溶于稀硫酸后,将所得溶液分成两份。滴加几滴 溶液。
溶液。
(3)a.若溶液变血红色,推断硬质玻璃管 中固体物质的成分为
中固体物质的成分为_______  选填序号,下同
选填序号,下同 ,写出溶液变血红色的离子方程式:
,写出溶液变血红色的离子方程式:_______ ;
b.若溶液未变血红色,推断硬质玻璃管 中固体物质的成分为
中固体物质的成分为_______ ,其发生的离子方程式为_______ 。
①一定有 ②一定有
②一定有 ③只有
③只有 ④只有
④只有
(4)如何设计实验证明溶液中存在 ?
?_______
(5)已知氧化性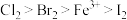 ,则向
,则向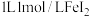 溶液中通入
溶液中通入 的
的 发生反应的总离子方程式为
发生反应的总离子方程式为_______ 。
探究一:设计如图所示装置进行“铁与水反应”的实验

(1)硬质玻璃管中反应的化学方程式为
(2)装置
 中的现象是
中的现象是探究二:设计如下实验方案确定反应后硬质玻璃管
 中黑色固体的成分。
中黑色固体的成分。实验操作:待硬质玻璃管
 冷却后,取少许其中的固体物质溶于稀硫酸后,将所得溶液分成两份。滴加几滴
冷却后,取少许其中的固体物质溶于稀硫酸后,将所得溶液分成两份。滴加几滴 溶液。
溶液。(3)a.若溶液变血红色,推断硬质玻璃管
 中固体物质的成分为
中固体物质的成分为 选填序号,下同
选填序号,下同 ,写出溶液变血红色的离子方程式:
,写出溶液变血红色的离子方程式:b.若溶液未变血红色,推断硬质玻璃管
 中固体物质的成分为
中固体物质的成分为①一定有
 ②一定有
②一定有 ③只有
③只有 ④只有
④只有
(4)如何设计实验证明溶液中存在
 ?
?(5)已知氧化性
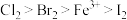 ,则向
,则向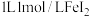 溶液中通入
溶液中通入 的
的 发生反应的总离子方程式为
发生反应的总离子方程式为
您最近一年使用:0次
3 . 下列关于物质或离子检验的叙述正确的是
A.向某溶液中加入稀盐酸酸化的 溶液,有白色沉淀,证明原溶液中有 溶液,有白色沉淀,证明原溶液中有 |
B.某溶液中加入 溶液,产生白色沉淀,证明原溶液中含 溶液,产生白色沉淀,证明原溶液中含 |
C.灼烧白色粉末,火焰呈黄色,证明原粉末中有 ,无 ,无 |
D.向某固体样品中加入浓NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,则证明样品中含有 |
您最近一年使用:0次
2022-03-14更新
|
369次组卷
|
3卷引用:江西省南昌市第十九中学2021-2022学年高一下学期第一次月考化学试卷
名校
4 . 下表是元素周期表的一部分,针对表中的①~⑩号元素,用元素符号或化学式回答以下问题:
(1)⑦⑧⑨⑩号元素原子分别形成简单离子的离子半径由大到小的顺序_______ (填离子符号)
(2)①和⑤号元素形成的原子可构成10电子分子,该分子电子式为_______ .
(3)⑤⑦元素原子可形成 和
和 类型化合物,写出其
类型化合物,写出其 型化合物与水反应的化学方程式
型化合物与水反应的化学方程式_______
(4)由⑧、⑩构成的化合物属于_______ (填电解质或非电解质)熔融状态下该化合物是否导电_______ (填是或否)
(5)元素⑦与元素⑧相比,金属性较强的是_______ (填元素符号),下列表述中能证明这一事实的是_______ (填字母).
a.⑦单质的熔点比⑧单质低 b.⑦单质与水反应比⑧单质剧烈
c.⑦最高价氧化物对应的水化物的碱性比⑧强 d.⑦的化合价比⑧低
(6)元素④的一种原子的质子数比中子数少1,则mg此元素构成的单质标准状况下的体积为_______ (结果保留两位小数)
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ⑥ | |||
| 三 | ⑦ | ⑧ | ⑨ | ⑩ |
(2)①和⑤号元素形成的原子可构成10电子分子,该分子电子式为
(3)⑤⑦元素原子可形成
 和
和 类型化合物,写出其
类型化合物,写出其 型化合物与水反应的化学方程式
型化合物与水反应的化学方程式(4)由⑧、⑩构成的化合物属于
(5)元素⑦与元素⑧相比,金属性较强的是
a.⑦单质的熔点比⑧单质低 b.⑦单质与水反应比⑧单质剧烈
c.⑦最高价氧化物对应的水化物的碱性比⑧强 d.⑦的化合价比⑧低
(6)元素④的一种原子的质子数比中子数少1,则mg此元素构成的单质标准状况下的体积为
您最近一年使用:0次
名校
解题方法
5 . 为证明卤族元素的非金属性强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检查)。

I.实验过程:
①打开弹簧夹,打开活塞 a,滴加浓盐酸。
②当 B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当 B 中溶液由黄色变为棕红色时,关闭活塞 a。
④……
(1)B中溶液发生反应的离子方程式为___________ 。
(2)为验证溴的氧化性强于碘,过程④的操作和现象是___________ 。
(3)过程③的实验目的是__ 。
(4)请从原子结构的角度解释氯、溴、碘单质的氧化性逐渐减弱的原因:__
Ⅱ.实验过程中需用到 20mL1mol/L NaBr溶液。
(5)配制 20mL1mol/L NaBr溶液需用托盘天平称取NaBr固体的质量为__ g;
(6)在配制过程中,下列实验操作对所配制溶液的物质的量浓度偏高的有___________。

I.实验过程:
①打开弹簧夹,打开活塞 a,滴加浓盐酸。
②当 B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当 B 中溶液由黄色变为棕红色时,关闭活塞 a。
④……
(1)B中溶液发生反应的离子方程式为
(2)为验证溴的氧化性强于碘,过程④的操作和现象是
(3)过程③的实验目的是
(4)请从原子结构的角度解释氯、溴、碘单质的氧化性逐渐减弱的原因:
Ⅱ.实验过程中需用到 20mL1mol/L NaBr溶液。
(5)配制 20mL1mol/L NaBr溶液需用托盘天平称取NaBr固体的质量为
(6)在配制过程中,下列实验操作对所配制溶液的物质的量浓度偏高的有___________。
| A.称量时将NaBr固体放在右盘; |
| B.用烧杯溶解NaBr 固体后,洗涤烧杯2~3次,洗涤液未转移到容量瓶; |
| C.溶液注入容量瓶前没有恢复到室温就进行定容; |
| D.定容时俯视观察凹液面。 |
您最近一年使用:0次
6 . 铁的化合物在生活中有非常重要的作用。
(1)写出上 溶液腐蚀覆铜板来制作印刷电路板的化学方程式:
溶液腐蚀覆铜板来制作印刷电路板的化学方程式:___________
(2)向沸水中逐滴加入5-6滴,继续煮沸至液体呈红褐色,停止加热制得 胶体,可利用
胶体,可利用___________ 来区分 胶体和
胶体和 饱和溶液。
饱和溶液。
(3)我国正在推行垃圾分类,为研究旧物的再利用,实验室用严重锈蚀的废铁屑为原料制备硫酸亚铁晶体(FeSO4∙7H2O),流程如下;

①试剂X是将铁及其铁表面的氧化物溶解,则实际X最好是___________
A.稀盐酸 B.稀硫酸 C.稀硝酸
②要想证明酸溶后的溶液中存在Fe3+,应取少量酸溶后溶液于试管中滴加_______ ,产生的现象为:________ 。
③写出还原反应的离子方程式_________ 。
④也可以用废铁屑制备氯化铁,则在选择合适的酸进行酸溶后应加________ (填字母)。
A.氧化剂 B.还原剂
(1)写出上
 溶液腐蚀覆铜板来制作印刷电路板的化学方程式:
溶液腐蚀覆铜板来制作印刷电路板的化学方程式:(2)向沸水中逐滴加入5-6滴,继续煮沸至液体呈红褐色,停止加热制得
 胶体,可利用
胶体,可利用 胶体和
胶体和 饱和溶液。
饱和溶液。(3)我国正在推行垃圾分类,为研究旧物的再利用,实验室用严重锈蚀的废铁屑为原料制备硫酸亚铁晶体(FeSO4∙7H2O),流程如下;

①试剂X是将铁及其铁表面的氧化物溶解,则实际X最好是
A.稀盐酸 B.稀硫酸 C.稀硝酸
②要想证明酸溶后的溶液中存在Fe3+,应取少量酸溶后溶液于试管中滴加
③写出还原反应的离子方程式
④也可以用废铁屑制备氯化铁,则在选择合适的酸进行酸溶后应加
A.氧化剂 B.还原剂
您最近一年使用:0次
7 . 下列装置完成相关实验,其中不合理的是
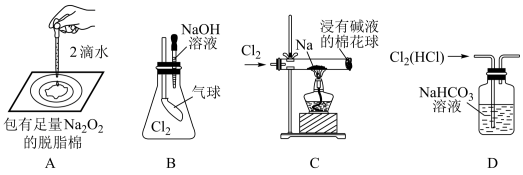

| A.图A是证明Na2O2与水反应放热 | B.图B是证明Cl2能与烧碱溶液反应 |
| C.图C是探究钠与Cl2反应 | D.图D除去Cl2中的少量HCl |
您最近一年使用:0次
2021-11-16更新
|
626次组卷
|
8卷引用:江西省赣州市2021-2022学高三上学期期末考试化学试题
名校
8 . 下列图示实验(部分夹持装置省略)正确的是
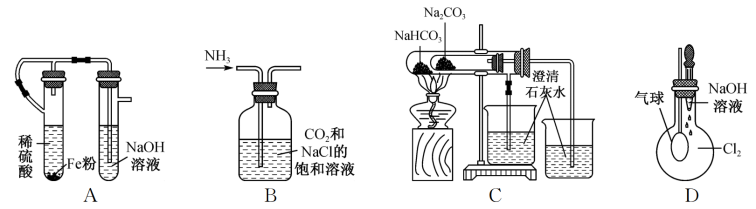

| A.图A可用于制备氢氧化亚铁 |
| B.图B可用于制备NaHCO3 |
| C.图C可用于验证碳酸钠和碳酸氢钠的稳定性 |
| D.图D可用于证明Cl2能否溶于水或与NaOH溶液反应 |
您最近一年使用:0次
2021-10-20更新
|
1121次组卷
|
12卷引用:江西省丰城中学2022-2023学年高三上学期月考化学试题
江西省丰城中学2022-2023学年高三上学期月考化学试题(已下线)基础卷01-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)(已下线)一轮巩固卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)湖北省蕲春县第一高级中学2022届高三5月第三次模拟考试化学试题辽宁省朝阳市建平县实验中学2022-2023学年高三上学期月考化学试题辽宁省大连市普兰店区第一中学2022届高三上学期期中联考化学试题安徽省六安一中,阜阳一中,合肥八中等校2022届高三上学期联考化学试题宁夏石嘴山市第三中学2021-2022学年高三上学期期中考试化学(理)试题辽宁省大连市第一中学 2021-2022学年高三上学期期中联考化学试题福建省南平市高级中学2021-2022学年高三上学期第三次月考化学试题河北省辛集市第一中学2021-2022学年高一上学期第四次月考化学试题安徽省亳州市第五完全中学2021-2022学年高三上学期期中考试化学试题
名校
解题方法
9 . 现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X_______
(2)上述实验流程中①②③步均要进行的实验操作是_______ (填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液后发生反应的离子方程式:_______ 、_______ 。
(4)(本小题两空均填化学式)按此实验方案得到的溶液3中肯定含有_______ 杂质。为了解决这个问题,可以向溶液3中加入适量的_______ 。
(5)在①步操作中如何证明加的BaCl2溶液已过量?_______ 。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X
(2)上述实验流程中①②③步均要进行的实验操作是
(3)上述实验流程中加入过量Na2CO3溶液后发生反应的离子方程式:
(4)(本小题两空均填化学式)按此实验方案得到的溶液3中肯定含有
(5)在①步操作中如何证明加的BaCl2溶液已过量?
您最近一年使用:0次
2021-06-21更新
|
421次组卷
|
4卷引用:江西省宜春市上高二中2022-2023学年高一上学期第一次月考化学试题
名校
10 . 下列实验过程可以达到实验目的的是
| 选项 | 实验操作和现象 | 实验目的 |
| A | 盐酸滴入硅酸钠溶液中出现白色沉淀 | 证明非金属性: |
| B | 向碳酸钙固体中加入盐酸,将生成的气体依次通过饱和碳酸钠溶液、浓硫酸 | 制取并纯化 |
| C | 向盛有2mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液(无色),观察颜色变化 | 探究维生素C的还原性 |
| D | 向 支盛有 支盛有 溶液的试管中分别加入 溶液的试管中分别加入 溶液和 溶液和 溶液,观察到加入 溶液,观察到加入 溶液的 溶液的 分解速率更快 分解速率更快 | 证明 对 对 分解的催化效果比 分解的催化效果比 的效果好 的效果好 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-05-07更新
|
419次组卷
|
6卷引用:江西省萍乡市萍乡实验学校2021-2022学年高一下学期第二次调研考试化学试题



