名校
解题方法
1 . 由硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、Al2O3和SiO2)得到绿矾(FeSO4•7H2O),然后制取透明氧化铁颜料的流程如图:
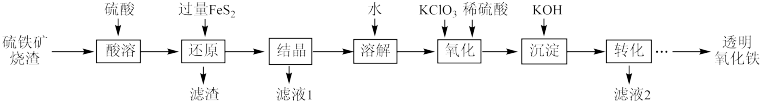
已知:
I.透明氧化铁又称纳米氧化铁,粒子直径很微小(10~90nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
II.Fe3+能将FeS2中的硫元素氧化为+6价。
(1)FeS2的电子式是_____ 。
(2)“滤渣”中的主要成分是_____ (填名称)。
(3)流程中“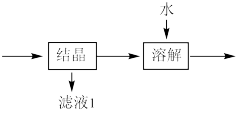 ”环节的目的是
”环节的目的是_____ 。
(4)“还原”过程中涉及的离子方程式为_____ 。
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到均匀、色泽纯正的氢氧化铁,而且还可以_____ 。
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示。
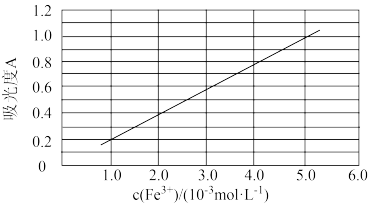
称取3.47g透明氧化铁,用稀硫酸溶解并定容至1L,准确移取该溶液10.00mL,加入足量KSCN溶液,再用蒸馏水定容至100mL,测得溶液吸光度A=0.8,则透明氧化铁中氧化铁黄的质量分数为_____ 。

已知:
I.透明氧化铁又称纳米氧化铁,粒子直径很微小(10~90nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
II.Fe3+能将FeS2中的硫元素氧化为+6价。
(1)FeS2的电子式是
(2)“滤渣”中的主要成分是
(3)流程中“
 ”环节的目的是
”环节的目的是(4)“还原”过程中涉及的离子方程式为
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到均匀、色泽纯正的氢氧化铁,而且还可以
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示。

称取3.47g透明氧化铁,用稀硫酸溶解并定容至1L,准确移取该溶液10.00mL,加入足量KSCN溶液,再用蒸馏水定容至100mL,测得溶液吸光度A=0.8,则透明氧化铁中氧化铁黄的质量分数为
您最近一年使用:0次
名校
解题方法
2 . 甘氨酸亚铁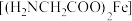 是一种新型治疗缺铁性贫血的药物,它和普通的药物相比没有铁腥味,不刺激肠胃。是一款无味、易溶于水而且不易变质的有机铁。其制备过程分为两个步骤:
是一种新型治疗缺铁性贫血的药物,它和普通的药物相比没有铁腥味,不刺激肠胃。是一款无味、易溶于水而且不易变质的有机铁。其制备过程分为两个步骤:
Ⅰ.活性 的制备:称取
的制备:称取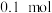 草酸亚铁晶体(
草酸亚铁晶体( )在隔绝空气的情况下加热至300℃,时间
)在隔绝空气的情况下加热至300℃,时间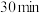 ,反应完成后冷却至室温。
,反应完成后冷却至室温。
(1)冷却时需注意的操作是_______ 。
(2)下图是将一定质量的草酸亚铁在氩气氛围中进行热重分析的示意图。B→C阶段反应的化学方程式为_______ 。[ (残留固体质量/样品起始质量)
(残留固体质量/样品起始质量) ]。
]。

Ⅱ.甘氨酸亚铁的制备:
查阅资料:
实验步骤:向如图三颈烧瓶中加入 和少量柠檬酸,再加入
和少量柠檬酸,再加入 甘氨酸,通一段时间
甘氨酸,通一段时间 ,加入石蜡油。水浴加热至70℃,恒温搅拌6小时,剩余少量黑色不溶物。将所得混合物通过_______、_______,得到无色澄清溶液。向溶液中加入无水乙醇,生成白色沉淀,将沉淀过滤、洗涤得产品,将粗产品纯化后得精品。
,加入石蜡油。水浴加热至70℃,恒温搅拌6小时,剩余少量黑色不溶物。将所得混合物通过_______、_______,得到无色澄清溶液。向溶液中加入无水乙醇,生成白色沉淀,将沉淀过滤、洗涤得产品,将粗产品纯化后得精品。

(3)石蜡油的作用_______ 。
(4)柠檬酸的作用_______ 。
(5)步骤Ⅱ的两步操作分别为_______ 、_______ (填操作名称)。
(6)最后制得10.2g甘氨酸亚铁,则其产率为_______ 。
(7)分析化学中甘氨酸的测定方法:在非水体系中用高氯酸标准溶液滴定甘氨酸来测定产品中的甘氨酸的含量。设计实验,将所得粗产品中的甘氨酸分离出来形成非水体系直接用于滴定,方案为_______ 。
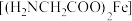 是一种新型治疗缺铁性贫血的药物,它和普通的药物相比没有铁腥味,不刺激肠胃。是一款无味、易溶于水而且不易变质的有机铁。其制备过程分为两个步骤:
是一种新型治疗缺铁性贫血的药物,它和普通的药物相比没有铁腥味,不刺激肠胃。是一款无味、易溶于水而且不易变质的有机铁。其制备过程分为两个步骤:Ⅰ.活性
 的制备:称取
的制备:称取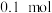 草酸亚铁晶体(
草酸亚铁晶体( )在隔绝空气的情况下加热至300℃,时间
)在隔绝空气的情况下加热至300℃,时间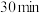 ,反应完成后冷却至室温。
,反应完成后冷却至室温。(1)冷却时需注意的操作是
(2)下图是将一定质量的草酸亚铁在氩气氛围中进行热重分析的示意图。B→C阶段反应的化学方程式为
 (残留固体质量/样品起始质量)
(残留固体质量/样品起始质量) ]。
]。
Ⅱ.甘氨酸亚铁的制备:
查阅资料:
甘氨酸( ) ) | 柠檬酸 | 甘氨酸亚铁 |
| 易溶于水,微溶于乙醇,可溶于冰醋酸 | 易溶于水和乙醇,酸性较强 | 易溶于水,难溶于乙醇、冰醋酸 |
 和少量柠檬酸,再加入
和少量柠檬酸,再加入 甘氨酸,通一段时间
甘氨酸,通一段时间 ,加入石蜡油。水浴加热至70℃,恒温搅拌6小时,剩余少量黑色不溶物。将所得混合物通过_______、_______,得到无色澄清溶液。向溶液中加入无水乙醇,生成白色沉淀,将沉淀过滤、洗涤得产品,将粗产品纯化后得精品。
,加入石蜡油。水浴加热至70℃,恒温搅拌6小时,剩余少量黑色不溶物。将所得混合物通过_______、_______,得到无色澄清溶液。向溶液中加入无水乙醇,生成白色沉淀,将沉淀过滤、洗涤得产品,将粗产品纯化后得精品。
(3)石蜡油的作用
(4)柠檬酸的作用
(5)步骤Ⅱ的两步操作分别为
(6)最后制得10.2g甘氨酸亚铁,则其产率为
(7)分析化学中甘氨酸的测定方法:在非水体系中用高氯酸标准溶液滴定甘氨酸来测定产品中的甘氨酸的含量。设计实验,将所得粗产品中的甘氨酸分离出来形成非水体系直接用于滴定,方案为
您最近一年使用:0次
2021-03-13更新
|
517次组卷
|
5卷引用:新疆维吾尔自治区喀什第六中学2022-2023学年高三上学期9月月考化学试题
19-20高一·全国·课后作业
名校
解题方法
3 . 下列关于铁及其化合物的说法正确的是 ( )
| A.铁是地壳中含量最多的金属元素,因此在日常生活中应用最广 |
| B.FeCl2溶液存放时,在溶液中放入少量的铁粉,目的是防止Fe2+被氧化 |
| C.隔绝空气的情况下,FeCl2溶液中加入Na2O2后得到白色沉淀Fe(OH)3 |
| D.FeO、Fe2O3、Fe3O4均为铁的氧化物,并且都是黑色 |
您最近一年使用:0次
2020-08-14更新
|
386次组卷
|
4卷引用:新疆乌鲁木齐市第八中学2021-2022学年高一上学期第二次月考化学试题
新疆乌鲁木齐市第八中学2021-2022学年高一上学期第二次月考化学试题(已下线)3.1.1 铁及其化合物练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)(已下线)【知识图鉴】单元讲练测必修第一册第三单元03巩固练北京市育英学校2023-2024学年高一上学期期末考试化学试题
名校
解题方法
4 . 下图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料。
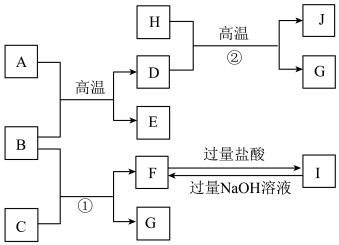
根据图示回答问题:
(1)写出下列物质的化学式:A______ ,E______ ;
(2)反应①的化学方程式是_________________________ ;反应②的化学方程式是___________________________ ;
(3)J与盐酸反应的化学方程式是______________________ ;反应后的溶液与足量的D反应的离子方程式是______________________ ,如何检验最后溶液中的阳离子:______________________________________ 。
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为__________________ 。

根据图示回答问题:
(1)写出下列物质的化学式:A
(2)反应①的化学方程式是
(3)J与盐酸反应的化学方程式是
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为
您最近一年使用:0次
2019-02-19更新
|
476次组卷
|
2卷引用:新疆维吾尔自治区生产建设兵团第一师高级中学2018-2019学年高一上学期期末考试化学试题



