名校
1 . 下列反应的离子方程式正确的是
A.少量 通入 通入 中: 中: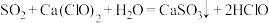 |
B.向二元弱酸 溶液中滴入足量烧碱溶液: 溶液中滴入足量烧碱溶液: |
C. 溶于HI溶液: 溶于HI溶液: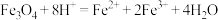 |
D.向含 的溶液通入标准状况下 的溶液通入标准状况下 : : |
您最近一年使用:0次
2 . 某实验小组探究Fe2+与H2O2反应中滴加KSCN溶液变红色后又褪色的原因,提出如下假设:
a.Fe3+被H2O2还原 b.SCN-被O2氧化 c.SCN-被H2O2氧化。
设计如下实验,下列说法错误的是
a.Fe3+被H2O2还原 b.SCN-被O2氧化 c.SCN-被H2O2氧化。
设计如下实验,下列说法错误的是
| 实验 | 滴加试剂 | 现象 |
| I | i.向2mLFeCl2溶液中滴加2滴0.1mol·L-1KSCN溶液 ii.再滴加5滴5%H2O2溶液(物质的量浓度约为1.5mol·L-1、pH约为5) | i.无明显现象 ii.溶液变红,大约10秒左右红色褪去,并测得生成了两种可直接排放到空气中的气体 |
| II | iii.取褪色后溶液两份,一份滴加FeC13溶液;另一份滴加KSCN溶液 iV.取褪色后溶液,滴加盐酸和BaCl2溶液 | iii.一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色 iV.产生白色沉淀 |
| III | V.向2mL0.1mol·L-1FeCl3溶液中滴加2滴0.1mol·L-1KSCN溶液,观察现象;后通入O2,观察现象 | V.先变红,通入氧气后无明显变化 |
| A.实验I褪色后的溶液中n(H+)变小 | B.通过实验II、III可验证假设c正确 |
C.实验II证明SCN-被氧化成SO | D.实验III的目的是排除假设b |
您最近一年使用:0次
名校
3 . 下列离子方程式正确的是
A.铜与稀硝酸: |
B.用 溶液吸收少量的 溶液吸收少量的 : : |
C. 溶液与足量NaOH溶液反应: 溶液与足量NaOH溶液反应: |
D.向 溶液中通入等物质的量的 溶液中通入等物质的量的 : :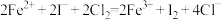 |
您最近一年使用:0次
2024-03-13更新
|
476次组卷
|
2卷引用:山东省青岛第二中学2023-2024学年高一上学期第二次月考化学试卷
名校
4 . 向500 含
含 、
、 、
、 的溶液中缓慢通入
的溶液中缓慢通入 L
L (标准状况),测得溶液中部分离子的物质的量与V的关系如图所示。下列叙述正确的是
(标准状况),测得溶液中部分离子的物质的量与V的关系如图所示。下列叙述正确的是

 含
含 、
、 、
、 的溶液中缓慢通入
的溶液中缓慢通入 L
L (标准状况),测得溶液中部分离子的物质的量与V的关系如图所示。下列叙述正确的是
(标准状况),测得溶液中部分离子的物质的量与V的关系如图所示。下列叙述正确的是
A.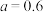 |
B. 时反应为 时反应为 |
C.原溶液中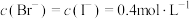 |
D.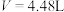 时总反应为 时总反应为 |
您最近一年使用:0次
2024-02-23更新
|
244次组卷
|
2卷引用:湖北省荆州八县市2023-2024学年高一上学期期末联考化学试题
5 . 用富含铁元素的食品,可以补充人体所需的铁元素。某班级研究性学习小组对菠菜中的铁元素展开了检测,实验如下:

(1)下列图示装置或操作合理的是________ 。
(2)写出试剂B的化学式___________ 。
(3)试剂C若为双氧水,请写出该反应的离子方程式:___________ ;该实验证明菠菜中含有的铁元素为_____ 价。
(4)其中一名同学在研究过程中向滤液A中先加入氯水,再加入试剂B,也看到溶液变红,由此也得出和其他同学一样的结论。他的做法是否正确?______ ,原因是什么?___________ 。
(5)另取少量滤液 ,向其中加入少量NaOH溶液,观察到的现象是
,向其中加入少量NaOH溶液,观察到的现象是________ ;原因是___________ 、________ (用离子方程式解释)。

(1)下列图示装置或操作合理的是
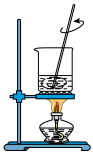 | 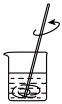 | 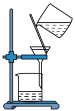 |  |
| A.灼烧 | B.溶解 | C.过滤 | D.检测菠菜液中的铁元素 |
(2)写出试剂B的化学式
(3)试剂C若为双氧水,请写出该反应的离子方程式:
(4)其中一名同学在研究过程中向滤液A中先加入氯水,再加入试剂B,也看到溶液变红,由此也得出和其他同学一样的结论。他的做法是否正确?
(5)另取少量滤液
 ,向其中加入少量NaOH溶液,观察到的现象是
,向其中加入少量NaOH溶液,观察到的现象是
您最近一年使用:0次
名校
6 . 实验室常采用点滴板来完成部分实验,这样既可以节约药品的用量,又便于观察实验现象。图中所示的实验点滴板上描述的实验现象或推论正确的是


A.往 固体中滴加 固体中滴加 溶液,有气体产生且生成大量的白色沉淀 溶液,有气体产生且生成大量的白色沉淀 |
| B.新制氯水滴加到pH试纸或淀粉KI溶液孔穴中,都体现新制氯水的漂白性 |
C.生锈铁屑加过量稀硫酸后,通过滴加 溶液的褪色来验证原溶液中存在 溶液的褪色来验证原溶液中存在 |
D.生锈铁屑加过量稀硫酸后,若滴加KSCN溶液变成血红色可验证原溶液存在 |
您最近一年使用:0次
7 . 室温下,探究0.1mol/LFeSO4溶液的性质,下列实验方案能达到探究目的的是
| 选项 | 探究目的 | 实验方案 |
| A | Fe2+能否催化H2O2分解 | 向2mL5%H2O2溶液中滴加几滴FeSO4溶液,观察气泡产生情况 |
| B | 溶液中是否含有Fe2+ | 向2mLFeSO4溶液中滴加几滴新制氯水,再滴加KSCN溶液,观察溶液颜色变化 |
| C | Fe2+是否水解 | 向2mLFeSO4溶液中滴加2~3滴酚酞试液,观察溶液颜色变化 |
| D | Fe2+是否有还原性 | 向2mLFeSO4溶液中滴加几滴酸性KMnO4溶液,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 为测定某补血剂样品(主要成分是硫酸亚铁晶体 )中铁元素的含量,某学兴趣小组设计了如下实验方案:
)中铁元素的含量,某学兴趣小组设计了如下实验方案:
方案一:将 转化为
转化为 ,测定质量变化.
,测定质量变化.
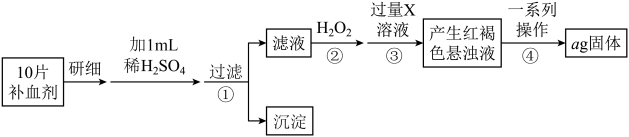
(1)写出步骤②中发生的反应的离子方程式__________________________
(2)步骤④中一系列操作依次是:过滤、洗涤、灼烧、冷却、称量,写出发生反应的化学方程式_______________________________ .
(3)假设实验无损耗,则每片补血剂含铁元素的质量为____________ g(用含a的代数式表示)。
方案二:用酸性 溶液滴定测定铁元素的含量
溶液滴定测定铁元素的含量
实验前,首先要准确配制 的酸性
的酸性 溶液250mL
溶液250mL
(4)计算所需 固体的质量为
固体的质量为____________ g.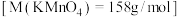
(5)配制溶液时,必须用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、________________
(6)配制过程中,下列操作导致溶液浓度偏小的是(填序号)_______
A.加水定容时俯视刻度线
B.定容加水时超过刻度线后,立即吸出多余的水
C.溶液从烧杯转移到容量瓶后没有洗涤烧杯
(7)若某同学取5片补血剂样品配成100mL溶液,取20.00mL,用上述操作配置的 溶液滴定,耗去
溶液滴定,耗去 ,反应的离子方程式为
,反应的离子方程式为______________________ ,每片补血剂含铁元素的质量____________ g(用代数式表示).
 )中铁元素的含量,某学兴趣小组设计了如下实验方案:
)中铁元素的含量,某学兴趣小组设计了如下实验方案:方案一:将
 转化为
转化为 ,测定质量变化.
,测定质量变化.
(1)写出步骤②中发生的反应的离子方程式
(2)步骤④中一系列操作依次是:过滤、洗涤、灼烧、冷却、称量,写出发生反应的化学方程式
(3)假设实验无损耗,则每片补血剂含铁元素的质量为
方案二:用酸性
 溶液滴定测定铁元素的含量
溶液滴定测定铁元素的含量实验前,首先要准确配制
 的酸性
的酸性 溶液250mL
溶液250mL(4)计算所需
 固体的质量为
固体的质量为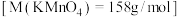
(5)配制溶液时,必须用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、
(6)配制过程中,下列操作导致溶液浓度偏小的是(填序号)
A.加水定容时俯视刻度线
B.定容加水时超过刻度线后,立即吸出多余的水
C.溶液从烧杯转移到容量瓶后没有洗涤烧杯
(7)若某同学取5片补血剂样品配成100mL溶液,取20.00mL,用上述操作配置的
 溶液滴定,耗去
溶液滴定,耗去 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次
名校
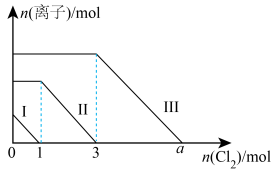
9 . 向 、
、 的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示(已知:
的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示(已知: 、
、 、
、 )。下列说法正确的是
)。下列说法正确的是
 、
、 的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示(已知:
的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示(已知: 、
、 、
、 )。下列说法正确的是
)。下列说法正确的是
A. |
B.折线II表示 的变化情况,折线III表示 的变化情况,折线III表示 的变化情况 的变化情况 |
C.若 ,溶液中发生离子反应: ,溶液中发生离子反应: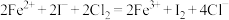 |
D.原溶液中 |
您最近一年使用:0次
2023-12-23更新
|
237次组卷
|
2卷引用:湖南省长沙市名校联合体2023-2024学年高一上学期第二次联考化学试题
10 . 对于下列实验,能正确描述其反应的离子方程式是
A.向饱和碳酸钠溶液中通入过量 : : |
B.向 溶液中通入过量的 溶液中通入过量的 : : |
C.漂白粉溶液中通入少量 气体: 气体: |
D.向 溶液中加入 溶液中加入 : : |
您最近一年使用:0次



