名校
1 . 下列反应的离子方程式正确的是
A.少量 通入 通入 中: 中: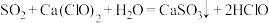 |
B.向二元弱酸 溶液中滴入足量烧碱溶液: 溶液中滴入足量烧碱溶液: |
C. 溶于HI溶液: 溶于HI溶液: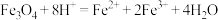 |
D.向含 的溶液通入标准状况下 的溶液通入标准状况下 : : |
您最近一年使用:0次
2 . 部分含铁物质的分类与相应铁元素的化合价关系如图。下列说法不正确的是
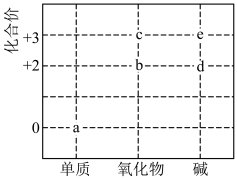
| A.b可被还原为a | B.d在空气中可被还原为e |
| C.一定条件下a能与水蒸气反应 | D.c溶于盐酸后所得溶液能使KSCN溶液变红 |
您最近一年使用:0次
3 . 下列离子方程式书写不正确的是
A.向 溴化亚铁溶液中通入标准状况下的 溴化亚铁溶液中通入标准状况下的 氯气: 氯气: |
B.硫酸亚铁溶液与稀硫酸、双氧水混合: |
C.碳酸钙溶于硝酸: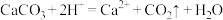 |
D.碳酸氢钠溶液与少量石灰水反应: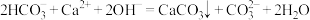 |
您最近一年使用:0次
4 . 某实验小组探究Fe2+与H2O2反应中滴加KSCN溶液变红色后又褪色的原因,提出如下假设:
a.Fe3+被H2O2还原 b.SCN-被O2氧化 c.SCN-被H2O2氧化。
设计如下实验,下列说法错误的是
a.Fe3+被H2O2还原 b.SCN-被O2氧化 c.SCN-被H2O2氧化。
设计如下实验,下列说法错误的是
| 实验 | 滴加试剂 | 现象 |
| I | i.向2mLFeCl2溶液中滴加2滴0.1mol·L-1KSCN溶液 ii.再滴加5滴5%H2O2溶液(物质的量浓度约为1.5mol·L-1、pH约为5) | i.无明显现象 ii.溶液变红,大约10秒左右红色褪去,并测得生成了两种可直接排放到空气中的气体 |
| II | iii.取褪色后溶液两份,一份滴加FeC13溶液;另一份滴加KSCN溶液 iV.取褪色后溶液,滴加盐酸和BaCl2溶液 | iii.一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色 iV.产生白色沉淀 |
| III | V.向2mL0.1mol·L-1FeCl3溶液中滴加2滴0.1mol·L-1KSCN溶液,观察现象;后通入O2,观察现象 | V.先变红,通入氧气后无明显变化 |
| A.实验I褪色后的溶液中n(H+)变小 | B.通过实验II、III可验证假设c正确 |
C.实验II证明SCN-被氧化成SO | D.实验III的目的是排除假设b |
您最近一年使用:0次
解题方法
5 . 电子工业常用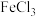 溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含
溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含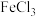 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得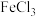 溶液,处理流程如下:
溶液,处理流程如下:
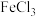 溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含
溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含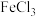 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得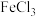 溶液,处理流程如下:
溶液,处理流程如下: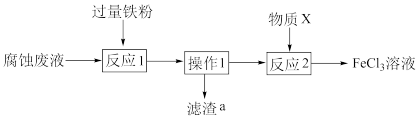
A. 溶液腐蚀铜箔的原理为 溶液腐蚀铜箔的原理为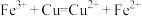 |
| B.反应1和反应2都发生了氧化还原反应 |
| C.实验室中进行操作1时,用到的主要玻璃仪器有漏斗、烧杯和玻璃棒 |
| D.滤渣a的主要成分是Cu和Fe,物质X可以选用氯气 |
您最近一年使用:0次
解题方法
6 . 在无色透明强酸性溶液中,能大量共存的离子组是
A. | B. |
C. | D.Na+、Fe2+、Ba2+、ClO- |
您最近一年使用:0次
7 . 下列离子方程式正确的是
| A.Na2O2放入水中:Na2O2+H2O=2Na++2OH-+O2↑ |
| B.Na投入FeSO4溶液:2Na+Fe2+=2Na++Fe |
| C.用铝粉和NaOH溶液反应制取少量H2:Al+OH-+3H2O=2[Al(OH)4]-+3H2↑ |
D.向AlCl3溶液中滴加足量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH |
您最近一年使用:0次
解题方法
8 . 向盛有氯气的集气瓶中,注入约五分之一容器体积的下列液体并轻轻振荡,观察到的现象记录如图所示。判断瓶中注入的液体是
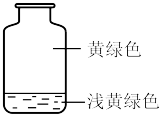

| A.AgNO3溶液 | B.NaOH溶液 | C.水 | D.FeCl2溶液 |
您最近一年使用:0次
9 . 下列说法不正确 的是
A. 为白色固体,易被空气氧化 为白色固体,易被空气氧化 |
B.工业上常用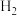 和 和 直接化合的方法生产氯化氢以制得盐酸 直接化合的方法生产氯化氢以制得盐酸 |
C.实验室常用 溶液吸收多余的 溶液吸收多余的 以避免污染 以避免污染 |
D.将废铁屑加入 溶液中,可用于除去工业废气中的 溶液中,可用于除去工业废气中的 |
您最近一年使用:0次
解题方法
10 . 下列反应的离子方程式正确的是
A.氯气尾气处理的原理: |
B.少量 通入 通入 溶液中: 溶液中: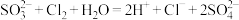 |
C.向红色 溶液中加入过量铁粉至溶液红色褪去: 溶液中加入过量铁粉至溶液红色褪去: |
| D.向含氯化亚铁的氯化铁溶液中通入适量氯气除杂质Fe2+:2Fe2++Cl2=2Fe3++2Clˉ |
您最近一年使用:0次



