1 . 如图是氮元素的几种化合价与物质类别的对应关系:

回答下列问题:
(1)写出N2的一种用途:___ 。
(2)从氮元素化合价分析,N2具有氧化性和还原性。写出氮气表现氧化性的一个化学方程式:__ 。
(3)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为___ 。
(4)实验室制取物质B的化学方程式为___ 。
(5)NO2与水反应生成物质A的化学方程式为___ 。
(6)浓硝酸与木炭在加热条件下反应的化学方程式为___ 。

回答下列问题:
(1)写出N2的一种用途:
(2)从氮元素化合价分析,N2具有氧化性和还原性。写出氮气表现氧化性的一个化学方程式:
(3)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为
(4)实验室制取物质B的化学方程式为
(5)NO2与水反应生成物质A的化学方程式为
(6)浓硝酸与木炭在加热条件下反应的化学方程式为
您最近一年使用:0次
2020-09-23更新
|
1438次组卷
|
3卷引用:高一必修第一册(鲁科2019)第3章 章末综合检测卷
2 . 如图是氮元素的几种价态与物质类别的对应关系。请回答下列问题:

(1)写出N2的一种用途:___ 。
(2)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为___ 。
(3)实验室制取物质B的化学方程式为____ 。
(4)NO2与水反应生成物质A的化学方程式为____ 。
(5)浓硝酸与木炭在加热条件下反应的化学方程式为___ 。

(1)写出N2的一种用途:
(2)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为
(3)实验室制取物质B的化学方程式为
(4)NO2与水反应生成物质A的化学方程式为
(5)浓硝酸与木炭在加热条件下反应的化学方程式为
您最近一年使用:0次
2019-12-05更新
|
594次组卷
|
6卷引用:鲁科版必修一2019—2020学年第三章检测试题
鲁科版必修一2019—2020学年第三章检测试题(已下线)第三单元 物质的性质与转化(基础过关)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)贵州省三穗县三中2019-2020学年高一上学期期末考试化学试题广西壮族自治区崇左市扶绥县第二中学2019-2020学年高一上学期期末考试化学试题广西壮族自治区来宾市金秀县民族中学2019-2020学年高一上学期期末考试化学试题(已下线)考点16 常见非金属元素单质及其重要化合物4——氮-2020年【衔接教材·暑假作业】新高三一轮复习化学
3 . 请分析下列各组物质,用序号填写出它们的对应关系:
①碳架异构、②官能团位置异构、③官能团类别异构、④顺反异构、⑤对映异构、⑥同一物(填序号)
(1)C2H5OH和CH3OCH3_____________________ ;
(2)
______________________ ;
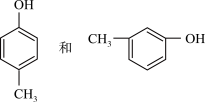
(3)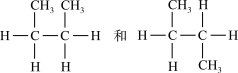
__________________ ;
(4)
________________________ ;
(5)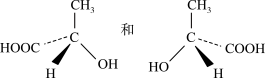
____________________________ ;
(6)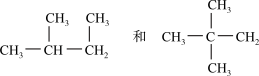
________________________________ ;
①碳架异构、②官能团位置异构、③官能团类别异构、④顺反异构、⑤对映异构、⑥同一物(填序号)
(1)C2H5OH和CH3OCH3
(2)

(3)
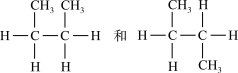
(4)

(5)

(6)
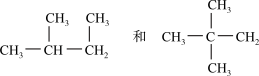
您最近一年使用:0次
2019-07-22更新
|
394次组卷
|
3卷引用:第一单元 有机化合物的结构与性质 烃(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版选修5)
(已下线)第一单元 有机化合物的结构与性质 烃(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版选修5)云南省丘北二中2018-2019学年高二下学期期末考试化学试题云南省玉溪市通海县第三中学2019-2020学年高二上学期12月月考化学试题
4 . 利用元素的化合价推测物质的性质是化学研究的重要手段。图是硫元素的常见化合价与部分物质类别的对应关系:
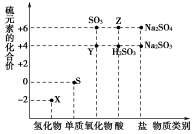
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有____________________ (填化学式)。
(2)将X与Y混合,可生成淡黄色固体。该反应中氧化剂与还原剂的物质的量之比为________ 。
(3)检验物质Y的方法是_________________________________________ 。
(4)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为______________________________________________________________ 。
(5)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是________ (填字母)。
a.Na2S+S b.Na2SO3+S
c.SO2+Na2SO4 d.Na2SO3+Na2SO4

(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
(2)将X与Y混合,可生成淡黄色固体。该反应中氧化剂与还原剂的物质的量之比为
(3)检验物质Y的方法是
(4)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为
(5)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是
a.Na2S+S b.Na2SO3+S
c.SO2+Na2SO4 d.Na2SO3+Na2SO4
您最近一年使用:0次
2018-09-05更新
|
550次组卷
|
2卷引用:2018-2019学年人教版高中化学必修一模块综合测评题(A)
21-22高一下·全国·单元测试
解题方法
5 . 氨气( )
)
(1)分子结构:由极性键形成的_______ 形的极性分子,N原子有一孤对电子;N为_______ 价,为N元素的最低价态;
(2)物理性质:_______ 气味的气体,密度比空气_______ ,_______ 溶于水,常温常压下1体积水能溶解_______ 体积的氨气,易_______ ;
(3)化学性质:
①与 反应:
反应:_______ ,溶液呈弱碱性,氨水的成分为:_______ ;氨水易_______ ;
②与酸反应:硫酸_______ ,盐酸_______ (有白烟生成);
③还原性(催化氧化):_______ (N为 价,最低价态,具有还原性);
价,最低价态,具有还原性);
(4)实验室制法_______ ;工业上采取 与
与 在高温高压催化剂条件下合成氨气;
在高温高压催化剂条件下合成氨气;
(5)用途:化工原料,制硝酸、氮肥等,做_______ 剂。
 )
)(1)分子结构:由极性键形成的
(2)物理性质:
(3)化学性质:
①与
 反应:
反应:②与酸反应:硫酸
③还原性(催化氧化):
 价,最低价态,具有还原性);
价,最低价态,具有还原性);(4)实验室制法
 与
与 在高温高压催化剂条件下合成氨气;
在高温高压催化剂条件下合成氨气;(5)用途:化工原料,制硝酸、氮肥等,做
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
6 . 【卷号】15000
【题号】3491666971516928
6 .
(1)硫
物理性质
硫为_______ 黄色晶体,俗称_______ 。密度比水_______ ,不溶于_______ ,微溶于_______ ,易溶于_______ 。
(2)(2)化学性质
硫元素位于第3周期VIA族,原子最外层有6个电子,在反应中易得到2个电子而呈-2价;硫元素的最高正价为+6价;单质硫中硫元素的化合价为0,处于中间价态,故单质硫既有_______ 又有_______ ,在反应中既可作_______ 又可作_______ 。如:
①氧化性:
i.与金属反应
Na+S Na2S(剧烈反应,轻微爆炸)
Na2S(剧烈反应,轻微爆炸)
2Al+3S Al2S3
Al2S3
Fe+S
_______ (黑色)
2Cu+S
_______ (黑色)
ii.与非金属反应:H2+S
_______
②还原性
S+O2 SO2(在空气中燃烧产生淡蓝色火焰,在纯氧中燃烧产生明亮的蓝紫色火焰,均产生刺激性气味。)
SO2(在空气中燃烧产生淡蓝色火焰,在纯氧中燃烧产生明亮的蓝紫色火焰,均产生刺激性气味。)
S+2H2SO4(浓) 3SO2↑+2H2O
3SO2↑+2H2O
【注意】硫与氧气反应只能生成SO2,不能生成SO3
③既有氧化性又有还原性:3S+6NaOH 2Na2S+Na2SO3+3H2O
2Na2S+Na2SO3+3H2O
【拓展】3S+6KOH——K2SO3+2K2S+3H2O(可用热碱液除去试管中残留的硫)
特性:Hg、Ag在常温下不跟O2反应,但易跟S反应。Hg+S——HgS(可用于消除室内洒落的Hg)
(3)存在与用途:游离态的硫主要存在于_______ 。化合态主要以化合物的形式存在。硫黄主要用于制造_______ 等,还用于制造黑火药、烟花爆竹等。
【题号】3491666971516928
6 .
(1)硫
物理性质
硫为
(2)(2)化学性质
硫元素位于第3周期VIA族,原子最外层有6个电子,在反应中易得到2个电子而呈-2价;硫元素的最高正价为+6价;单质硫中硫元素的化合价为0,处于中间价态,故单质硫既有
①氧化性:
i.与金属反应
Na+S
 Na2S(剧烈反应,轻微爆炸)
Na2S(剧烈反应,轻微爆炸)2Al+3S
 Al2S3
Al2S3Fe+S

2Cu+S

ii.与非金属反应:H2+S

②还原性
S+O2
 SO2(在空气中燃烧产生淡蓝色火焰,在纯氧中燃烧产生明亮的蓝紫色火焰,均产生刺激性气味。)
SO2(在空气中燃烧产生淡蓝色火焰,在纯氧中燃烧产生明亮的蓝紫色火焰,均产生刺激性气味。)S+2H2SO4(浓)
 3SO2↑+2H2O
3SO2↑+2H2O【注意】硫与氧气反应只能生成SO2,不能生成SO3
③既有氧化性又有还原性:3S+6NaOH
 2Na2S+Na2SO3+3H2O
2Na2S+Na2SO3+3H2O【拓展】3S+6KOH——K2SO3+2K2S+3H2O(可用热碱液除去试管中残留的硫)
特性:Hg、Ag在常温下不跟O2反应,但易跟S反应。Hg+S——HgS(可用于消除室内洒落的Hg)
(3)存在与用途:游离态的硫主要存在于
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
7 . 新型无机非金属材料
(1)硅单质
①Si位于元素周期表第_______ 周期,第_______ 族,处于金属与非金属过渡位置,为半导体材料。硅在地壳中含量仅次于氧,居第2位。
②硅在自然界的存在形态:没有游离态,只有化合态_______ 、硅酸盐。
③用途:主要用来做集成电路、晶体管、硅整流器等_______ 材料,还可以制成太阳能电池、硅的合金可用来制造变压器铁芯等。
(2)二氧化硅(硅石)
①SiO2是自然界中沙子、石英的主要成分。天然二氧化硅叫_______ ;结晶的二氧化硅叫_______ 。二氧化硅可以用来制造_______ ,具有优良的性能。
②光导纤维主要特性:①抗干扰性能好,不发生辐射;②通讯质量好;③质量轻、耐腐蚀。
(1)硅单质
①Si位于元素周期表第
②硅在自然界的存在形态:没有游离态,只有化合态
③用途:主要用来做集成电路、晶体管、硅整流器等
(2)二氧化硅(硅石)
①SiO2是自然界中沙子、石英的主要成分。天然二氧化硅叫
②光导纤维主要特性:①抗干扰性能好,不发生辐射;②通讯质量好;③质量轻、耐腐蚀。
您最近一年使用:0次
21-22高一下·全国·单元测试
8 . 蛋白质的用途:蛋白质是人类必需的营养物质,绝大多数酶是_______ ,是生物体内重要的_______ 。蛋白质在医药、食品、纺织等领域中有重要的应用价值。
您最近一年使用:0次
21-22高一下·全国·单元测试
9 . 纤维
(1)分类:天然纤维和化学纤维
①天然纤维:棉花、羊毛、蚕丝、麻等。
②化学纤维:再生纤维和合成纤维(再生纤维:用化学方法将农林产品中的_______ 、_______ 等天然高分子加工成黏纤化胶纤维、大豆蛋白纤维等;合成纤维:以石油、_______ 和煤等为原料制成有机小分子单体,再经聚合反应生产合成纤维:如_______ 、_______ 、腈纶、丙纶、氯纶、芳纶。)
(2)合成纤维的性质和用途
①性质:合成纤维具有_______ 、弹性好、耐磨、_______ 、不易_______ 等优良性能。
②用途:制作衣服、绳索、渔网、工业用滤布和_______ 、_______ 的结构材料等。
(1)分类:天然纤维和化学纤维
①天然纤维:棉花、羊毛、蚕丝、麻等。
②化学纤维:再生纤维和合成纤维(再生纤维:用化学方法将农林产品中的
(2)合成纤维的性质和用途
①性质:合成纤维具有
②用途:制作衣服、绳索、渔网、工业用滤布和
您最近一年使用:0次



