2025高三上·全国·专题练习
1 . 一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。称取TiO2样品0.60 g,消耗0.20 mol·L-1的NH4Fe(SO4)2溶液36.75 mL,则样品中TiO2的质量分数是_______ 。
您最近一年使用:0次
2025高三上·全国·专题练习
2 . 已知MnO2与浓盐酸反应的化学方程式为MnO2+ 4HCl(浓) MnCl2+Cl2↑+2H2O,回答下列问题:
MnCl2+Cl2↑+2H2O,回答下列问题:
(1)该反应的离子方程式为___________ 。
(2)被氧化的HCl占HCl总量的___________ 。
(3)当标准状况下有11.2 L氯气生成时,该反应转移的电子数为___________ (设NA为阿伏加德罗常数的值)。
(4)1.74 g MnO2与100 mL 12 mol·L-1的过量浓盐酸完全反应(假设HCl无挥发),在反应后的溶液中加入足量的AgNO3溶液,可生成___________ g沉淀。
 MnCl2+Cl2↑+2H2O,回答下列问题:
MnCl2+Cl2↑+2H2O,回答下列问题:(1)该反应的离子方程式为
(2)被氧化的HCl占HCl总量的
(3)当标准状况下有11.2 L氯气生成时,该反应转移的电子数为
(4)1.74 g MnO2与100 mL 12 mol·L-1的过量浓盐酸完全反应(假设HCl无挥发),在反应后的溶液中加入足量的AgNO3溶液,可生成
您最近一年使用:0次
3 . 某研究性学习小组,进行甲、乙、丙三组实验:各取 同浓度的盐酸,加入不同质量的同种铝合金颗粒,充分反应,产生气体。有关数据记录如下:
同浓度的盐酸,加入不同质量的同种铝合金颗粒,充分反应,产生气体。有关数据记录如下:
请回答以下问题:
(1)计算丙中产生气体的物质的量为___________ mol;
(2)实验中所用合金粉末中镁、铝的物质的量之比为___________ ;
(3)实验乙结束后的混合体系中加入一定量的NOH溶液,充分反应,得到固体M。如果固体M的质量不再减少,消耗NaOH的质量至少为___________ g。
 同浓度的盐酸,加入不同质量的同种铝合金颗粒,充分反应,产生气体。有关数据记录如下:
同浓度的盐酸,加入不同质量的同种铝合金颗粒,充分反应,产生气体。有关数据记录如下:| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量(g) | 1.008 | 1.260 | 1.512 |
| 生成气体体积(mL)(标况) | 1075.2 | 1344 | 1344 |
(1)计算丙中产生气体的物质的量为
(2)实验中所用合金粉末中镁、铝的物质的量之比为
(3)实验乙结束后的混合体系中加入一定量的NOH溶液,充分反应,得到固体M。如果固体M的质量不再减少,消耗NaOH的质量至少为
您最近一年使用:0次
名校
解题方法
4 . 为确定某一铁铜样品中各成份的含量,某同学进行了如下实验:准确称取一份质量为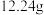 铁铜样品,逐渐加入一定体积某浓度的稀硝酸,每次实验充分反应后,测得生成
铁铜样品,逐渐加入一定体积某浓度的稀硝酸,每次实验充分反应后,测得生成 气体的体积为
气体的体积为 (已换成标准状况,假设生成的
(已换成标准状况,假设生成的 全部逸出),并测得剩余固体质量为
全部逸出),并测得剩余固体质量为 。各次实验的数据如下表:
。各次实验的数据如下表:
根据以上实验数据,请回答:
(1)上述实验当加入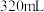 稀硝酸后,所发生反应的离子方程式为
稀硝酸后,所发生反应的离子方程式为______ 。
(2)稀硝酸的物质的量浓度为______  。
。
(3)样品中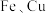 的物质的量之比为
的物质的量之比为______ 。
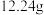 铁铜样品,逐渐加入一定体积某浓度的稀硝酸,每次实验充分反应后,测得生成
铁铜样品,逐渐加入一定体积某浓度的稀硝酸,每次实验充分反应后,测得生成 气体的体积为
气体的体积为 (已换成标准状况,假设生成的
(已换成标准状况,假设生成的 全部逸出),并测得剩余固体质量为
全部逸出),并测得剩余固体质量为 。各次实验的数据如下表:
。各次实验的数据如下表:稀硝酸体积 | 0 | 80 | 160 | 240 | 320 | 400 |
| 0 | 0.896 | 1.792 | 2.688 | 3.584 | 4.48 |
剩余固体质量 | 12.24 | 8.88 | 5.52 | 1.92 | 0 | 0 |
(1)上述实验当加入
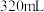 稀硝酸后,所发生反应的离子方程式为
稀硝酸后,所发生反应的离子方程式为(2)稀硝酸的物质的量浓度为
 。
。(3)样品中
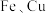 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
5 . 随着科学技术的进步,科学家研究出了种类繁多的合金来满足各行各业的需求。称取某镁铝合金 放入过量氢氧化钠溶液中,制得
放入过量氢氧化钠溶液中,制得 (标准状况下),试回答:
(标准状况下),试回答:
(1)目前用量最大的合金是__________ ;常见的一些合金硬度比其成分金属的__________ 。
(2)该合金中镁铝的物质的量之比是多少_______ (写出计算过程)。
 放入过量氢氧化钠溶液中,制得
放入过量氢氧化钠溶液中,制得 (标准状况下),试回答:
(标准状况下),试回答:(1)目前用量最大的合金是
(2)该合金中镁铝的物质的量之比是多少
您最近一年使用:0次
2024-01-24更新
|
46次组卷
|
2卷引用:山西省阳泉市2023-2024学年高一上学期期末教学质量监测化学试题
名校
解题方法
6 . 室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入 、
、 的混合气体和
的混合气体和 空气,此时活塞位置如图所AB所示,
空气,此时活塞位置如图所AB所示,

(1)A室混合气体的物质的量为__________ ,所含分子总数为__________ 。
(2)若将 、
、 的混合气体点燃引爆。活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来
的混合气体点燃引爆。活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来 、
、 的体积之比可能为
的体积之比可能为__________ 。若实验测得A室混合气体的质量为 ,则该混合气体的密度是同温同压下氧气密度的
,则该混合气体的密度是同温同压下氧气密度的__________ 倍。
 、
、 的混合气体和
的混合气体和 空气,此时活塞位置如图所AB所示,
空气,此时活塞位置如图所AB所示,
(1)A室混合气体的物质的量为
(2)若将
 、
、 的混合气体点燃引爆。活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来
的混合气体点燃引爆。活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来 、
、 的体积之比可能为
的体积之比可能为 ,则该混合气体的密度是同温同压下氧气密度的
,则该混合气体的密度是同温同压下氧气密度的
您最近一年使用:0次
名校
解题方法
7 . 将标准状况下的 气体溶于
气体溶于 水中(水的密度为
水中(水的密度为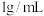 ),得到的盐酸密度为
),得到的盐酸密度为 (即
(即 ),则该盐酸的物质的量浓度是
),则该盐酸的物质的量浓度是__________ (请写出计算过程)。
 气体溶于
气体溶于 水中(水的密度为
水中(水的密度为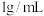 ),得到的盐酸密度为
),得到的盐酸密度为 (即
(即 ),则该盐酸的物质的量浓度是
),则该盐酸的物质的量浓度是
您最近一年使用:0次
名校
解题方法
8 . 相同温度和压强下,质量相等的氢气和甲烷,它们的体积之比为________ ,密度比为________ ;若把质量相等的这两种气体混合,则混合气体的平均相对分子质量为_______ (保留3位有效数字)。
您最近一年使用:0次
21-22高一上·浙江·阶段练习
解题方法
9 . 向含CuCl2和HCl的100g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图[仅考虑沉淀为Cu(OH)2]。求:_____ 。
(2)图像中,m1=_____ 。
(3)计算M点时溶液中溶质的质量分数_____ (结果保留到0.1%)。

(2)图像中,m1=
(3)计算M点时溶液中溶质的质量分数
您最近一年使用:0次
10 . 将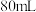 一定物质的量浓度的
一定物质的量浓度的 溶液分成A、B两等份,分别向A、B中通入物质的量不等的
溶液分成A、B两等份,分别向A、B中通入物质的量不等的 ,充分反应后,再继续向两溶液中分别逐滴加入
,充分反应后,再继续向两溶液中分别逐滴加入 的盐酸,边滴边振荡,产生的
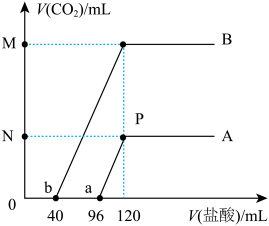
的盐酸,边滴边振荡,产生的 气体体积(假设所产生的气体全部逸出)与所加的盐酸体积之间的关系如图所示,回答下列问题:
气体体积(假设所产生的气体全部逸出)与所加的盐酸体积之间的关系如图所示,回答下列问题:
已知:①不考虑水电离出的 和
和 及
及 和
和 与水发生的反应;
与水发生的反应;
②不考虑溶液混合时引起的体积和温度的变化;
③只考虑反应过程中盐酸的酸性。
(1)由曲线A可知:
①相同状况下,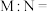
_______ 。
②P点溶液中,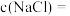
_______  (用含x的代数式表示)。
(用含x的代数式表示)。
(2)由曲线B可知:
①“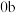 ”段发生反应的离子方程式为
”段发生反应的离子方程式为_______ 。
②向原B等份的 溶液中通入
溶液中通入 后,所得溶液中的溶质为
后,所得溶液中的溶质为_______ (填化学式),其质量之比为_______ 。
(3)若将M、N两处所产生的气体全部通入足量的某未知浓度的澄清石灰水中,所得沉淀的质量为_______ g(用含x的代数式表示,不考虑气体的逸出,下同),原 溶液中溶质的质量为
溶液中溶质的质量为_______ g。
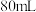 一定物质的量浓度的
一定物质的量浓度的 溶液分成A、B两等份,分别向A、B中通入物质的量不等的
溶液分成A、B两等份,分别向A、B中通入物质的量不等的 ,充分反应后,再继续向两溶液中分别逐滴加入
,充分反应后,再继续向两溶液中分别逐滴加入 的盐酸,边滴边振荡,产生的
的盐酸,边滴边振荡,产生的 气体体积(假设所产生的气体全部逸出)与所加的盐酸体积之间的关系如图所示,回答下列问题:
气体体积(假设所产生的气体全部逸出)与所加的盐酸体积之间的关系如图所示,回答下列问题:
已知:①不考虑水电离出的
 和
和 及
及 和
和 与水发生的反应;
与水发生的反应;②不考虑溶液混合时引起的体积和温度的变化;
③只考虑反应过程中盐酸的酸性。
(1)由曲线A可知:
①相同状况下,
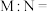
②P点溶液中,
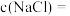
 (用含x的代数式表示)。
(用含x的代数式表示)。(2)由曲线B可知:
①“
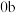 ”段发生反应的离子方程式为
”段发生反应的离子方程式为②向原B等份的
 溶液中通入
溶液中通入 后,所得溶液中的溶质为
后,所得溶液中的溶质为(3)若将M、N两处所产生的气体全部通入足量的某未知浓度的澄清石灰水中,所得沉淀的质量为
 溶液中溶质的质量为
溶液中溶质的质量为
您最近一年使用:0次