名校
1 . 根据下图和热反应方程式,写反应II的热化学方程___________ 。
反应III:S(s) + O2 (g)=SO2 (g) ΔH3 =−297 kJ/mol
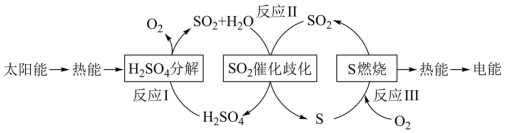
反应III:S(s) + O2 (g)=SO2 (g) ΔH3 =−297 kJ/mol
您最近一年使用:0次
2 . 如图为元素周期表的一部分,回答问题:___________ (填字母)。
A.离子键 B.极性共价键 C.非极性共价键
(2)C、N、O、F四种元素的原子半径由大到小的顺序是___________ 。
(3)PH3、H2S、HCl三种化合物的稳定性由强到弱的顺序是___________ 。
(4)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是___________ ,原子序数为___________ 。
(5)探究主族元素X、Y、Z的金属性递变规律
若X、Y、Z三种元素分别对应上图周期表中元素,则X的化学符号为___________ 。可以推出元素的金属性同一周期由左到右,逐渐___________ ,同一主族从上到下,逐渐___________ 。
(6)用一个离子方程式证明非金属性Cl>I:___________ 。

A.离子键 B.极性共价键 C.非极性共价键
(2)C、N、O、F四种元素的原子半径由大到小的顺序是
(3)PH3、H2S、HCl三种化合物的稳定性由强到弱的顺序是
(4)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是
(5)探究主族元素X、Y、Z的金属性递变规律
| 实验内容 | 实验现象 |
| i.各取1.0g形状相同的金属X和金属Z,分加入到5mL水中 | 金属X与水反应比金属Z剧烈 |
| ii.各取1.0g形状相同的金属Z和金属Y,分别加入5mL1.0mol/L盐酸中 | 金属Z与盐酸反应比金属Y剧烈 |
(6)用一个离子方程式证明非金属性Cl>I:
您最近一年使用:0次
名校
3 . Ⅰ.现有10种物质:①空气;②金刚石;③生石灰;④无水酒精;⑤稀硫酸;⑥干冰;⑦铜;⑧高锰酸钾;⑨水;⑩碳酸钠。用物质的序号填空:
(1)属于混合物的有___________ ,属于单质的有___________ 。
(2)属于碱性氧化物的有___________ ,属于盐类的有___________ 。
(3)属于非电解质的有___________ ,能导电的有___________ ,属于弱电解质的有___________ 。
Ⅱ.请对以下过程形成的物质进行分类:
①冰块加入水中后充分搅拌;
②向蒸馏水中加入过量碳酸钙;
③饱和氯化铁溶液中加入氢氧化钠溶液;
④碘和酒精的混合物;
⑤用烧杯盛放蒸馏水,用半透膜盛放氢氧化铁胶体并放入烧杯中,分离后烧杯中的液体;
⑥将纳米材料分散在塑料中制备复合材料。
(4)属于胶体的是___________ 。
(1)属于混合物的有
(2)属于碱性氧化物的有
(3)属于非电解质的有
Ⅱ.请对以下过程形成的物质进行分类:
①冰块加入水中后充分搅拌;
②向蒸馏水中加入过量碳酸钙;
③饱和氯化铁溶液中加入氢氧化钠溶液;
④碘和酒精的混合物;
⑤用烧杯盛放蒸馏水,用半透膜盛放氢氧化铁胶体并放入烧杯中,分离后烧杯中的液体;
⑥将纳米材料分散在塑料中制备复合材料。
(4)属于胶体的是
您最近一年使用:0次
4 . 回答下列问题。
(1)有下列反应:
①
②
③
④
上述反应中不属于氧化还原反应的是___________ (填序号,下同); 只作还原剂的是
只作还原剂的是___________ ;属于氧化还原反应,但其中的 既不被氧化,又不被还原的是
既不被氧化,又不被还原的是___________ 。
(2)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应: 。
。
①用双线桥标出电子转移的方向和数目___________ 。
②若消耗30g的NO得到还原产物的质量为___________ g。
(3)下列三个氧化还原反应中,氧化性最强的物质是___________ 。
①
②
③
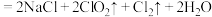
若溶质中 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还可以用上述反应中的
不被氧化,除单质外,还可以用上述反应中的___________ 做氧化剂。③中氧化产物是___________ ,还原产物是___________ 。
(1)有下列反应:
①

②

③

④

上述反应中不属于氧化还原反应的是
 只作还原剂的是
只作还原剂的是 既不被氧化,又不被还原的是
既不被氧化,又不被还原的是(2)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应:
 。
。①用双线桥标出电子转移的方向和数目
②若消耗30g的NO得到还原产物的质量为
(3)下列三个氧化还原反应中,氧化性最强的物质是
①

②

③

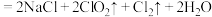
若溶质中
 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还可以用上述反应中的
不被氧化,除单质外,还可以用上述反应中的
您最近一年使用:0次
名校
解题方法
5 . 某化学兴趣小组的同学设计实验方案来制备氢氧化铁胶体,请思考并回答下列问题。
(1)按照下列实验操作来制备氢氧化铁胶体,不能达到预期目的的是_______。
(2)在制备Fe(OH)3胶体实验中,需要标识的图标是_______ (填序号)。_______ 。
(4)鉴别烧杯中制得的是胶体还是溶液,最常用的方法是_______ 。
(5)某同学认为Fe(OH)3胶体中可能含有FeCl3溶液,为了提纯Fe(OH)3胶体,他可以采用的提纯方法是_______ 。
(6)某同学按要求制备了Fe(OH)3胶体,但是他又向Fe(OH)3胶体中逐滴加入了稀H2SO4 溶液,结果出现了一系列变化。
①先出现红褐色沉淀,原因是_______ 。
②随后沉淀溶解,此反应的离子方程式是_______ 。
(7)在外加电场的情况下,发现Fe(OH)3胶粒向阴极移动,下列说法正确的是_______。
(1)按照下列实验操作来制备氢氧化铁胶体,不能达到预期目的的是_______。
| A.取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加稀的FeCl3溶液。继续煮沸 |
| B.取少量自来水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和FeCl3溶液。继续煮沸 |
| C.取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和FeCl3溶液。继续煮沸至液体呈透明的红褐色 |
| D.取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和FeCl3溶液。持续煮沸至液体变浑浊 |
(2)在制备Fe(OH)3胶体实验中,需要标识的图标是
a.  b.
b.  c.
c.  d.
d. 
(4)鉴别烧杯中制得的是胶体还是溶液,最常用的方法是
(5)某同学认为Fe(OH)3胶体中可能含有FeCl3溶液,为了提纯Fe(OH)3胶体,他可以采用的提纯方法是
(6)某同学按要求制备了Fe(OH)3胶体,但是他又向Fe(OH)3胶体中逐滴加入了稀H2SO4 溶液,结果出现了一系列变化。
①先出现红褐色沉淀,原因是
②随后沉淀溶解,此反应的离子方程式是
(7)在外加电场的情况下,发现Fe(OH)3胶粒向阴极移动,下列说法正确的是_______。
| A.Fe(OH)3胶体粒子能吸附阳离子,从而使Fe(OH)3胶体带正电荷 |
| B.能用过滤的方法除去Fe(OH)3胶体中的硝酸钾溶液 |
| C.Fe(OH)3溶胶中,胶体粒子的直径为1~100 nm |
| D.Fe(OH)3固体与水混合形成的分散系会产生丁达尔效应 |
您最近一年使用:0次
名校
解题方法
6 . I.按要求回答下列问题。
(1)已知H3PO3是二元酸,写出其与足量NaOH反应的化学方程式_______ 。
(2)下列各项与胶体性质有关的有_______ 。(填序号)
a.卤水点豆腐
b.明矾净水
c.油水分离
d.血液透析
e.酸碱中和
f.三角洲形成
g.制备氢氧化铁沉淀
h.臭氧消毒
(3)写出下列反应的离子方程式。
①NH4Fe(SO4)2与足量NaOH溶液反应:_______ 。
②澄清石灰水与少量NaHCO3溶液反应:_______ 。
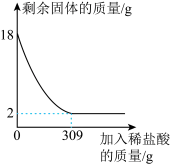
Ⅱ.已知赤铁矿石的主要成分为氧化铁。某课外兴趣小组的同学将18g赤铁矿石样品(杂质既不溶于水,也不参加反应)放入烧杯中,并不断加入稀盐酸,烧杯中固体的质量随加入稀盐酸的质量变化情况如图所示。_______ g。
(5)计算加入稀盐酸至恰好完全反应时所得溶液的溶质质量分数_______ 。
(1)已知H3PO3是二元酸,写出其与足量NaOH反应的化学方程式
(2)下列各项与胶体性质有关的有
a.卤水点豆腐
b.明矾净水
c.油水分离
d.血液透析
e.酸碱中和
f.三角洲形成
g.制备氢氧化铁沉淀
h.臭氧消毒
(3)写出下列反应的离子方程式。
①NH4Fe(SO4)2与足量NaOH溶液反应:
②澄清石灰水与少量NaHCO3溶液反应:
Ⅱ.已知赤铁矿石的主要成分为氧化铁。某课外兴趣小组的同学将18g赤铁矿石样品(杂质既不溶于水,也不参加反应)放入烧杯中,并不断加入稀盐酸,烧杯中固体的质量随加入稀盐酸的质量变化情况如图所示。
(5)计算加入稀盐酸至恰好完全反应时所得溶液的溶质质量分数
您最近一年使用:0次
名校
7 . 按要求书写离子方程式或者化学方程式
(1)向NaHSO4溶液中滴加NaHSO3溶液反应的离子方程式为_____ 。
(2)向NaHCO3溶液中滴加少量氢氧化钙溶液的离子方程式为_____ 。
(3)碳酸钙固体溶于醋酸溶液的化学方程式为_____ 。
(4)三氧化二铁固体溶于氢碘酸(HI)溶液中的离子方程式为_____ 。
(5)向含FeI2和FeBr2各1mol的混合液中通入氯气2mol,发生反应的离子方程式为_____ 。
(6)配平化学方程式,并用单线桥法标明电子转移的方向和数目。
①_____ 。
_____KMnO4+_____HCl(浓)═_____KCl+_____MnCl2+_____Cl2↑+_____H2O
②_____ 。
_____ClO﹣+_____Fe(OH)3+_____═_____Cl﹣+_____FeO +_____H2O
+_____H2O
(7)工业上采用无水芒硝(Na2SO4)碳粉还原法生产硫化钠(Na2S),若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生反应的化学方程式:_____ 。
(8)氯气能用于制备漂白液,但若温度过高会发生副反应生成NaCl、NaClO3.请写出在加热时,当NaOH与Cl2反应生成的n(NaClO):n(NaClO3)=5:1时,NaOH与Cl2反应的化学方程式:_____ 。
(1)向NaHSO4溶液中滴加NaHSO3溶液反应的离子方程式为
(2)向NaHCO3溶液中滴加少量氢氧化钙溶液的离子方程式为
(3)碳酸钙固体溶于醋酸溶液的化学方程式为
(4)三氧化二铁固体溶于氢碘酸(HI)溶液中的离子方程式为
(5)向含FeI2和FeBr2各1mol的混合液中通入氯气2mol,发生反应的离子方程式为
(6)配平化学方程式,并用单线桥法标明电子转移的方向和数目。
①
_____KMnO4+_____HCl(浓)═_____KCl+_____MnCl2+_____Cl2↑+_____H2O
②
_____ClO﹣+_____Fe(OH)3+_____═_____Cl﹣+_____FeO
 +_____H2O
+_____H2O(7)工业上采用无水芒硝(Na2SO4)碳粉还原法生产硫化钠(Na2S),若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生反应的化学方程式:
(8)氯气能用于制备漂白液,但若温度过高会发生副反应生成NaCl、NaClO3.请写出在加热时,当NaOH与Cl2反应生成的n(NaClO):n(NaClO3)=5:1时,NaOH与Cl2反应的化学方程式:
您最近一年使用:0次
名校
解题方法
8 . 按要求回答问题
(1)①铁片②CaCO3③氨水④醋酸铅⑤Na2O⑥亚硫酸⑦盐酸⑧KHSO4⑨蔗糖⑩CO2其中属于电解质的是_____ 属于非电解质的是_____ 属于强电解质的是_____ 能导电的是_____ (用序号) 。
(2)写出下列物质在水溶液中的电离方程式:
亚硫酸_____ ;KHSO4_____ 。
(3)①爆鸣气②液氯③铝热剂④普通玻璃⑤水玻璃⑥漂白粉⑦含氧40%的氧化镁⑧石油⑨福尔马林⑩CuSO4·5H2O⑪纯碱⑫分子式C2H4的烃⑬分子式为C5H10O2的有机物,以上物质中一定为纯净物的是_____ 可能是纯净物,也可能是混合物的是_____ (用序号) 。
(1)①铁片②CaCO3③氨水④醋酸铅⑤Na2O⑥亚硫酸⑦盐酸⑧KHSO4⑨蔗糖⑩CO2其中属于电解质的是
(2)写出下列物质在水溶液中的电离方程式:
亚硫酸
(3)①爆鸣气②液氯③铝热剂④普通玻璃⑤水玻璃⑥漂白粉⑦含氧40%的氧化镁⑧石油⑨福尔马林⑩CuSO4·5H2O⑪纯碱⑫分子式C2H4的烃⑬分子式为C5H10O2的有机物,以上物质中一定为纯净物的是
您最近一年使用:0次
名校
解题方法
9 . 离子反应是中学化学中重要的反应类型,回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在_______ (填序号)。
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)将两种化合物一起溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子:K+、Mg2+、Fe3+、Ba2+、S 、OH-、C
、OH-、C 和Cl-,取该溶液进行如下实验:
和Cl-,取该溶液进行如下实验:
Ⅰ.取少量溶液滴入紫色石蕊溶液,溶液呈蓝色。
Ⅱ.取少许溶液滴入BaCl2溶液,无白色沉淀产生。
Ⅲ.另取少许溶液先滴加硝酸再加AgNO3溶液,产生白色沉淀。
Ⅳ.再取少许原溶液滴入少量H2SO4溶液,有白色沉淀产生。
①根据以上现象判断,原溶液中肯定不存在的离子是_______ ,肯定存在的离子是_______ 。
②写出实验Ⅲ中可能发生反应的离子方程式:_______ 。
③如溶液中各种离子的个数相等,确定溶液中____ (填“有”或“无”)K+,判断依据是_______ 。
(1)在发生离子反应的反应物或生成物中,一定存在
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)将两种化合物一起溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子:K+、Mg2+、Fe3+、Ba2+、S
 、OH-、C
、OH-、C 和Cl-,取该溶液进行如下实验:
和Cl-,取该溶液进行如下实验:Ⅰ.取少量溶液滴入紫色石蕊溶液,溶液呈蓝色。
Ⅱ.取少许溶液滴入BaCl2溶液,无白色沉淀产生。
Ⅲ.另取少许溶液先滴加硝酸再加AgNO3溶液,产生白色沉淀。
Ⅳ.再取少许原溶液滴入少量H2SO4溶液,有白色沉淀产生。
①根据以上现象判断,原溶液中肯定不存在的离子是
②写出实验Ⅲ中可能发生反应的离子方程式:
③如溶液中各种离子的个数相等,确定溶液中
您最近一年使用:0次
名校
10 . 回答下列问题:
(1)已知某有机化合物的结构简式为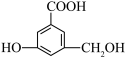 。请回答下列问题:
。请回答下列问题:
①乙二酸与乙二醇反应生成高聚酯:______ 。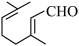 )分子中含官能团的实验方案,需愿考如下问题。
)分子中含官能团的实验方案,需愿考如下问题。
①检验分子中醛基常用的试剂是______ ,化学方程式:______ 。
②若只有三种试剂,a溴水、b新制的氢氧化铜、c稀硫酸,应先检验的官能团是______ ,原因______ ;加入试剂顺序为______ (字母顺序)。
(1)已知某有机化合物的结构简式为
 。请回答下列问题:
。请回答下列问题:①当与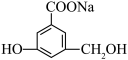 。
。
②当与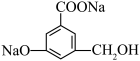 。
。
③当与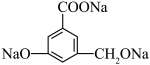 。
。
①乙二酸与乙二醇反应生成高聚酯:
②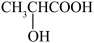 自身酯化生成环酯:
自身酯化生成环酯:
 )分子中含官能团的实验方案,需愿考如下问题。
)分子中含官能团的实验方案,需愿考如下问题。①检验分子中醛基常用的试剂是
②若只有三种试剂,a溴水、b新制的氢氧化铜、c稀硫酸,应先检验的官能团是
您最近一年使用:0次



