解题方法
1 . 下表为元素周期表中的一部分,表中列出10种元素在周期表中的位置,按要求回答下列各题。
(1)这10种元素中,化学性质最稳定的元素是_____ (写元素符号)。
(2)地壳中含量最丰富的元素是_____ (写元素名称)。
(3)元素①②③最高价氧化物对应的水化物,碱性最强的物质名称是_____
(4)元素⑥的氢化物的化学式是_____ (写一种)。
(5)④⑥⑦中原子半径由大到小的顺序是_____ (写元素名称)
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ④ | ⑥ | ⑦ | |||||
| 3 | ① | ② | ③ | ⑤ | ⑧ | ⑨ | ⑩ | |
(1)这10种元素中,化学性质最稳定的元素是
(2)地壳中含量最丰富的元素是
(3)元素①②③最高价氧化物对应的水化物,碱性最强的物质名称是
(4)元素⑥的氢化物的化学式是
(5)④⑥⑦中原子半径由大到小的顺序是
您最近一年使用:0次
解题方法
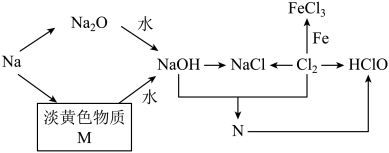
2 . 钠元素、氯元素及其它们对应的化合物有如下图转化关系。淡黄色物质M可在潜水艇中作为氧气的来源,常被用作供氧剂,物质N常被用来杀菌消毒。请按要求填空: ___________ 中;金属钠在空气中燃烧时火焰颜色呈___________ 色。
(2)写出物质M与水反应的化学方程式:___________ ,该反应中的氧化剂为___________ ;当生成标准状况下的氧气11.2 L时,转移电子数目为___________ (用NA表示阿伏加德罗常数的值)。
(3)新制的氯水呈___________ 色,放置一段时间后,溶液的pH___________ (填“增大”或“减小”)。
(4)物质N在空气中的CO2作用下,能产生有漂白、杀菌作用的次氯酸,该反应的化学方程式为NaClO+CO2+H2O=NaHCO3+HClO,该反应___________ (填“属于”或“不属于”)氧化还原反应。
(5)在酸性条件下,向铬废水中加入绿矾(FeSO4·7H2O),可将Cr2O 还原为Cr3+,该反应的离子方程式为
还原为Cr3+,该反应的离子方程式为___________ 。
(2)写出物质M与水反应的化学方程式:
(3)新制的氯水呈
(4)物质N在空气中的CO2作用下,能产生有漂白、杀菌作用的次氯酸,该反应的化学方程式为NaClO+CO2+H2O=NaHCO3+HClO,该反应
(5)在酸性条件下,向铬废水中加入绿矾(FeSO4·7H2O),可将Cr2O
 还原为Cr3+,该反应的离子方程式为
还原为Cr3+,该反应的离子方程式为
您最近一年使用:0次
解题方法
3 . 表列出了①~⑨九种元素在周期表中的位置:
(1)①~⑨九种元素中原子半径最大的是__________ (填元素符号)。
(2)元素③的原子结构示意图为__________ ;元素①与⑨组成的化合物的电子式:___________ ;由⑤、⑥两种元素组成的化合物的化学键类型为__________ (“离子键”或“共价键”)。
(3)元素③、④的简单氢化物的稳定性较弱的是_____________ (填化学式);元素⑧、⑨的最高价氧化物对应的水化物中,酸性较强的是_____________ (填化学式)。
(4)元素①与②所形成的最简单有机物的空间结构是__________ ,该物质与⑨的单质在光照下发生反应,该反应的产物是__________ (填“纯净物”或“混合物”)。元素①与②所形成的最简单烯烃为M,写出M与元素⑨的单质在一定条件下反应的化学方程式:_____________ ,该反应类型为__________ 。
(5)元素⑥的单质在空气中燃烧生成__________ 色固体,此固体与二氧化碳反应的化学方程式为____________ 。
族 周期 | IA | 0 | ||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(2)元素③的原子结构示意图为
(3)元素③、④的简单氢化物的稳定性较弱的是
(4)元素①与②所形成的最简单有机物的空间结构是
(5)元素⑥的单质在空气中燃烧生成
您最近一年使用:0次
解题方法
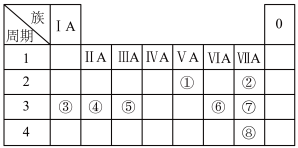
4 . 下表列出了①~⑧八种元素在周期表中的位置。
(1)元素①的原子结构示意图:________ 。
(2)元素③与⑥组成的化合物的电子式:_______ 。
(3)元素②、③的离子中,半径较大的是_______ (填化学式)。
(4)元素④的单质与盐酸反应的离子方程式:________ 。
(5)元素⑤的最高价氧化物是______ (填“酸性”“碱性”或“两性”)氧化物。
(6)元素⑦、⑧形成单质的氧化性较弱的是______ (填化学式),从实验证据的角度列举能证明其氧化性强弱关系的反应:_______ (填化学方程式)。
(7)已知硒(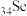 )与⑥同主族,请根据硒元素在元素周期表中的位置,推测硒及其化合物可能具有的性质:
)与⑥同主族,请根据硒元素在元素周期表中的位置,推测硒及其化合物可能具有的性质:_______ (填序号)。
a.Se的最低负化合价为-2价 b. 既有氧化性又有还原性
既有氧化性又有还原性
c.Se的气态氢化物的稳定性比⑥的强 d.最高价氧化物对应的水化物为
(1)元素①的原子结构示意图:
(2)元素③与⑥组成的化合物的电子式:
(3)元素②、③的离子中,半径较大的是
(4)元素④的单质与盐酸反应的离子方程式:
(5)元素⑤的最高价氧化物是
(6)元素⑦、⑧形成单质的氧化性较弱的是
(7)已知硒(
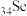 )与⑥同主族,请根据硒元素在元素周期表中的位置,推测硒及其化合物可能具有的性质:
)与⑥同主族,请根据硒元素在元素周期表中的位置,推测硒及其化合物可能具有的性质:a.Se的最低负化合价为-2价 b.
 既有氧化性又有还原性
既有氧化性又有还原性c.Se的气态氢化物的稳定性比⑥的强 d.最高价氧化物对应的水化物为

您最近一年使用:0次
解题方法
5 . 物质类别和元素价态,是学习元素及其化合物性质的重要认识视角。下图中X、Y、Z三种物质均含有Na元素。
(1)X的化学式为_______ ,X与水反应生成Z和 ,该反应的氧化剂是
,该反应的氧化剂是________ 。
(2)钠长期置于空气中,最后形成的物质是______ (填化学式),通常将钠保存在______ 中。
(3)钠与水反应的离子方程式为_______ 。
(4)写出淡黄色固体Y与二氧化碳反应的化学方程式:______ 。
(5)纯碱和小苏打都是重要的化工原料,某同学设计如下几组实验方法鉴别纯碱和小苏打。_____ 。
②乙和丙两组实验对比,丙组能更便捷的验证两者的热稳定性,丙组实验中B处盛放的物质应为_____ (填化学式)。
(6)取10g 和
和 固体混合物充分加热,质量减少3.1g,则原混合物中
固体混合物充分加热,质量减少3.1g,则原混合物中 的质量为
的质量为_____ g。
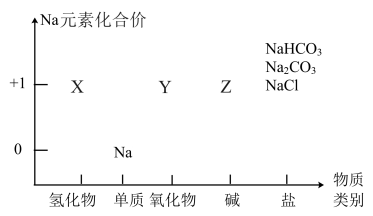
(1)X的化学式为
 ,该反应的氧化剂是
,该反应的氧化剂是(2)钠长期置于空气中,最后形成的物质是
(3)钠与水反应的离子方程式为
(4)写出淡黄色固体Y与二氧化碳反应的化学方程式:
(5)纯碱和小苏打都是重要的化工原料,某同学设计如下几组实验方法鉴别纯碱和小苏打。
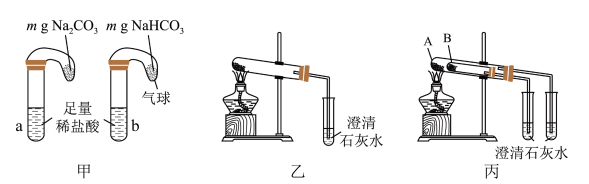
②乙和丙两组实验对比,丙组能更便捷的验证两者的热稳定性,丙组实验中B处盛放的物质应为
(6)取10g
 和
和 固体混合物充分加热,质量减少3.1g,则原混合物中
固体混合物充分加热,质量减少3.1g,则原混合物中 的质量为
的质量为
您最近一年使用:0次
解题方法
6 . 现有部分短周期元素的性质或原子结构如表:
(1)元素T在周期表中的位置为___________ 。
(2)元素X、Y的简单离子中,半径较小的是:___________ (填离子符号)。
(3)元素Z与元素T相比,非金属性较强的是___________ (填元素符号),下列表述中能证明这一事实的是___________ 。
①常温下Z的单质是气体,T的单质是固体
②Z的氢化物比T的稳定
③Z最高价氧化物对应水化物的酸性比T的强
(4)X、Z元素的最高价氧化物对应的水化物之间反应的离子方程式为___________ 。
| 元素编号 | 元素性质或原子结构 |
| T | M层上有6个电子 |
| X | 短周期中原子半径最大的主族元素 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高化合价是+7价 |
(2)元素X、Y的简单离子中,半径较小的是:
(3)元素Z与元素T相比,非金属性较强的是
①常温下Z的单质是气体,T的单质是固体
②Z的氢化物比T的稳定
③Z最高价氧化物对应水化物的酸性比T的强
(4)X、Z元素的最高价氧化物对应的水化物之间反应的离子方程式为
您最近一年使用:0次
7 . 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。根据题意回答下列问题:
(1)①的元素符号是___________ ;
(2)③、④的原子半径大小是:③___________ ④(填“>”或“<”);
(3)②、⑤的非金属性从强到弱的顺序是:___________ (填元素符号);
(4)③的最高价氧化物的水化物和④的最高价氧化物的水化物在溶液中反应的离子方程式为___________ 。
| 族 周期 | IA | 0 | |||||||
| 1 | ⅡA | ⅢA | ⅣA | VA | VIA | ⅦA | |||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | Ar | |||||
(2)③、④的原子半径大小是:③
(3)②、⑤的非金属性从强到弱的顺序是:
(4)③的最高价氧化物的水化物和④的最高价氧化物的水化物在溶液中反应的离子方程式为
您最近一年使用:0次
解题方法
8 . 下表是元素周期表的部分内容,请根据表中信息回答下列问题:____ 种元素。
(2)①-④的四种元素中非金属性最强的是______ (填序号)。
(3)元素②和元素④的原子中半径较大的是______ (填元素符号)。
(4)元素④的最高价氧化物对应的水化物是______ (填“强”或“弱”)酸。
(5)元素③的单质_____ (填“能”或“不能”)与水反应。
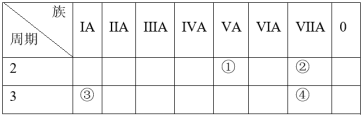
(2)①-④的四种元素中非金属性最强的是
(3)元素②和元素④的原子中半径较大的是
(4)元素④的最高价氧化物对应的水化物是
(5)元素③的单质
您最近一年使用:0次
9 . 无机盐X(仅含两种元素)可通过单质甲与Ca(OH)2浊液共热的方法来制备,某同学为探究X的组成和性质,设计了如下实验(流程图中部分产物已略去)。
(1)甲的化学式为______ 。
(2)X的化学式为______ 。
(3)在澄清石灰水中通入少量气体丙,反应的离子方程式为____ 。
(4)将气体乙通入气体丙的水溶液中的现象为_______ 。
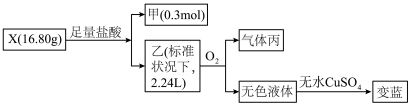
(1)甲的化学式为
(2)X的化学式为
(3)在澄清石灰水中通入少量气体丙,反应的离子方程式为
(4)将气体乙通入气体丙的水溶液中的现象为
您最近一年使用:0次
解题方法
10 . 下表列出了①~⑦七种元素在周期表中的位置。
请按要求回答下列问题。
(1)写出③和⑤形成的化合物的化学式________ 。
(2)画出⑥的原子结构示意图________ 。
(3)写出⑦形成的单质的电子式________ 。
(4)比较①和②原子半径大小________ (用元素符号表示)。
(5)写出③常见的单质与④的单质在加热条件下反应的化学方程式________________ 。
族 周期 | ⅠA | 0 | ||||||
1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ||||
(1)写出③和⑤形成的化合物的化学式
(2)画出⑥的原子结构示意图
(3)写出⑦形成的单质的电子式
(4)比较①和②原子半径大小
(5)写出③常见的单质与④的单质在加热条件下反应的化学方程式
您最近一年使用:0次



