1 . 利用下列装置(夹持装置省略)进行实验,能达到实验目的的是
|
|
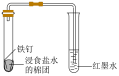
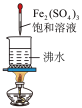
| A.证明氯水中有酸 | B.观察铁的的吸氧腐蚀 |
|
|
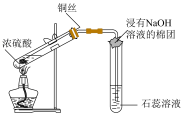
| C.制备Fe(OH)3胶体 | D.检验二氧化硫的漂白性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 下列实验操作能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 制备 胶体 胶体 | 将NaOH浓溶液滴加到饱和 溶液中 溶液中 |
B | 检验乙醇和浓硫酸加热生成乙烯 | 将产生的气体通入酸性 溶液中 溶液中 |
C | 检验久置的 溶液是否被完全氧化 溶液是否被完全氧化 | 取少量待测液,滴加 溶液 溶液 |
D | 探究浓度对反应速率的影响 | 常温下将铁片分别插入稀硝酸和浓硝酸中 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
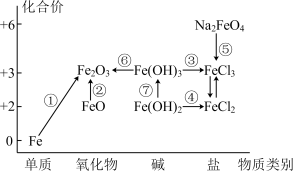
3 . 元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的“价一类”二维图,箭头表示部分物质间的转化关系。
(1) 中Fe的化合价为
中Fe的化合价为______________________ 。
(2)磁性氧化铁的化学式为______________________ ,将其完全溶于较浓的盐酸中,其反应的离子方程式为______________________ 。
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
______________________ 。
(4)根据下左图装置,用NaOH 溶液、铁屑、稀 等试剂制备
等试剂制备 沉淀。
沉淀。______________________ 。
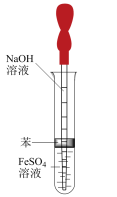
②在I和Ⅱ中加入试剂后,应先______________________ (选填“打开”或“关闭”)止水夹。某同学用上右图装置也可制备 沉淀,原因是
沉淀,原因是______________________ 。
(5)已知 在强碱溶液中稳定存在,pH越小稳定性越差;则制备
在强碱溶液中稳定存在,pH越小稳定性越差;则制备 时需要在
时需要在______________________ (填“酸性”“碱性”或“中性”)环境中进行;  也可以作为净水剂,能与水反应生成具有吸附性的 Fe(OH)₃胶体和一种无色无味气体,写出其中离子方程式:
也可以作为净水剂,能与水反应生成具有吸附性的 Fe(OH)₃胶体和一种无色无味气体,写出其中离子方程式:______________________ 。检验溶液中 的试剂是
的试剂是______________________ 。
(1)
 中Fe的化合价为
中Fe的化合价为(2)磁性氧化铁的化学式为
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(4)根据下左图装置,用NaOH 溶液、铁屑、稀
 等试剂制备
等试剂制备 沉淀。
沉淀。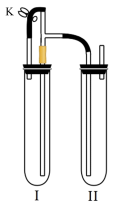
②在I和Ⅱ中加入试剂后,应先
 沉淀,原因是
沉淀,原因是(5)已知
 在强碱溶液中稳定存在,pH越小稳定性越差;则制备
在强碱溶液中稳定存在,pH越小稳定性越差;则制备 时需要在
时需要在 也可以作为净水剂,能与水反应生成具有吸附性的 Fe(OH)₃胶体和一种无色无味气体,写出其中离子方程式:
也可以作为净水剂,能与水反应生成具有吸附性的 Fe(OH)₃胶体和一种无色无味气体,写出其中离子方程式: 的试剂是
的试剂是
您最近半年使用:0次
4 . 某校化学学习小组探究 与
与 溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有
溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有 固体。回答下列问题:
固体。回答下列问题:
(1)写出实验中制备 的化学方程式
的化学方程式________ 。
(2)配制100mL
 溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和
溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和________ 。
【实验探究】
向3mL
 溶液中通入
溶液中通入 ,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
猜想1: 水解产生了红棕色的
水解产生了红棕色的 胶体;
胶体;
猜想2: 与溶液中某种
与溶液中某种 价含硫微粒形成了红棕色的配合物。
价含硫微粒形成了红棕色的配合物。
(3)为验证上述猜想,甲同学用激光笔照射该红棕色溶液,________ ,证明猜想1不成立。
(4)乙同学查阅文献得知猜想2正确,并设计了下表3组实验,以确定红棕色配合物的配体是 、
、 、
、 中的哪一种(实验均在常温下进行)。
中的哪一种(实验均在常温下进行)。
已知:常温下,溶液中 价含硫微粒物质的量分数随pH变化曲线如图所示。
价含硫微粒物质的量分数随pH变化曲线如图所示。________ (填写微粒符号),依据的实验证据是________ 。
(5)丙同学查阅资料得知:
利用分光光度计可测定溶液中有色物质的吸光度,吸光度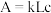 ,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
丙同学经过思考,认为乙同学的实验方案不严谨,除了pH会影响溶液红棕色的深浅,还有一个因素也可能会影响溶液红棕色的深浅。于是设计如下实验进行探究,请帮助该同学完成实验方案,填写下表中空白处。
实验结果讨论:若 ,则该因素不影响溶液红棕色的深浅;若
,则该因素不影响溶液红棕色的深浅;若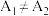 ,则该因素会影响溶液红棕色的深浅。
,则该因素会影响溶液红棕色的深浅。
(6)丁同学查阅资料得知:
配合物在溶液中存在解离平衡,如: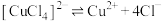 。
。
丁同学设计实验,利用分光光度计测定上述溶液中红棕色物质的吸光度,证明解离平衡的存在。请完成表中内容。
实验限选试剂为: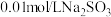 溶液,
溶液,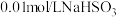 溶液,
溶液, 固体,
固体,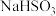 固体
固体
 与
与 溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有
溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有 固体。回答下列问题:
固体。回答下列问题: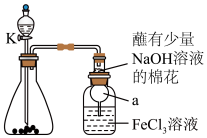
(1)写出实验中制备
 的化学方程式
的化学方程式(2)配制100mL

 溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和
溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和【实验探究】
向3mL

 溶液中通入
溶液中通入 ,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:猜想1:
 水解产生了红棕色的
水解产生了红棕色的 胶体;
胶体;猜想2:
 与溶液中某种
与溶液中某种 价含硫微粒形成了红棕色的配合物。
价含硫微粒形成了红棕色的配合物。(3)为验证上述猜想,甲同学用激光笔照射该红棕色溶液,
(4)乙同学查阅文献得知猜想2正确,并设计了下表3组实验,以确定红棕色配合物的配体是
 、
、 、
、 中的哪一种(实验均在常温下进行)。
中的哪一种(实验均在常温下进行)。组别 | 溶液1(1mL) | 溶液2(2mL) | 现象 |
a |
|
| 溶液1和溶液2混合后,组别a、b、c所得溶液红棕色依次加深。 |
b |  的饱和溶液,用 的饱和溶液,用 固体调节. 固体调节. | ||
c |  的饱和溶液,用 的饱和溶液,用 固体调节 固体调节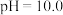 |
 价含硫微粒物质的量分数随pH变化曲线如图所示。
价含硫微粒物质的量分数随pH变化曲线如图所示。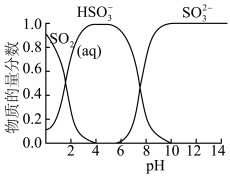
(5)丙同学查阅资料得知:
利用分光光度计可测定溶液中有色物质的吸光度,吸光度
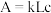 ,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。丙同学经过思考,认为乙同学的实验方案不严谨,除了pH会影响溶液红棕色的深浅,还有一个因素也可能会影响溶液红棕色的深浅。于是设计如下实验进行探究,请帮助该同学完成实验方案,填写下表中空白处。
实验序号 | 操作 | 吸光度 |
1 | 把1mL 0.1mol/L 溶液与2mL 溶液与2mL 饱和溶液混合均匀,溶液变成红棕色,测定溶液中红棕色物质的吸光度。 饱和溶液混合均匀,溶液变成红棕色,测定溶液中红棕色物质的吸光度。 |
|
2 |
|
 ,则该因素不影响溶液红棕色的深浅;若
,则该因素不影响溶液红棕色的深浅;若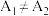 ,则该因素会影响溶液红棕色的深浅。
,则该因素会影响溶液红棕色的深浅。(6)丁同学查阅资料得知:
配合物在溶液中存在解离平衡,如:
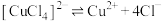 。
。丁同学设计实验,利用分光光度计测定上述溶液中红棕色物质的吸光度,证明解离平衡的存在。请完成表中内容。
实验限选试剂为:
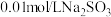 溶液,
溶液,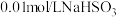 溶液,
溶液, 固体,
固体,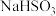 固体
固体实验序号 | 操作 | 吸光度 | 结论 |
3 | 向3mL 0.1mol/L 溶液中通入 溶液中通入 ,溶液立即由黄色变成红棕色,测定溶液中红棕色物质的吸光度 ,溶液立即由黄色变成红棕色,测定溶液中红棕色物质的吸光度 |
| |
4 |
  (填“大于”、“小于”或“等于”) (填“大于”、“小于”或“等于”) | 平衡向 |
您最近半年使用:0次
解题方法
5 . 化学处处呈现美。下列有关说法正确的是
| A.干冰制造舞台烟雾发生了共价键断裂 |
| B.“日照澄洲江雾开”的现象属于丁达尔效应 |
| C.“铁水打花”又叫打铁花,利用了铁元素的焰色试验 |
D.“雨过天背云破处,这般颜色做将来”,瓷器青色来自 |
您最近半年使用:0次
解题方法
6 . 经实验发现,一般的溶液几乎都有丁达尔效应(粒子对光的散射现象),且丁达尔现象随其浓度升高逐渐增强,胶体的丁达尔现象比溶液的强。现用以下装置区别FeCl3溶液和Fe(OH)3胶体,下列说法不正确的是
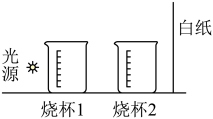
| A.烧杯1中盛放溶液,烧杯2中盛放胶体时,两个烧杯中均有明显的丁达尔现象 |
| B.烧杯1中盛放胶体,烧杯2中盛放溶液时,胶体有明显的丁达尔现象,溶液无明显现象 |
| C.将烧杯1和2中的液体互换,出现二次丁达尔现象的为溶液,只出现一次丁达尔现象的为胶体 |
| D.将烧杯1和2中的液体互换,只出现一次丁达尔现象的为溶液,出现二次丁达尔现象的为胶体 |
您最近半年使用:0次
解题方法
7 . 科技是国家强盛之基,创新是民族进步之魂。下列说法正确的是
| A.“长江2000”突破新技术,其燃料煤油属于可再生能源 |
| B.“九章三号”跑出新速度,其芯片材料的主要成分为SiO2 |
C.“奋斗者号”下潜新深度,其钛合金材料中的 位于元素周期表ds区 位于元素周期表ds区 |
| D.“祝融号”探寻新发现,其保温材料纳米气凝胶能产生丁达尔效应 |
您最近半年使用:0次
8 . 设NA表示阿伏加德罗常数,下列说法中不正确的是
| A.一定量的Fe与含1mol HNO3的稀硝酸恰好反应,如还原产物为NO,则被还原的氮原子数小于NA |
| B.1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒 |
| C.常温常压下,NA个臭氧分子的体积大于22.4L |
| D.1.8g水中含有的电子总数为NA |
您最近半年使用:0次
9 . 化学服务于社会,下列有关项目与所述化学知识没有关联的是
选项 | 项目 | 化学知识 |
A | 医院用 作“钡餐” 作“钡餐” |  不溶于酸和水 不溶于酸和水 |
B | 工厂电解熔融 获得铝 获得铝 |  熔点高 熔点高 |
C | 作坊往豆浆中加入石膏制作豆腐 | 石膏能使蛋白质发生盐析 |
D | 利用植物油生产氢化植物油 | 植物油能发生加成反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
10 . 用可溶性 溶液生产纳米
溶液生产纳米 的一种工艺流程如下:
的一种工艺流程如下:
 溶液生产纳米
溶液生产纳米 的一种工艺流程如下:
的一种工艺流程如下: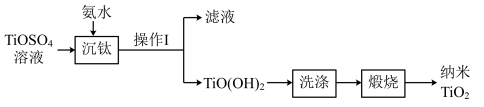
| A.实验室中进行“操作Ⅰ”时,需要的玻璃仪器有烧杯、玻璃棒、普通漏斗 |
B.“沉钛”时反应的离子方程式为: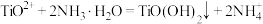 |
C.回收“滤液”中的 时,高温灼烧有利于提高其产率 时,高温灼烧有利于提高其产率 |
D.空气与纳米 所形成的分散系,可检测出有丁达尔效应 所形成的分散系,可检测出有丁达尔效应 |
您最近半年使用:0次


 溶液
溶液



