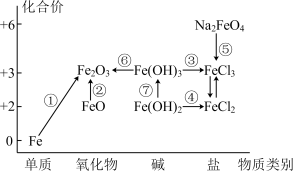
元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的“价一类”二维图,箭头表示部分物质间的转化关系。
(1) 中Fe的化合价为
中Fe的化合价为______________________ 。
(2)磁性氧化铁的化学式为______________________ ,将其完全溶于较浓的盐酸中,其反应的离子方程式为______________________ 。
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
______________________ 。
(4)根据下左图装置,用NaOH 溶液、铁屑、稀 等试剂制备
等试剂制备 沉淀。
沉淀。______________________ 。
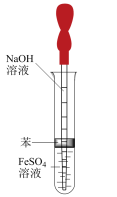
②在I和Ⅱ中加入试剂后,应先______________________ (选填“打开”或“关闭”)止水夹。某同学用上右图装置也可制备 沉淀,原因是
沉淀,原因是______________________ 。
(5)已知 在强碱溶液中稳定存在,pH越小稳定性越差;则制备
在强碱溶液中稳定存在,pH越小稳定性越差;则制备 时需要在
时需要在______________________ (填“酸性”“碱性”或“中性”)环境中进行;  也可以作为净水剂,能与水反应生成具有吸附性的 Fe(OH)₃胶体和一种无色无味气体,写出其中离子方程式:
也可以作为净水剂,能与水反应生成具有吸附性的 Fe(OH)₃胶体和一种无色无味气体,写出其中离子方程式:______________________ 。检验溶液中 的试剂是
的试剂是______________________ 。
(1)
 中Fe的化合价为
中Fe的化合价为(2)磁性氧化铁的化学式为
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(4)根据下左图装置,用NaOH 溶液、铁屑、稀
 等试剂制备
等试剂制备 沉淀。
沉淀。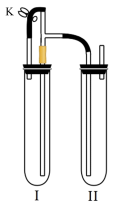
②在I和Ⅱ中加入试剂后,应先
 沉淀,原因是
沉淀,原因是(5)已知
 在强碱溶液中稳定存在,pH越小稳定性越差;则制备
在强碱溶液中稳定存在,pH越小稳定性越差;则制备 时需要在
时需要在 也可以作为净水剂,能与水反应生成具有吸附性的 Fe(OH)₃胶体和一种无色无味气体,写出其中离子方程式:
也可以作为净水剂,能与水反应生成具有吸附性的 Fe(OH)₃胶体和一种无色无味气体,写出其中离子方程式: 的试剂是
的试剂是
更新时间:2024-05-01 14:02:00
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】将饱和FeCl3溶液滴入沸水时,液体变为红褐色,得到的是Fe(OH)3胶体。用此分散系进行实验:
(1)请写出制备Fe(OH)3胶体的化学方程式____________________________________________ 。
(2)证明有Fe(OH)3胶体生成的实验操作是用一束光照射此液体,可以看到有光亮的通路,利用的胶体性质是______________ 。
(3)将Fe(OH)3胶体装入U形管内,用石墨做电极,接通直流电源,通电一段时间后发现阴极附近颜色加深,这种现象叫_____ 。
(4)向Fe(OH)3胶体中逐滴加入稀硫酸,可以看到有红褐色沉淀产生,因为胶体发生了_______ ,继续滴加稀硫酸直至过量,可以看到的实验现象是________________________________________ 。
(1)请写出制备Fe(OH)3胶体的化学方程式
(2)证明有Fe(OH)3胶体生成的实验操作是用一束光照射此液体,可以看到有光亮的通路,利用的胶体性质是
(3)将Fe(OH)3胶体装入U形管内,用石墨做电极,接通直流电源,通电一段时间后发现阴极附近颜色加深,这种现象叫
(4)向Fe(OH)3胶体中逐滴加入稀硫酸,可以看到有红褐色沉淀产生,因为胶体发生了
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】高铁酸钾( ,极易溶于水)是常见的水处理剂,其原理如图所示。
,极易溶于水)是常见的水处理剂,其原理如图所示。
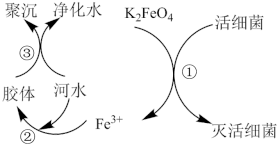
【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
请回答下列问题:
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 价。
(2)过程①中活性菌表现了_______ (填“氧化”或“还原”)性,该过程的还原产物是_______ (填离子符号);过程③属于_______ (填“物理”或“化学”)变化。
(3)根据上述原理分析,作水处理剂时, 的作用有
的作用有_______ 。(填两个)
(4)制备高铁酸钾常用的反应原理为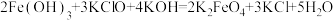 。
。
①通过该反应说明:在碱性条件下,氧化性
_______  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
②将该反应改写为离子方程式:_______ 。
③若该反应中生成2mol ,则电子转移的数目为:
,则电子转移的数目为:_______ 。
 ,极易溶于水)是常见的水处理剂,其原理如图所示。
,极易溶于水)是常见的水处理剂,其原理如图所示。
【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
请回答下列问题:
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)过程①中活性菌表现了
(3)根据上述原理分析,作水处理剂时,
 的作用有
的作用有(4)制备高铁酸钾常用的反应原理为
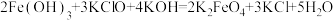 。
。①通过该反应说明:在碱性条件下,氧化性

 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。②将该反应改写为离子方程式:
③若该反应中生成2mol
 ,则电子转移的数目为:
,则电子转移的数目为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】请回答下列问题:
(1)现有下列物质,请用序号填空:①氧化钠固体 ②胆矾晶体 ③熔融氯化钠 ④稀盐酸 ⑤氨水 ⑥蔗糖 ⑦二氧化碳。上述状态下可导电的是_______ 。属于强电解质的是_______ 。
(2)向50ml沸水中加入5~6滴饱和FeCl3溶液,加热至产生红褐色液体,停止加热,利用_______ 来证明得到的分散系是氢氧化铁胶体。
(3)NaHSO4 固体溶于水的电离方程式为_______ ;
(4)写出硫酸铁和氢氧化钡溶液反应的离子方程式为_______ 。
(5)A、B、C、D为四种可溶性的盐,它们包含的阳离子和阴离子分别为Ba2+、Ag+、Na+、Cu2+和NO 、SO
、SO 、Cl-、CO
、Cl-、CO (离子在物质中不能重复出现)。
(离子在物质中不能重复出现)。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据实验事实可推断它们的化学式为:C_______ ,D_______ ;A溶液中阴离子的检验方法_______ 。
(1)现有下列物质,请用序号填空:①氧化钠固体 ②胆矾晶体 ③熔融氯化钠 ④稀盐酸 ⑤氨水 ⑥蔗糖 ⑦二氧化碳。上述状态下可导电的是
(2)向50ml沸水中加入5~6滴饱和FeCl3溶液,加热至产生红褐色液体,停止加热,利用
(3)NaHSO4 固体溶于水的电离方程式为
(4)写出硫酸铁和氢氧化钡溶液反应的离子方程式为
(5)A、B、C、D为四种可溶性的盐,它们包含的阳离子和阴离子分别为Ba2+、Ag+、Na+、Cu2+和NO
 、SO
、SO 、Cl-、CO
、Cl-、CO (离子在物质中不能重复出现)。
(离子在物质中不能重复出现)。①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据实验事实可推断它们的化学式为:C
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有五瓶损坏标签的试剂,分别盛有硫酸溶液、氢氧化钾溶液、硝酸钡溶液、碳酸氢钠溶液、氯化铜溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E。观察发现,C试剂颜色为蓝色,其余为无色;四种无色试剂A、B、D、E用小试管各取少量,两两相互滴加,反应现象为:A与其余三种混合无明显现象,B与D出现白色沉淀,B与E无明显现象,D与E混合有气泡产生;A与C混合有蓝色沉淀。由此,可判定各试剂瓶中所盛试剂为(用主要成分的化学式表示):
(1)A____________ ,B____________ ,C____________ ,D____________ ,E____________ 。
(2)另外,请写出下面的离子方程式:
①B与D:_____________________________________________ 。
②D与E:______________________________________________ 。
③A与C:_____________________________________________ 。
(1)A
(2)另外,请写出下面的离子方程式:
①B与D:
②D与E:
③A与C:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】硒(Se)是动物体必需的营养元素。也可用作光敏材料、电解锰的催化剂。
(1)硒是第34号元素,在元素周期表中位于第四周期ⅥA族,则其原子结构示意图为___________ 。
(2)硒与碲为伴生元素,其矿物经处理后可获得SeO2和TeO2的混合物,二者的物理性质如下表。则分离该混合物最适宜的方法是___________ 。
(3)已知常温下亚硒酸和硒酸的电离常数如下表:
①亚硒酸中硒元素的化合价为___________ 。
②亚硒酸的二级电离常数Ka2=___________ (写出表达式),从结构与性质的关系解释,亚硒酸的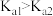 的原因是
的原因是___________ 。
③亚硒酸溶液中通入SO2可发生反应制取硒单质,反应的离子方程式为___________ 。
④电解亚硒酸溶液可制得硒酸,则电解时阳极的电极反应式为___________ 。
⑤亚硒酸钠溶液中滴加少量硒酸氢钠溶液,反应的离子方程式为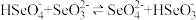 ,此反应的平衡常数K=
,此反应的平衡常数K=___________ 。
(1)硒是第34号元素,在元素周期表中位于第四周期ⅥA族,则其原子结构示意图为
(2)硒与碲为伴生元素,其矿物经处理后可获得SeO2和TeO2的混合物,二者的物理性质如下表。则分离该混合物最适宜的方法是
| 物质 | 熔点/℃ | 沸点/℃ | 升华/℃ | 溶解性 |
| SeO2 | 340 | 684 | 315 | 易溶于水 |
| TeO2 | 733 | 1260 | 450 | 微溶于水 |
(3)已知常温下亚硒酸和硒酸的电离常数如下表:
| 名称 | 分子式 | Ka1 | Ka2 |
| 亚硒酸 | H2SeO3 | 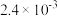 | 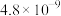 |
| 硒酸 | H2SeO4 | 完全电离 |  |
①亚硒酸中硒元素的化合价为
②亚硒酸的二级电离常数Ka2=
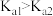 的原因是
的原因是③亚硒酸溶液中通入SO2可发生反应制取硒单质,反应的离子方程式为
④电解亚硒酸溶液可制得硒酸,则电解时阳极的电极反应式为
⑤亚硒酸钠溶液中滴加少量硒酸氢钠溶液,反应的离子方程式为
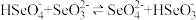 ,此反应的平衡常数K=
,此反应的平衡常数K=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】目前,世界上多采用电解熔融氯化钠的方法来生产金属钠: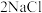 (熔融)
(熔融)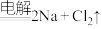 。已知A、B、C、D、E、F有如图转化关系。
。已知A、B、C、D、E、F有如图转化关系。 化学方程式:
化学方程式:___________ 。
(2)C电离方程式___________ 。
(3)E和F生成 离子方程式
离子方程式___________ 。
(4)工业生产中常利用B与 反应来制备漂白粉,写出反应的化学方程式
反应来制备漂白粉,写出反应的化学方程式___________ 。
(5)检验D溶液中含有 的方法是
的方法是___________ 。
(6)若向E溶液中继续通入 ,写出反应的化学方程式
,写出反应的化学方程式___________ 。
(7)若把A投入盛有D的溶液中,写出总反应的离子方程式___________ 。
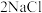 (熔融)
(熔融)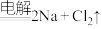 。已知A、B、C、D、E、F有如图转化关系。
。已知A、B、C、D、E、F有如图转化关系。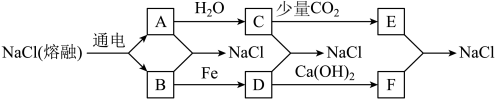
 化学方程式:
化学方程式:(2)C电离方程式
(3)E和F生成
 离子方程式
离子方程式(4)工业生产中常利用B与
 反应来制备漂白粉,写出反应的化学方程式
反应来制备漂白粉,写出反应的化学方程式(5)检验D溶液中含有
 的方法是
的方法是(6)若向E溶液中继续通入
 ,写出反应的化学方程式
,写出反应的化学方程式(7)若把A投入盛有D的溶液中,写出总反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】锰及其化合物在生产生活中有许多用途。在实验室中模拟工业利用软锰矿(主要成分为MnO2,含少量SiO2、Fe2O3和Al2O3等)制备金属锰等物质,设计流程如下:
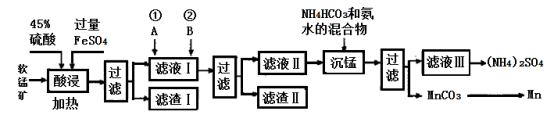
已知:Mn2+有较强的还原性,在空气中能被氧气氧化,碳酸锰在空气中高温加热固体产物为Mn2O3;部分氢氧化物的Ksp(近似值)如下表。
(1)“酸浸”前需将软锰矿粉碎的目的是______________________ ;酸浸过程MnO2发生反应的离子方程式为____________________________________________ 。
(2)向滤液I中需先加A物质,再加B物质,若加入的物质均为非金属化合物的溶液,则A为___________ ,B为___________ 。滤渣I的成分是___________ 。
(3)“酸浸”需适宜的酸浓度、液固比、酸浸温度等,其中浸取率随酸浸时间的变化如图所示:
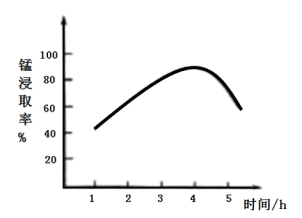
当浸取时间超过4h时,锰浸取率反而减小,其原因是______________________________ 。
(4)加入B调节溶液pH,则PH的理论最小值为___________ 。(已知:当某种离子浓度小于1×10-5 mol/L时,可认为其沉淀完全。结果保留两位小数)
(5)“沉锰”过程中加入氨水的目的是(从化学平衡移动的角度解释)____________________ 。
(6)写出由MnCO3和金属铝为原料制备金属锰的过程中所涉及的化学方程式:____________________________ 、_____________________________________ 。

已知:Mn2+有较强的还原性,在空气中能被氧气氧化,碳酸锰在空气中高温加热固体产物为Mn2O3;部分氢氧化物的Ksp(近似值)如下表。
| 物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
| Ksp | 10-13 | 10‑17 | 10-39 | 10-33 |
(1)“酸浸”前需将软锰矿粉碎的目的是
(2)向滤液I中需先加A物质,再加B物质,若加入的物质均为非金属化合物的溶液,则A为
(3)“酸浸”需适宜的酸浓度、液固比、酸浸温度等,其中浸取率随酸浸时间的变化如图所示:

当浸取时间超过4h时,锰浸取率反而减小,其原因是
(4)加入B调节溶液pH,则PH的理论最小值为
(5)“沉锰”过程中加入氨水的目的是(从化学平衡移动的角度解释)
(6)写出由MnCO3和金属铝为原料制备金属锰的过程中所涉及的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】新型电池在飞速发展的信息技术中发挥着越来越重要的作用。Li2FeSiO4是极具发展潜力的新型锂离子电池电极材料,在苹果的几款最新型的产品中已经有了一定程度的应用。其中一种制备Li2FeSiO4的方法为:固相法:2Li2SiO3+FeSO4 Li2FeSiO4+Li2SO4+SiO2
Li2FeSiO4+Li2SO4+SiO2
某学习小组按如下实验流程制备Li2FeSiO4并测定所得产品中Li2FeSiO4的含量。
实验(一)制备流程:
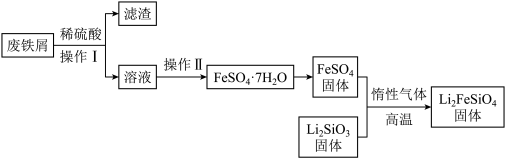
实验(二)Li2FeSiO4含量测定:
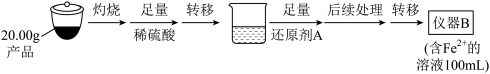
从仪器B中取20.00mL溶液至锥形瓶中,另取0.2000mol·Lˉ1的酸性KMnO4标准溶液装入仪器C中,用氧化还原滴定法测定Fe2+含量。相关反应为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,杂质不与酸性KMnO4标准溶液反应。经4次滴定,每次消耗KMnO4溶液的体积如下:
(1)实验(二)中的仪器名称:仪器B__ ,仪器C__ 。
(2)制备Li2FeSiO4时必须在惰性气体氛围中进行,其原因是__ 。
(3)操作Ⅱ的步骤__ ,在操作Ⅰ时,所需用到的玻璃仪器中,除了普通漏斗、烧杯外,还需__ 。
(4)还原剂A可用SO2,写出该反应的离子方程式__ ,此时后续处理的主要目的是__ 。
(5)滴定终点时现象为__ ;根据滴定结果,可确定产品中Li2FeSiO4的质量分数为_ 。
 Li2FeSiO4+Li2SO4+SiO2
Li2FeSiO4+Li2SO4+SiO2某学习小组按如下实验流程制备Li2FeSiO4并测定所得产品中Li2FeSiO4的含量。
实验(一)制备流程:

实验(二)Li2FeSiO4含量测定:

从仪器B中取20.00mL溶液至锥形瓶中,另取0.2000mol·Lˉ1的酸性KMnO4标准溶液装入仪器C中,用氧化还原滴定法测定Fe2+含量。相关反应为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,杂质不与酸性KMnO4标准溶液反应。经4次滴定,每次消耗KMnO4溶液的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗KMnO4溶液体积 | 20.00mL | 19.98mL | 21.38mL | 20.02mL |
(2)制备Li2FeSiO4时必须在惰性气体氛围中进行,其原因是
(3)操作Ⅱ的步骤
(4)还原剂A可用SO2,写出该反应的离子方程式
(5)滴定终点时现象为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】化学实验小组的同学们进入四川博物馆,看到许多矿石标本,其中三种矿石及其主要成分如下:

回答下列问题:
(1)加热条件下,1mol氨气与足量孔雀石反应可以产生1.5mol金属铜,发生反应的化学方程式为__ 。
(2)辉铜矿石主要含有硫化亚铜(Cu2S)和少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如图:
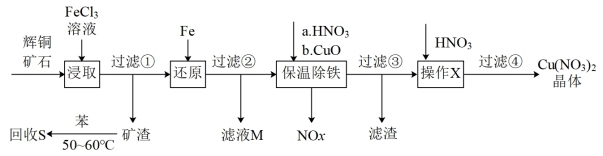
①回收S,温度控制在50℃~60℃之间,温度不宜过高或过低的原因分别是___ 、___ 。
②气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该物质的化学式为__ ;向滤液M中加入(或通入)下列__ (填正确答案标号)物质,可得到另一种可循环利用的物质。
A.铁 B.氯气 C.高锰酸钾 D.盐酸
③保温除铁过程中加入CuO的作用是__ 。
④操作X中硝酸溶液的作用是__ 。
(3)已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度的升高而减少,如图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线。则:
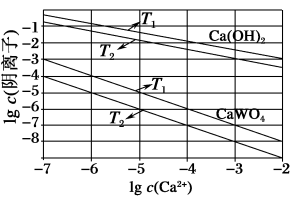
①T1___ T2(填“>”或“<”);T1时,Ksp(CaWO4)=___ 。
②向钨酸钠溶液中加入石灰乳得到大量钨酸钙,发生反应的离子方程式为___ 。

回答下列问题:
(1)加热条件下,1mol氨气与足量孔雀石反应可以产生1.5mol金属铜,发生反应的化学方程式为
(2)辉铜矿石主要含有硫化亚铜(Cu2S)和少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如图:

①回收S,温度控制在50℃~60℃之间,温度不宜过高或过低的原因分别是
②气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该物质的化学式为
A.铁 B.氯气 C.高锰酸钾 D.盐酸
③保温除铁过程中加入CuO的作用是
④操作X中硝酸溶液的作用是
(3)已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度的升高而减少,如图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线。则:

①T1
②向钨酸钠溶液中加入石灰乳得到大量钨酸钙,发生反应的离子方程式为
您最近一年使用:0次



